Гідратний шар
Гідратний шар (рос. гидратный слой, англ. hydrate layer, нім. Hydratschicht f) — тонкий шар, утворений орієнтованими молекулами води біля границі розділу фаз внаслідок гідратації мінералу (повітряної бульбашки).
Загальний опис
Вода в гідратному шарі має аномальні властивості: підвищену в'язкість, знижену розчинність, знижену дифузію розчинених речовин та ін. Наявлість гідратного шару визначає його технологічні властивості у фізико-хімічних процесах збагачення — флотації, масляній та полімерній агрегації тощо.
Присутність твердої фази обумовлює підвищення ступеня впорядкованості в прилеглих елементарних водних шарах за рахунок її орієнтуючого впливу. Останнє викликане міжмолекулярними ван-дер-ваальсовими силами (дисперсійними, орієнтаційними й індукційними), а також водневими зв'язками. При цьому поблизу гідрофобної поверхні молекули води орієнтуються паралельно їй, а поблизу гідрофільної нормально. Останній варіант забезпечує щільнішу упаковку молекул в прилеглих мономолекулярних шарах, очевидно, до відстані між молекулами води 0,3 нм, менше якого починають переважати сили відштовхування електронних хмар сусідніх молекул, що перекриваються. Істотний вплив на структуру води поблизу твердої поверхні здійснюють розчинені речовини. Наприклад, підвищення концентрації електроліту руйнує структуру води поблизу твердої гідрофільної поверхні. Крім того, електроліти формують подвійний електричний шар (ПЕШ), який багато в чому визначає характер і інтенсивність міжфазних взаємодій. Для опису аномальних властивостей рідини в пристінному просторі і між обмежуючими поверхнями (в порах, капілярах і т. д.) Б. В. Дерягіним і його школою було введено поняття «розклинюючого тиску». Товщина структурованих пристінних шарів води може досягати декількох десятків нм.
Особливі випадки
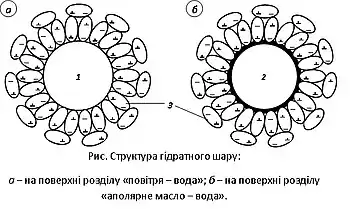
Аномальні властивості характерні і для границі розділу «вода-газ». Молекули води тіт орієнтуються атомами оксигену (кисню) у бік газової фази, утворюючи ПЕШ, який цілком розташовується в рідині. Присутність розчинених речовин як у вигляді йонів, так і недисоційованих молекул приводить до зміни структури поверхневого шару, поверхневого потенціалу і натягу.
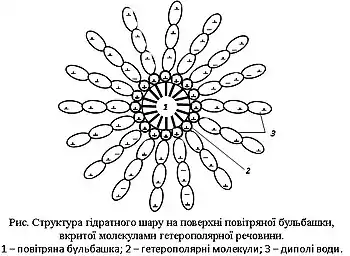
Значні зміни полярності поверхні й структури гідратних шарів спостерігаються при закріпленні (адсорбції) на бульбашці гетеропо-лярних молекул, які мають аполярний (вуглеводневий) радикал і полярну групу. Адсорбція таких молекул супроводжується вирівнюван-ням полярностей дотичних фаз і внаслідок цього зниженням вільної поверхневої енергії системи в результаті особливої орієнтації гетеро-полярних молекул на межі розділу «газ — рідина». Полярною части-ною вони будуть звернені до полярної рідини — води, аполярним ра-дикалом — до повітря. Таке розташування гетерополярних молекул на межі розділу фаз обумовлено тим, що диполі води, що активно взає-модіють з полярними групами молекул, практично не взаємодіють з аполярними (вуглеводневими) групами радикалу і прагнуть немовби виштовхнути їх у повітряну фазу. При малій кількості гетерополяр-них молекул на поверхні вони розташовуватимуться майже у пло-щині поверхневого шару, а при великій кількості — перпендикулярно поверхні розділу «повітря — вода», тобто займатимуть положення, яке відповідає мінімальному значенню вільної поверхневої енергії. Однак така орієнтація гетерополярних молекул призводить до поляризації поверхні бульбашки і однакової орієнтації молекул води, яка поширюватиметься, поступово слабшаючи, у глибину рідини, поки не порушиться тепловим рухом. У результаті цього навколо бульбашки може утворитися значний за товщиною (до 10–5 см) гідратний шар (рис.).
Аналогічне явище в присутності гетерополярних молекул спостерігається також на поверхні розділу «крапля аполярного масла — вода» або «повітряна бульбашка покрита маслом — вода», оскільки у даному випадку не існує принципової різниці між повітряною бульбашкою і краплиною аполярного масла. Адсорбція гетерополярних молекул зменшує ступінь гідрофобності поверхні розділу «аполярне масло — вода».
Утворення товстих гідратних шарів навколо бульбашок і крапель приводить:
– по-перше, до зростання жорсткості їхньої поверхні та наближення її форми до сферичної. Оскільки сфера є однією з найменш вигідних у гідродинамічному відношенні форм, швидкість підйому бульбашок і крапель при цьому зменшиться, а тривалість перебування їх у пульпі збільшиться;
– по-друге, наявність гідратних шарів на поверхні бульбашок і крапель утруднює їхню коалесценцію. Термодинамічна ймовірність її може бути реалізована тільки за певних витрат енергії активації, необхідної для руйнування гідратних шарів, наприклад, за рахунок кінетичної енергії зіткнення бульбашок або крапель.
Усе це спричиняє збільшення концентрації і стійкості бульба-шок та крапель аполярних масел у пульпі.
Література
- Эйзенберг Д., Кауцман В. Структура и свойства воды. — Ленинград: Гидрометеоиздат. — 1975. — 280 с.
- Смирнов В. О., Білецький В. С. Флотаційні методи збагачення корисних копалин. Донецьк: Східний видавничий дім, НТШ-Донецьк — 2010. — 496 стор.
- Антонченко В. Я. Физика воды. — К.: Наукова думка, — 1986. — 127 с.
- Дерягин Б. В., Овчаренко Ф. Д., Чураев Н. В. Вода в дисперсных системах. — Москва: Химия, 1989.
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2004. — Т. 1 : А — К. — 640 с. — ISBN 966-7804-14-3.
