Дифузія
Дифу́зія (лат. diffusio — поширення, розтікання, розсіювання, взаємодія) — процес взаємного проникнення молекул або атомів однієї речовини поміж молекул або атомів іншої, що зазвичай приводить до вирівнювання їх концентрацій у всьому займаному об'ємі.
У деяких ситуаціях одна з речовин уже має вирівняну концентрацію, і говорять про дифузію одної речовини в іншій. При цьому зазвичай перенесення речовини відбувається з області з високою концентрацією в область з низькою концентрацією (вздовж вектора градієнта концентрації).
Прикладом дифузії може служити перемішування газів (наприклад, поширення запахів) або рідин (якщо у воду капнути чорнила, то рідина через деякий час стане рівномірно пофарбованою). Інший приклад пов'язаний з твердим тілом: атоми дотичних металів перемішуються на межі дотику. Важливу роль дифузія частинок грає у фізиці плазми.
Зазвичай під дифузією розуміють процеси, що супроводжуються перенесенням речовини, однак іноді дифузійними називають також інші процеси перенесення: теплопровідність, в'язке тертя тощо.
Швидкість дифузії залежить від багатьох факторів. Так, у разі металевого стрижня дифузія тепла проходить дуже швидко. Якщо ж стрижень виготовлений з синтетичного матеріалу, дифузія тепла протікає повільно. Дифузія молекул в загальному випадку протікає ще повільніше. Наприклад, якщо шматочок цукру опустити на дно склянки з водою, і воду не перемішувати, то пройде кілька тижнів, перш ніж розчин стане однорідним. Ще повільніше відбувається дифузія однієї твердої речовини в іншу. Наприклад, якщо мідь покрити золотом, то буде відбуватися дифузія золота в мідь, але при нормальних умовах (кімнатна температура і атмосферний тиск) золотовмісний шар досягне товщини в кілька мікронів тільки через кілька тисяч років. Інший приклад: на золотий злиток був покладений злиток свинцю, і під вантажем за п'ять років свинцевий злиток проникнув в золотий злиток на сантиметр.
Кількісно опис процесів дифузії дав німецький фізіолог Адольф Фік у 1855 р.
Загальна інформація
Дифузія — один із ступенів численних технологічних процесів фізичної хімії (адсорбції, сушки, екстрагування, брикетування з в'яжучими речовинами, тощо). Дифузія відбувається в газах, рідинах і твердих тілах. Механізм дифузії в цих речовинах істотно різний. Дифузія що відбувається внаслідок теплового руху атомів, молекул, — молекулярна дифузія. Дифундувати можуть як частинки сторонніх речовин (домішок), нерівномірно розподілених у середовищі, так і частинки самої речовини середовища. У останньому випадку процес називається самодифузією. Термодифузія — це дифузія під дією градієнта температури в об'ємі тіла, бародифузія — під дією градієнта тиску або гравітаційного поля. Перенесення заряджених частинок під дією зовнішнього електричного поля — електродифузія. У рухомому середовищі може виникати конвекційна дифузія, при вихровому русі газу або рідини — турбулентна дифузія.
Наслідком дифузії є переміщення часток із областей, де їхня концентрація висока, в області, де їхня концентрація низька, тобто вирівнювання концентрації часток у термодинамічній системі, встановлення рівноваги за складом.
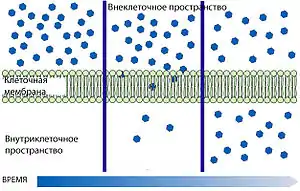
Дифузія дуже розповсюджене явище, яке відіграє велику роль у функціонуванні живих організмів. У легенях молекули кисню дифундують у кровоносні судини, завдяки процесам дифузії відбувається обмін речовин у клітинах.
Дифузія широко використовується у техніці. Наприклад, робота біполярного транзистора основана на дифузії неосновних носіїв заряду через p-n перехід. Вибіркове перенесення певних компонентів у пори речовини — інфільтраційна дифузія. Дифузія має особливе значення в шахтах, де вона сприяє рівномірному розподілу шкідливих газів в атмосфері гірн. виробок, попередженню їх небезпечних скупчень. Суттєве значення відіграє дифузія в технологічних процесах при застосуванні реагентів. Різні речовини дифундують з різною швидкістю, що залежить від молекулярної маси речовини. Цей факт використовується для розділення ізотопів.
У загальному випадку можна сказати, що темп дифузії пропорційний швидкості молекул (яка, в свою чергу, пропорційна температурі і обернено пропорційна масі молекул), а також пропорційний площі перерізу зразка.
Математичний опис
Дифузійний потік
Дифузійним потоком або густиною дифузійного потоку j називають кількість речовини, що проходить через одиницю площі за одиницю часу. Ця величина дорівнює
- .
тобто, потік пропорційний градієнту концентрації (перший закон Фіка). Знак мінус показує, що дифузія відбувається у напрямку, протилежному до зростання градієнту. Величина називається коефіцієнтом дифузії, і є мірою дії середовища на частинки. Фізичний сенс коефіцієнта дифузії: це кількість речовини, що проходить через ділянку в 1 м2 при градієнті концентрації речовини у 1 моль/м3 на метр.
Рівняння дифузії
З рівняння неперервності (яке можна розуміти як закон збереження кількості частинок) можна вивести рівняння дифузії
а використавши вираз для густини потоку, можна отримати феноменологічне рівняння дифузії
- ,
що у випадку незмінного D перетворюється на другий закон Фіка:
- ,
де — оператор Лапласа.[1]
У більш загальному випадку систем часток, які взаємодіють між собою рівняння дифузії записується у вигляді:
- ,
де μ — хімічний потенціал а f — інтенсивність джерел речовини. Це рівняння виражає той факт, що умовою рівноваги за складом є рівність хімічного потенціалу у всій термодинамічній системі, а вирівнювання концентрації — це лише частковий випадок для однорідних систем, близьких до ідеального газу.
У найпростішому випадку розглядається одновимірна система з початковою концентрацією заданою дельта-функцією[2], що відповідає одноразовому миттєвому внесенню дифундуючої речовини у середовище (наприклад, крапля чорнил, що потрапляє всередину трубки з водою)
У випадку довільної початкової функції ,
- , де
де <math}\xi</math> — поточна координата інтегрування. Таке рівняння називається фундаментальним розв'язком рівняння дифузії при заданих початкових умовах.
Більш складні випадки включають коефіцієнт дифузії, що залежить від часу, температури або концентрації дифундуючої речовини, змінну геометрію середовища, хімічні реакції між речовиною і середовищем, тощо.[3]З математичної точки зору, рівняння дифузії є частковим випадком рівняння Нав'є — Стокса. Також, у загальному вигляді, вони є аналогічними рівнянням теплопровідності.
Випадкові блукання
При дифузії кожна частинка речовини рухається хаотично під дією оточуючих її частинок. Цей рух є аналогічним броунівському, а тому має аналогічні характеристики. Для частки характерна пропорційність середнього зміщення квадратному кореню з часу.
- ,
де , , — координати частки в момент часу t, , , — її координати в початковий момент часу. Це співвідношення дозволяє ввести кількісну характеристику дифузії — коефіцієнт дифузії D:
- .
Види дифузії
Дифузія в газах
В газах швидкість дифузії залежить від середньої довжини вільного пробігу (обернено пропорційна тиску) і швидкості молекул (пропорційна ). Дифузія у плазмі подібна до дифузії у газах, але її опис містить у собі дію електричних і магнітних полів. Рух електронів у напівпровідниках може розглядатись як дифузія електронного газу, з урахуванням електромагнітної самодії заряду.[4] У випадку дифузії домішок із низькою концентрацією, маса частинок яких менша за масу частинок газу-середовища, можна вивести більш точну формулу для коефіцієнта дифузії: , де λ — середня довжина вільного пробігу частинки.[5]
У випадку більш важких домішок потрібно враховувати, що під λ насправді мається на увазі ефективна довжина пробігу — середня відстань, пролетівши яку частинка суттєво змінює свій напрям руху. У випадку домішок, що значно важчі за середовище, ця відстань у більша за довжину вільного пробігу.[5]
Дифузія в рідинах
Дифузія у рідинах є значно складнішою за дифузію у газах через відсутність у рідинах вільного пробігу молекул. У найпростішому варіанті опису, рідина розглядається як квазістаціонарна система, молекули якої час від часу роблять «стрибки» з одного стану в інший. У такому разі, замість вільного пробігу, система характеризується середнім періодом спокою τ0. Шанс зробити стрибок з одного стану в інший залежить від різниці потенційних енергій у цих станах, тому , де W — енергія активації. У такому варіанті коефіцієнт дифузії можна виразити як , де d — середня відстань між частинками рідини. Зі збільшенням температури, d зростає, а τ стрімко падає, тому загалом D зростає експоненційно.[4]
Дифузія в твердих тілах
У твердих тілах дифузія відбувається завдяки дефектам кристалічної ґратки, переміщенню атомів між її вузлами або обміну місцями сусідніх атомів. Швидкість дифузії у твердих тілах залежить від кількості дефектів у ґратці. Також, як і в рідинах, коефіцієнт дифузії експоненційно зростає з температурою, але значно швидше — наприклад, швидкість дифузії цинку в міді при підвищенні температури з 30 до 300 °C зростає в 1014 разів.[4].
Подібно до рідин, коефіцієнт дифузії у твердих тілах можна виразити як , де a — стала ґратки.
При контакті двох твердих речовин, коефіцієнт дифузії першої речовини в другу може відрізнятися від коефіцієнта дифузії другої в першу. Через це, у більш швидкодифундуючій речовині можуть утворюватись пори. Це явище називається ефектом Кіркендала[6]
Див. також
Примітки
- Уравнениия математической физики(рос.)
- Уравнение диффузии(рос.)
- ОСНОВНЫЕ ЗАКОНЫ ДИФФУЗИИ(рос.)
- диффузия(рос.)
- Диффузия(рос.)
- Механизмы диффузии(рос.)
