Вольфрамати
Вольфрамат — хімічна сполука, яка містить оксоаніон вольфраму або є змішаним оксидом, що містить вольфрам. Вольфрамати — солі вольфрамових кислот. Найпростіший іон вольфраму - , «ортовольфрамат».[1] Багато інших вольфраматів належать до великої групи багатоатомних іонів, які називаються поліоксометалатами («POMs») і конкретно називаються ізополіоксометалатами, оскільки вони містять поряд з киснем і, можливо, воднем, лише один інший елемент. Майже всі корисні вольфрамові руди є вольфраматами.
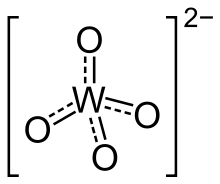
Структури
Ортовольфрамати мають стійку кристалічну структуру на основі тетраедричної групи з короткими відстанями W–O 1,79 Å. Структурно вони подібні до сульфатів. У поліоксовольфраматах переважають шестикоординатні октаедрічні групи. У цих сполуках відстані W–O подовжені.[1]
Деякі приклади іонів вольфрамату:[2]
Поширення в природі
Вольфрамати утворюються природним шляхом разом з молібдатами. Мінерал шеєліт, вольфрамат кальцію, часто містить домішки молібдатів; мінерал вольфраміт є вольфраматом марганцю та заліза — обидва є цінними рудними мінералами вольфраму. Повеліт — мінеральна форма молібдата кальцію, що містить невелику кількість вольфраму.
Реакції
Розчини вольфраматів, як і молібдати, дають інтенсивно сині розчини складного вольфрамату (V, VI), подібні до молібденової сині.[1]
На відміну від хроматів, вольфрамати не є хорошими окисниками, але, подібно до хроматів, розчини вольфраматів конденсуються із утворенням при підкисленні ізополівольфраматів.
Примітки
- Egon Wiberg, Arnold Frederick Holleman (2001). Inorganic Chemistry. Elsevier. ISBN 0-12-352651-5.
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (вид. 2nd). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- Jon A. McCleverty, N. G. Connelly,Nomenclature of inorganic chemistry II: recommendations 2000, International Union of Pure and Applied Chemistry Commission on the Nomenclature of Inorganic Chemistry, Published by Royal Society of Chemistry, 2001, ISBN 0-85404-487-6
