Торсійний кут зв'язку
Торсíйний кут зв'язку́ (рос. торсионный угол связи, англ. torsion bond angle), також діедральний кут між зв'язками — двогранний кут між площиною, в якій лежать атоми A, B і C молекули A-B-C-D, та площиною, в якій лежать атоми B, C, D. У проекції Ньюмена це кут (від 0° до 180°) між зв'язками, що йдуть до двох специфічних (фідусіальних) груп: один від атома, який розташований ближче (проксимальний), а інший від атома, що розташований далі (дистальний). Кут між A та D є додатним, якщо зв'язок А–В повертається за годинниковою стрілкою менш, ніж на 180° для того, щоб він міг затулити зв'язок C–D, від'ємний кут означає обертання в протилежну сторону.
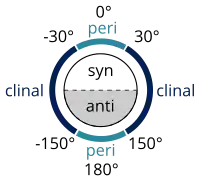
Стереохімічні розташування з торсійним кутом між 0 і ±90° мають назву син- (s), між ±90° і 180° — анти- (a), між 30° і 150° або між –30° і –150° — клінальні (c) (clinal), між 0° і 30° або між 150° і 180° — перипланарні (p) (periplanar). Два типи термінів можуть комбінуватись так, щоб вони визначали чотири області торсійного кута: 0° до 30° — синперипланарні (sp) (synperiplanar) (також мають назву син- або цис-конформації), 30° до 90° та –30° до –90° — синклінальні (sc) (synclinal) (також мають назву гош (gauche) або скошені (skew) конформації), 90° до 150° та –90° до 150° — антиклінальні (ac) (anticlinal), ±150° до 180° — антиперипланарні (ap) (antiperiplanar) (також мають назву анти- або транс-конформації).
Для макромолекул використовуються символи T, C, G+, G–, A+, A– (відповідно ap, sp, +sc, –sc, +ac, –ac).
Джерела
- Глосарій термінів з хімії / уклад. Й. Опейда, О. Швайка ; Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Дон. : Вебер, 2008. — 738 с. — ISBN 978-966-335-206-0.