Флороглюцинол
Флороглюцинол (систематична назва бензен-1,3,5-триол) — органічна сполука, якій властива кето-енольна таутомерія. Енольна форма належить до класу фенолів, а кетонна — до класу циклічних кетонів (циклогаксан-1,3,5-трион).
| Структурна формула | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| Загальна інформація | |||||||||||||||||||||||||
| Преференційна назва ІЮПАК | |||||||||||||||||||||||||
| Систематична назва ІЮПАК | Бензен-1,3,5-триол[1] | ||||||||||||||||||||||||
| Інші назви |
Флороглюцин, флороглюцинол, 1,3,5-тригідроксибензен | ||||||||||||||||||||||||
| Хімічна формула | C6H6O3 | ||||||||||||||||||||||||
| 3D Структура (JSmol) | Інтерактивне зображення | ||||||||||||||||||||||||
| Зовнішні ідентифікатори / Бази даних | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Властивості | |||||||||||||||||||||||||
| Молярна маса | 126.031694 г/моль[1] | ||||||||||||||||||||||||
| Агрегатний стан |
Твердий[1] | ||||||||||||||||||||||||
| Температура плавлення |
218,5 °C[1] | ||||||||||||||||||||||||
| Розчинність |
10,6 г/л (20 °C)[1] | ||||||||||||||||||||||||
| Безпека | |||||||||||||||||||||||||
| Маркування згідно системі УГС
Увага | |||||||||||||||||||||||||
| H-фрази | H: H315, H317, H319, H335, H341, H361[1] | ||||||||||||||||||||||||
| P-фрази | P: P201, P202, P261, P264, P271, P272, P280, P281, P302+P352, P304+P340, P305+P351+P338, P308+P313, P312, P321, P332+P313, P333+P313, P337+P313, P362, P363, P403+P233, P405, P501[1] | ||||||||||||||||||||||||
| LD50 |
4000 мг/кг (щур, орально)[1] | ||||||||||||||||||||||||
| Наскільки це можливо, значення величин подані в одиницях системи SI. Якщо не вказано іншого, усі дані відносяться до стандартного стану. | |||||||||||||||||||||||||
Отримання
Отримують відновленням 1,3,5-тринітробензену з подальшим гідролізом:
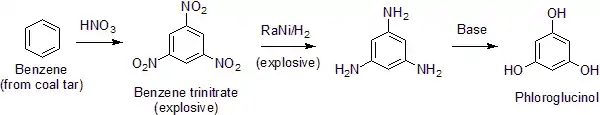
Тринітробензен одержують з тринітротолуену (окиснення CH3 до COOH, далі декарбоксилювання), оскільки через електродонорний ефект метильної групи толуен нітрується легше, ніж бензен[2].
Також отримують окисненням 1,3,5-триізопропілбензену[2]:
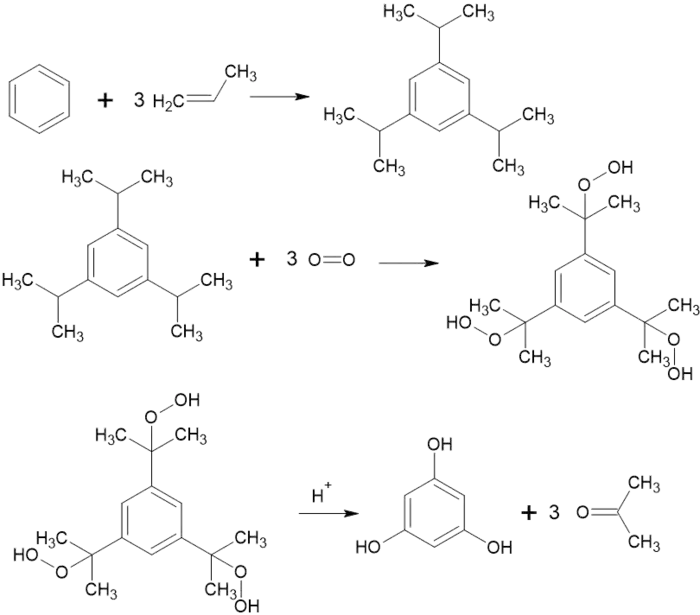
Ще один спосіб отримання — з триаміду бензентрикарбонової кислоти (перегрупування Гофмана, далі гідроліз)[2].
Хімічні властивості
Проявляє кето-енольну таутомерію і може вступати в реакції в обох формах. Наприклад, O-алкілювання (енольна форма) та взаємодія з гідроксиламіном (кетонна форма)[2]. Гідроксильні групи в енольній формі проявляють кислотні властивості і можуть відщеплювати протони, утворюючи моно-, ди- та трианіони[3].
В нейтральному середовищі енольна форма сильно переважає, а в лужному утворюється діаніон, який містить одну кетонну групу і дві депротоновані енольні[3].
Для енольної форми також характерні реакції електрофільного заміщення в ароматичномум кільці[2].
Джерела
Література
- Ластухін Ю. О., Воронов С. А. Органічна хімія : підручник. — Вид. 3-тє, стереотипне. — Львів : Центр Європи, 2006. — ISBN 966-7022-19-6.
Посилання
- PubChem. Phloroglucinol. pubchem.ncbi.nlm.nih.gov (англ.). Процитовано 10 грудня 2020.
- Fiege, Helmut; Voges, Heinz-Werner; Hamamoto, Toshikazu; Umemura, Sumio; Iwata, Tadao; Miki, Hisaya; Fujita, Yasuhiro; Buysch, Hans-Josef та ін. (15 червня 2000). У Wiley-VCH Verlag GmbH & Co. KGaA. Phenol Derivatives. Ullmann's Encyclopedia of Industrial Chemistry (англ.). Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. с. a19_313. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a19_313.
- Lohrie, Martin; Knoche, Wilhelm (1993-02). Dissociation and keto-enol tautomerism of phloroglucinol and its anions in aqueous solution. Journal of the American Chemical Society (англ.) 115 (3). с. 919–924. ISSN 0002-7863. doi:10.1021/ja00056a016. Процитовано 11 грудня 2020.

