ДНК-полімераза
ДНК-полімераза — це фермент, що бере участь у реплікації ДНК. Ферменти цього класу каталізують полімеризацію дезоксирибонуклеотидів уздовж ланцюжка ДНК, який фермент «зчитує» і використовує як шаблон. Тип нового нуклеотиду визначається за принципом комплементарності до матриці, з якої ведеться зчитування. Молекула ДНК, що синтезується, є комплементарною до матричного ланцюга й ідентична з одним із ланцюгів другої подвійної спіралі.
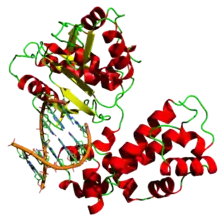
Розрізняють ДНК-залежну ДНК-полімеразу (КФ 2.7.7.7), що використовує як матрицю один з ланцюгів ДНК, і РНК-залежну ДНК-полімеразу (інша назва — зворотна транскриптаза КФ 2.7.7.49), здатну до зчитування інформації з РНК (зворотна транскрипція). ДНК-полімераза є голоферментом, оскільки для нормального функціонування вона потребує присутності іонів магнію як кофактора. При відсутності іонів магнію про неї можна говорити як про апофермент.
Дія ДНК-полімерази
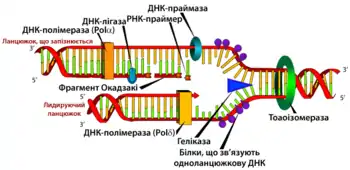
ДНК-полімераза додає вільні нуклеотиди до 3’-кінця ланцюга, що збирається. Це призводить до елонгації ланцюгу в напрямку 5'-3'.
Жодна з відомих ДНК-полімераз не може створити ланцюг «з нуля»: вони в змозі лише додавати нуклеотиди до вже існуючої 3'-гідроксильної групи. З цієї причини ДНК-полімераза потребує праймера, до якого вона могла б додати перший нуклеотид. Праймери складаються з основ РНК і ДНК, при цьому перші дві основи завжди є РНК-основами. Праймери синтезуються іншим ферментом — праймазою. Ще один фермент — геліказа - необхідний для розкручування подвійної спіралі ДНК з формуванням одноланцюжкової структури, яка забезпечує реплікацію обох ланцюжків відповідно до напівконсервативної моделі реплікації ДНК.
Деякі ДНК-полімерази також мають здатність виправляти помилки в тільки що зібраному ланцюжку ДНК. Якщо відбувається виявлення неправильної пари нуклеотидів, ДНК-полімераза відкатується на один крок назад. Завдяки своїй екзонуклеазній активності, ДНК-полімераза може вилучити неправильний нуклеотид з ланцюжка і вставити на його місце правильний, після чого реплікація продовжується в нормальному режимі.
Різноманіття ДНК-полімераз
Структура ДНК-полімераз досить жорстко фіксована. Їхні каталітичні субодиниці дуже мало відрізняються в різних видах живих клітин. Така фіксація структури зазвичай з'являється там, де відсутність різноманітності обумовлена величезною важливістю або навіть незамінністю для функціонування клітини.
Генами деяких вірусів теж кодується особлива ДНК-полімераза, яка може вибірково реплікувати вірусну ДНК. Ретровіруси мають ген незвичайної ДНК-полімерази, що є РНК-залежною ДНК-полімеразою, котра називається зворотною транскриптазою і що здійснює збирання ДНК, на основі шаблонної РНК.
Родини ДНК-полімераз
На основі своєї структури ДНК-полімерази можуть бути розбиті на сім різних родин: A, B, C, D, X, Y, і RT.
Родина A
Родина A містить реплікативні і відновні ДНК-полімерази. Реплікативні члени цього сімейства представлені, наприклад, добре дослідженою ДНК-полімеразою вірусу Т7 або еукаріотичною мітохондріальною ДНК-полімеразою γ. Серед відновних полімераз є такі приклади як полімераза I (Pol I) E. coli , Pol I Thermus aquaticus або Pol IBacillus stearothermophilus . Відновні полімерази беруть участь в процесі усунення помилок в ДНК, що збирається, а також в обробці фрагментів Окадзакі.
Родина B
До родини B в основному входять відновні полімерази, зокрема основні еукаріотичні ДНК-полімерази α, δ, ε, а також ДНК-полімераза ζ. До цієї родини також відносять ДНК-полімерази деяких бактерій і бактеріофагів, наприклад бактеріофагів T4, Phi29 і RB69. Ці ферменти використовуються в синтезі і 3’→5’, і 5’→3’ ланцюгів ДНК. Помітною особливістю полімераз цієї родини є чудова точність реплікації. Багато представників також володіє сильною 3’-5’-екзонуклеазною активністю (за винятком ДНК-полімераз α і ζ, які не мають здатності коректувати помилки).
Родина C
Полімерази цієї родини — в основному бактеріальні хромосомні реплікативні ферменти, що мають, крім того, 3’-5’-екзонуклеазну активність.
Родина D
Полімерази цієї родини недостатньо вивчені. Всі відомі зразки вважаються реплікативними полімеразами і виявлені у архей типу Euryarchaeota.
Родина X
До родини Х відноситься широко відома еукаріотична ДНК-полімераза β (Pol β), а також σ, λ, μ і кінцева дезоксинуклеотидил-трансфераза (TDT). ДНК-полімераза β необхідна для здійснення процесу відновлення пошкоджених ділянок ДНК. Полімерази λ і μ беруть участь у негомологічному з'єднанні кінців — процесі відновлення розривів подвійної спіралі. TDT експрессуєтся тільки в лімфоїдній тканині і додає «N нуклеотідов» до розривів подвійної спіралі, що утворюються під час В(Р)С-рекомбінації. Дріжджі Saccharomyces cerevisiae мають лише одну полімеразу X, Pol 4, що бере участь у негомологічному з'єднанні.
Родина Y
Полімерази цієї родини відрізняються від інших низькою продуктивністю на цілісних шаблонах, а також здатністю здійснювати реплікацію на шаблонах пошкодженої ДНК. Внаслідок цього члени сімейства називаються полімеразами транслезійного синтезу (ТЛС-полімеразами). Залежно від характеру пошкодження (лезії) ТЛС-полімерази можуть відновити початковий ланцюжок. Помилка може і не бути відновлена, що приводить до мутацій. Наприклад, пацієнти, які страждають від пігментної скенодерми, мають у своєму геномі мутантну ДНК-полімеразу η (ета), що може без помилок відновлювати пошкодження, викликані ультрафіолетом, проте інші полімерази, наприклад ζ (що відноситься до родини B), приводять до помилок, що, як вважається, приводить до схильності до онкологічних захворювань.
Інші члени цієї родини — людські полімерази ι, κ, а також кінцева дезоксинуклеотидил-трансфераза Rev1. У E. coli є дві ТЛС-полімерази: IV (DINB) і V (UMUC).
Родина RT
Родина зворотніх транскриптаз (назва сімейства походить від англ. reverse transcriptase) містить полімерази, виявлені як у ретровірусів, так і у еукаріотів. Еукаріотичні полімерази в основному представлені теломеразами. Ці полімерази використовують РНК як матрицю для синтезу ланцюжка ДНК.
Прокаріотичні ДНК-полімерази
У бактерій виявлено п'ять ДНК-полімераз:
- ДНК-полімераза I — задіяна у відновленні ДНК, має як 5'-3', так і 3'-5'-екзонуклеазну активність;
- ДНК-полімераза II — бере участь в реплікації пошкодженої ДНК. Має здатність 5'-3'-елонгації і 3'-5'-екзонуклеазну активність;
- ДНК-полімераза III — основна полімераза бактерій, що має також 3'-5'-екзонуклеазну активність;
- ДНК-полімераза IV — ДНК-полімераза сімейства Y;
- ДНК-полімераза V — ДНК-полімераза сімейства Y, що бере участь в пропуску пошкоджених ділянок ДНК.
Еукаріотичні ДНК-полімерази
Еукаріоти містять щонайменше п'ятнадцять видів ДНК-полімераз[1]:
- ДНК-полімераза α формує комплекс з праймазою, яка синтезуює праймер ДНК, після чого полімераза приєднує до цього праймеру нуклеотиди. Після того, як довжина ланцюжка досягне близько 20 нуклеотидів[2], до транскрипції приступають полімерази δ і ε;
- ДНК-полімераза β задіяна у відновленні ДНК;
- ДНК-полімераза γ, що здійснює реплікацію мітохондріальної ДНК;
- ДНК-полімераза δ — основна полімераза еукаріотів. Вона високопродуктивна, а також має 3'-5'-екзонуклеазну активність;
- ДНК-полимераза ε, що іноді заміщає ДНК-полімеразу δ під час синтезу 3’-5’-ланцюжка. Основне призначення цієї полімерази неясне;
- ДНК-полімерази η, ι, κ і Rev1 з сімейства Y, а також ζ з сімейства B. Ці полімерази задіяні в пропуску пошкоджених ділянок ДНК[3].
- Існують також інші еукаріотичні ДНК-полімерази, які поки що недостатньо вивчені: θ, λ, φ, σ і μ, та деякі інші.
Жодна еукаріотична полімераза не може відщеплювати праймери, тобто не має 5-3'-екзонуклеазної активності. Цю функцію виконують інші ферменти. Тільки полімерази, що здійснюють елонгацію (γ, δ і ε) мають 3'-5'-екзонукеазну активність.
Див. також
Примітки
- I. Hubscher, U.; Maga, G.; Spadari, S. (2002) Eukaryotic DNA polymerases. Annual Review of Biochemistry 71, 133-63.
- J. M. Berg; J. L. Tymoczko; L. Stryer «Biochemie», Springer, Heidelberg/Berlin 2003
- I. Prakash, S.; Johnson, R. E.; Prakash, L. (2005) Eukaryotic translesion synthesis DNA polymerases: specificity of structure and function. Annual Review of Biochemistry 74, 317-53.
Посилання
- PubMed
- Burgers P, Koonin E, Bruford E et al. (2001). Eukaryotic DNA polymerases: proposal for a revised nomenclature. J. Biol. Chem. 276 (47): 43487–90. PMID 11579108.
- DNA Polymerases: Custom Search Engine[недоступне посилання з квітня 2019] at custom-search-engine.com
- Annual Review of Biochemistry: EUKARYOTIC DNA POLYMERASES at annualreviews.org
- Unusual repair mechanism in DNA polymerase lambda, Ohio State University, July 25, 2006.
