Оксид бору
Окси́д бо́ру, бо́рний ангідри́д — неорганічна бінарна сполука Бору та Оксигену складу B2O3. Являє собою білу кристалічну або аморфну речовину. Стійкий до розкладання.
| Оксид бору | |
|---|---|
 | |
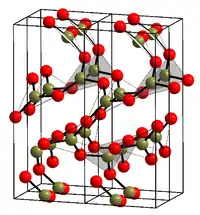 | |
| Назва за IUPAC | Бор оксид |
| Інші назви | триоксид бору, борний ангідрид |
| Ідентифікатори | |
| Номер CAS | 1303-86-2 |
| Номер EINECS | 215-125-8 |
| ChEBI | 30163 |
| RTECS | ED7900000 |
| SMILES |
B(=O)OB=O[1] |
| InChI |
InChI=1S/B2O3/c3-1-5-2-4 |
| Номер Гмеліна | 11108 |
| Властивості | |
| Молекулярна формула | B2O3 |
| Молярна маса | 69,620 г/моль |
| Зовнішній вигляд | безбарвні кристали або аморфний |
| Густина | 2,55 г/см³[2] |
| Тпл | 450 °C[2] |
| Розчинність (вода) | 2,2 г/100 г H2O (20 °C)[2] |
| Розчинність (етанол) | розчинний |
| Показник заломлення (nD) | 2,8017 (крист.) |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
В природі зустрічається у складі бури Na2B4O7·10H2O, борациту 2Mg3B8O15·MgCl2, гідроборациту, пандерміту, колеманіту.
Окрім сполуки B2O3 відомі також інші оксиди: монооксид B2O, субоксид B6O.
Поширення у природі
Оксид бору широко розповсюджений у природі у складі інших сполук. Він входить до складу борної кислоти H3BO3, яка міститься у водах термальних джерел у вулканічних місцевостях (мінерал сасолін, що містить борну кислоту, отримав назву від італійського курортного містечка Сасо Пізано, яке славиться своїми лікувальними джерелами).
Окрім того, оксид бору зустрічається і у вигляді боратів. Основними джерелами оксиду бору є мінерали бура Na2B4O7·10H2O, борацит 2Mg3B8O15·MgCl2, гідроборацит, пандерміт, колеманіт та ін.
Фізичні властивості
Оксид бору може перебувати у кристалічному та аморфному станах. Кристалічний B2O3 є хімічно неактивним, на відміну від аморфного. Сполука є стійкою до нагрівання, не відновлюється навіть при дії на неї коксу. Забарвлює полум'я пальника у зелений колір.
Отримання
Синтезувати оксид бору можна, наприклад, спалюючи на повітрі чистий бор або бороводні:
Оксид також утворюється в результаті розкладання деяких сполук бору:
Хімічні властивості
Кристалічний оксид бору є хімічно неактивним. Аморфний оксид бору реагує з водою з виділенням великої кількості тепла (тепла, що виділяється від додавання 100 г оксиду до 125 г води, достатньо, аби довести воду до кипіння).
Сполука реагує з лугами та концентрованою плавиковою кислотою:
Під дією металів бор відновлюється з оксиду:
Останній метод використовується для отримання бороводнів.
Див. також
Примітки
- Boric oxide
- За тиску 101,3 кПа
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Реми Г. Курс неорганической химии / А. В. Новоселова. — М. : ИИЛ, 1963. — Т. 1. — 922 с. (рос.)
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ / Р. А. Лидин. — 3-е. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0. (рос.)
- Глосарій термінів з хімії // Й. Опейда, О. Швайка. Ін-т фізико-органічної хімії та вуглехімії ім. Л.М.Литвиненка НАН України, Донецький національний університет — Донецьк: «Вебер», 2008. — 758 с. — ISBN 978-966-335-206-0.
