Фенілаланін
Фенілалані́н — амінокислота, одна з двадцяти стандартних амінокислот, що входять до складу білків. Ліпофільна (аполярна) амінокислота. Поглинає ультрафіолет (254 нм) і має слабку флуоресценцію.
| Фенілаланін | |
|---|---|
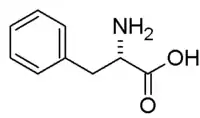 | |
| Назва за IUPAC | 2-Аміно-3-феніл-пропанова кислота |
| Ідентифікатори | |
| Абревіатури | Phe, F |
| Номер CAS | 63-91-2 |
| PubChem | 994 |
| Номер EINECS |
211-603-5 (D) 200-568-1 (L) 205-756-7 (DL) |
| DrugBank | 00120 |
| KEGG | D00021 і C00079 |
| Назва MeSH | D12.125.072.050.685 і D12.125.142.666 |
| ChEBI | 17295 |
| SMILES |
C1=CC=C(C=C1)CC(C(=O)O)N |
| InChI |
InChI=1S/C9H11NO2/c10-8(9(11)12)6-7-4-2-1-3-5-7/h1-5,8H,6,10H2,(H,11,12)/t8-/m0/s1 |
| Номер Бельштейна | 1910408 |
| Номер Гмеліна | 50837 |
| Властивості | |
| Молекулярна формула | C9H11NO2 |
| Молярна маса | 165,19 г/моль |
| Густина | 1,29 г/см3 |
| Тпл | 283 °C |
| Розчинність (вода) | 27 г/л |
| Кислотність (pKa) | 2,20; 9,09 |
| Ізоелектрична точка | 5,5 |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Біологічна роль
L-фенілаланін — це одна з основних 20 амінокислот, що бере участь у біохімічних процесах формування протеїнів та кодується певним геном ДНК. Кодони L-фенілаланіну UUU та UUC. Фенілаланін є попередником тирозину[1], сигнального монаміну допаміну, адреналіну та норадреналіну, а також пігменту шкіри меланіну.
Захворювання
Нездатність організмом метаболізувати фенілаланін викликає хворобу - фенілкетонурію, стан при якій підтримується дієтою та сучасними препаратами (наприклад, Пегваліаза, Сапроптерин).
Примітки
- Christianson, D. W.; Mangani, S.; Shoham, G.; Lipscomb, W. N. (1989). Binding of D-Phenylalanine and D-Tyrosine to Carboxypeptidase A (pdf). Journal of Biological Chemistry 264 (22): 12849–12853. PMID 2568989.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
