Хром(IV) оксид
Хром(IV) окси́д, окси́д хро́му(IV) — неорганічна сполука, оксид складу CrO2. За кімнатної температури має вигляд чорних, голкоподібних кристалів, які проявляють феромагнітні властивості.
| Хром(IV) оксид | |
|---|---|
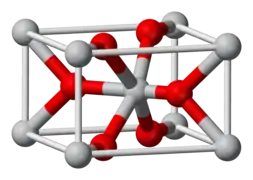 Кристалічна структура типу «рутил» | |
| Інші назви | діоксид хрому |
| Ідентифікатори | |
| Номер CAS | 12018-01-8 |
| Номер EINECS | 234-630-4 |
| ChEBI | 48263 |
| RTECS | GB6400000 |
| SMILES |
[O-2].[O-2].[Cr+4][1] |
| InChI |
InChI=1S/Cr.2O/q+4;2*-2 |
| Номер Гмеліна | 18391 |
| Властивості | |
| Молекулярна формула | CrO2 |
| Молярна маса | 83,995 г/моль |
| Зовнішній вигляд | чорні кристали |
| Густина | 4,89 г/см³[2] |
| Тпл | прибл. 400 °C (розкл.)[2] |
| Розчинність (вода) | нерозчинний |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
-598,0 кДж/моль |
| Пов'язані речовини | |
| Інші катіони | хром(III) оксид, хром(VI) оксид |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Широко застосовується у виробництві магнітних носіїв інформації.
Фізичні властивості
Оксид хрому кристалізується у вигляді чорних, голкоподібних тетрагональних кристалів, із кристалічною структурою рутилу. За кімнатної температури CrO2 проявляє феромагнітні властивості. Температура Кюрі для нього складає 116 °K і може бути підвищена до 155 °K за допомогою добавок заліза.
Оксид є сполукою змінного складу: його склад нестехіометричний і корелюється від CrO1,89 до CrO2,02.
Отримання
Вперше оксид хрому(VI) було синтезовано у 1859 році Фрідріхом Велером при розкладанні хроміл хлориду:
Синтез оксиду хрому можна провести також розкладанням хромового ангідриду CrO3, хром(III) хромату CrIII2(CrO4)3 (або Cr5O12), окисненням оксиду Cr(III). Нині у промислових масштабах застосовується метод, запатентований компанією «DuPont», — отримання оксиду(IV) із суміші CrO3 та Cr2O3[3]:
Хімічні властивості
За кімнатої температури оксид хрому є стабільним; розкладається при температурі понад 350 °C, утворюючи хром(III) оксид:
Кристали CrO2 нерозчинні у воді, але на їхній поверхні може протікати реакція диспропорціонування:
При сплавленні із лугами утворює хромати:
Застосування

Основною сферою застосування оксиду хрому(IV) є виробництво магнітних носіїв інформації (зокрема, магнітних стрічок). Завдяки низькій магнетострикції CrO2, дані з таких носіїв відтворюються практично без втрат.
Див. також
Примітки
- UNII-7BHJ7466GL
- За тиску 101,3 кПа
- Пат. 3,451,771 США, МПК C01G 37/02, H01F 1/34. Preparation of ferromagnetic CrO2 by heating CrO3 in the presence of O2 and Cr2O3 / Norman L. Cox, Claymont, and William T. Hicks, Wilmington, Del., assignors to E. I. du Pont de Nemours and Company, Wilmington, Del., a corporation of Delaware (США) – № 589,862 ; заявл. 27.10.66 ; опубл. 24.06.69 — 3 с.
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Chromium compounds // Kirk-Othmer Encyclopedia of Chemical Technology. — 4th. — New York : John Wiley & Sons, 2004. — Vol. 6. — P. 134. — ISBN 978-0-471-48517-9. (англ.)
- Рипан Р., Четяну И. Неорганическая химия: Химия металлов / В. И. Спицын. — М. : «Мир», 1972. — Т. 2. — 871 с. (рос.)