Азиди
Ази́ди — хімічні сполуки, що мають групу N3. До цього ряду належать солі азидної (азотистоводневої) кислоти HN3, похідні карбонових кислот (азоіміди RCON3), а також продукти заміщення гідрогену в HN3 на галоген (наприклад, азид йоду IN3). Азиди є псевдогалогенідами.
Будова

Внаслідок перегрупування групі N3- притаманна лінійна геометрія:
- R-N=N+=N- ↔ R-N--N+≡N
Гібридизація атомних орбіталей N в α-положенні — sp2, в β-положенні — sp, в γ-положенні — spn (1 < n < 2).
Властивості
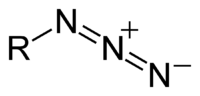
Азиди мають осно́вні властивості (головним чином за рахунок α-атома N).
Органічні азиди утворюються при взаємодії нітритної кислоти з гідразидами кислот. При нагріванні з лугами дають первинні аміни. Відновлюються до амінів, триазенів, легко відщеплюють азот. Ацилазиди перегруповуються в нейтральних або кислих середовищах (звичайно при нагріванні) до ізоціанатів (естерів ціанової кислоти):
- RCO-N3 → R-N=C=O + N2
Азиди лужних і лужноземельних металів при нагріванні дають чисті азот і метал. Азиди важких металів — сильні вибухові речовини. Наприклад, азид свинцю Pb(N3)2 вибухає від удару і використовується як детонатор у капсулях-детонаторах. Інший приклад — азид натрію NaN3.
Джерела
- Глосарій термінів з хімії / уклад. Й. Опейда, О. Швайка ; Ін-т фізико-органічної хімії та вуглехімії ім. Л. М. Литвиненка НАН України, Донецький національний університет. — Дон. : Вебер, 2008. — 738 с. — ISBN 978-966-335-206-0.
- Українська радянська енциклопедія : у 12 т. / гол. ред. М. П. Бажан ; редкол.: О. К. Антонов та ін. — 2-ге вид. — К. : Головна редакція УРЕ, 1974–1985.
Посилання
- Азиди // Велика українська енциклопедія : у 30 т. / проф. А. М. Киридон (відп. ред.) та ін. — 2016. — Т. 1 : А — Акц. — 592 с. — ISBN 978-617-7238-39-2.