Колігативні властивості
Колігативні властивості (від лат. colligo — зв'язувати, з'єднувати) — властивості розчинів, які залежать від кількості частинок розчинених речовин і не залежать від їх природи. Основою впливу розчинених речовин на властивості розчину є те, що вони знижують хімічний потенціал (μ) розчинника. До колігативних властивостей належать: зменшення тиску насиченої пари і температури плавлення, підвищення температури кипіння і поява осмотичного тиску[1][2][3].
Зниження тиску насиченої пари
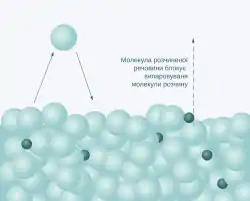
Зниження тиску насиченої пари розчину описується законом Рауля, який для ідеального бінарного (такого, що складається із двох компонентів — розчинника і однієї розчиненої речовини) розчину формулюється так: відносне зниження тиску насиченої пари розчинника над розчином рівне мольній частці розчиненої речовини:
- ,
де P0A — тиск пари над чистим розчинником, PA — тиск пари над розчином, XB — мольна частка розчиненої речовини[4].
З молекулярної точки зниження тиску насиченої пари розчинника над розчином із збільшенням концентрації розчиненої речовини можна пояснити тим, що наявність молекул розчиненої речовини на поверхні розчину перешкоджає виходу молекул розчинника у пару але не перешкоджає їх поверненню[5].
Зниження температури замерзання і підвищення температури кипіння
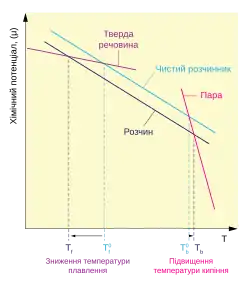
Щоб кількісно оцінити збільшення температури кипіння і зменшення температури плавлення розчину, слід знайти температуру при якій, за сталого тиску (1 атм.), пара чистого розчинника або чистий розчинник у твердій формі відповідно має такий же хімічний потенціал, як і розчинник у розчині (див. схему праворуч). Знайдені температури і будуть новими температурами фазового переходу[6].
Кількісно зміну температур плавлення і кипіння можна розрахувати за формулами:
- ,
де ΔTf — зміна температури плавлення, ΔTb — зміна температури кипіння, m — моляльна концентрація розчиненої речовини, K — кріоскопічна стала, E — ебуліоскопічна стала. Кріоскопічна та ебуліоскопічна сталі залежать тільки від природи розчинника[7]. Їх значення для деяких речовин наведене у таблиці:
| Розчинник | Кріоскопічна стала (K) | Ебуліоскопічна стала (E) |
|---|---|---|
| Бензен[8] | 5,12 | 2,53 |
| Камфора[8] | 40 | |
| Фенол[8] | 7,27 | 3,04 |
| Вода[8] | 1,86 | 0,51 |
| Хлороформ[9] | 4,70 | 3,63 |
Зниження температури плавлення розчину у порівнянні із чистим розчинником лежить в основі методу визначення молекулярної маси розчиненої речовини, що називається кріоскопією. Проте цей метод поступився більш точним і перестав використовуватись[8].
Осмос
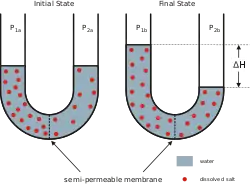
Осмос (від дав.-гр. ὠσμός — штовхати) — це спонтанний перехід чистого розчинника у розчин, відділений від нього напівпроникною мембраною, тобто проникною для розчинника і не проникною для розчиненої речовини. Осмотичний тиск (Π) — це тиск, який необхідно прикласти до розчину, щоб зупинити надходження розчинника. Причиною виникнення осмосу, як і інших колігативних властивостей, є зменшення хімічного потенціалу розчинника внаслідок наявності в ньому молекул розчиненої речовини[10].
Значення осмотичного тиску для сильно розведених розчинів можна приблизно обчислити, використовуючи рівняння, виведене Вант-Гоффом:
- ,
де R — універсальна газова стала, Т — абсолютна температура, ic — осмолярність розчину, тобто добуток фактора Вант-Гоффа (i), який визначається мірою дисоціації розчиненої речовини на окремі компоненти, і молярної концентрації розчиненої речовини (c). Для хлориду натрію, наприклад, i=2, оскільки ця сіль повністю дисоціює на Na+ і Cl-. Для розчину із кількома (n) розчиненими речовинами, загальний осмотичний тиск є сумою[11]:
Важливими прикладами осмосу є транспорт рідин через клітинні мембрани, діаліз та осмометрія — визначення молекулярних мас речовин шляхом вимірювання осмотичного тиску їх розчину. Цей метод широко використовується для з'ясування молекулярних мас макромолекул[10].
Примітки
- Nelson et al, 2008, с. 51.
- Atkins et al, 2006, с. 150.
- Третьяков, 2004, с. 81—85.
- Третьяков, 2004, с. 81—82.
- Atkins et al, 2006, с. 144.
- Atkins et al, 2006, с. 151.
- Третьяков, 2004, с. 82—83.
- Atkins et al, 2006, с. 153.
- Третьяков, 2004, с. 83.
- Atkins et al, 2006, с. 154.
- Nelson et al, 2008, с. 52.
Джерела
- Atkins P., de Paula J. (2006). Physical Chemistry (вид. 8th). W. H. Freeman and Company. ISBN 0-7167-8759-8.
- Nelson D.L., Cox M.M. (2008). Lehninger Principles of Biochemistry (вид. 5th). W. H. Freeman. ISBN 978-0-7167-7108-1.
- Тамм М. Е., Третьяков Ю. Д. Неорганическая химия. — Москва : ИЦ «Академия», 2004. — Т. 1. — 240 с. — ISBN 5-7695-1446-1.
