Полівалентні йодоорганічні сполуки
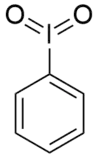
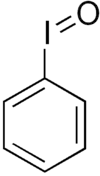
По́лівале́нтні йодоргані́чні сполу́ки — великий клас сполук, органічних похідних йоду у ступенях окиснення (III), (V) та (VII). Одним з найпростіших представників λ3-йоданів є йодозилбензен. Одним з найпростішіх представників λ5-йоданів є йодилбензен.
Номенклатура
Більшість полівалентних іодоорганічних сполук є гіпервалентними сполуками (сполуками з розширеним октетом). Найбільш адекватно класифікувати гіпервалентні йодоорганічні сполуки можна за допомогою N-X-L позначення Мартіна-Ардуенґо, в якому N позначує формальну кількість валентних електронів навколо центрального атому, X позначує кількість неподілених електронних пар та сігма-зв'язків та L позначує кількість лігандів.[1] Cтосовно солей йодонію, що формально не є гіпервалентними сполуками, це позначення не вживається.
Більшість полівалентних іодоорганічних сполук зі ступенями окиснення (III) та (V), зокрема солі йодонію, мають за рекомендацією IUPAC також назви λ3-йоданів та λ5-йоданів відповідно. [2][3][4] Згідно з цією номенклатурою цифри 3 та 5 позначають кількість валентних зв'язків - ковалентних, або йонних - навколо центрального атому.
У минулому вживалися назва "йодинани" для сполук з ступенем окиснення (ІІІ) та "перйодинани" для сполук з ступенем окиснення (V).
Важливо зазначити, що стосовно деяких поширених класів полівалентних органічних сполук, ламбда-номенклатура не вживається. Зокрема стосовно сполук що містять групи -I(OH)2, -I=O, -I=O2, або їхні похідні. Додатково деякі полівалентні йодоорганінічні сполуки мають широковживані тривіальні назви. Наприклад, широковживаною назвою йодозилбензена є йодозобензен.
Історія
Цей клас налічує величезну кількість різноманітних сполук. Вперше органічні речовини, що містять йод зі ступенем окиснення (ІІІ)та (V) описані у 1885 році Вілгеродтом, що зробив перший огляд цієї галузі хімії в 1914 році. Протягом наступних ста років було видано 4 книги, 12 всеобічних оглядів галузі та нечисленну кількість оглядів, присвячених специфічним питанням, пов'язаним з цими речовинами.
Загальні властивості
Станом на 2008 рік стверджується, що достатню стабільність мають полівалентні йодорганічні сполуки з ароматичними замісниками, за винятком невеликої кількості сполук з алкильними замісниками, що стабілізовані eлектронегативними атомами, наприклад з перфтороалкилами. Всі поливалентні іодоорганічні сполуки можна поділити на λ3-йодани та λ5-йодани. λ3-йодани мають загальну будову у вигляді деформованої трикутної піраміди з двома гетероатомами в апікальних вершинах, та двома електронними парами і органічним замісником в екваторіальній площі. Йодонієві солі, з двома органічними замісниками та одним гетероатомом, теж мають будову деформованої біпіраміди та відносяться до λ3-йоданів. λ5-йодани мають форму деформованого октаедра з неподіленою електронною парою в одній апікальній вершині, органічний замісник в другій апікальній вершині, та чотири гетероатоми в екваторіальній площині.
Важливі представники
Перйодат Деса-Мартіна, Реагент Козера
Примітки
- J.C. Martin Science, 1983, 221 (4610), pp 509-514 DOI:10.1126/science.221.4610.509
- David F. Banks Chem. Rev., 1966, 66 (3), pp 243–266 DOI:10.1021/cr60241a001
- Viktor V. Zhdankin and Peter J. Stang Chem. Rev., 2008, 108 (12), pp 5299–5358 DOI:10.1021/cr60241a001
- Viktor V. Zhdankin "Hypervalent Iodine Chemistry: Preparation, Structure and Synthetic Applications of Polyvalent Iodine Compounds" DOI:10.1002/9781118341155
