Пірофосфатна кислота
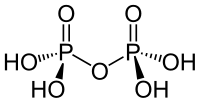
Пі́рофосфа́тна кислота́, дифосфа́тна кислота́ — неорганічна сполука, чотириосновна кислота складу H4P2O7. За звичайних умов є білою кристалічною речовиною у двох формах: стійкій з температурою плавлення 71,5 °C та нестійкій із 54,3 °C. Дуже добре розчиняється у воді.
| Пірофосфатна кислота | |
|---|---|
 | |
| Інші назви | дифосфатна кислота |
| Ідентифікатори | |
| Номер CAS | 2466-09-3 |
| Номер EINECS | 219-574-0 |
| DrugBank | 04160 |
| KEGG | C00013 |
| ChEBI | 29888 |
| SMILES |
OP(=O)(O)OP(=O)(O)O[1] |
| InChI |
InChI=1S/H4O7P2/c1-8(2,3)7-9(4,5)6/h(H2,1,2,3)(H2,4,5,6) |
| Номер Бельштейна | 3942075 |
| Номер Гмеліна | 82619 |
| Властивості | |
| Молекулярна формула | H4P2O7 |
| Молярна маса | 177,975 г/моль |
| Зовнішній вигляд | білі кристали |
| Тпл | 71,5 °C (стійка форма) 54,3 °C (нестійка форма) |
| Розчинність (вода) | 709 г/100 г H2O[2] |
| Кислотність (pKa) | 0,91 (pK1) 2,10 (pK2) 6,70 (pK3) 9,32 (pK4) |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
При взаємодії з основами утворює ряд солей пірофосфатів.
Отримання
Пірофосфатна кислота утворюється при нагріванні ортофосфатної кислоти, внаслідок міжмолекулярної дегідратації:
Іншим способом є насичення ортофосфатної кислоти оксидом фосфору(V). Дана реакція застосовується у виробництві H3PO4 для її концентрування:
Хімічні властивості
Пірофосфатна кислота є чотириосновною кислотою. При дисоціації за першим ступенем, вона навіть є сильнішою за ортофосфатну кислоту:
- (pK1 = 0,91)
- (pK2 = 2,10)
- (pK3 = 6,70)
- (pK3 = 9,32)
При взаємодії з насиченими розчинами лугів реакція нейтралізації проходить повністю, а з розведеними — переважно за двома ступенями:
При кип'ятінні у розведених розчинах відбувається зворотнє концентрування — пірофосфатна кислота розкладається з утворенням ортофосфатної:
Взаємодіє із деякими солями, якщо реакція веде до утворення малорозчинних пірофосфатів:
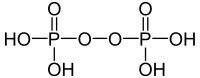
Із концентрованим розчину пероксидом водню H4P2O7 окиснюється до пероксодифосфатної кислоти H4P2O8, яка є нестійкою сполукою і при розведенні зворотньо розкладається на фосфатну та пероксофосфатну кислоти:
Примітки
- Diphosphoric acid
- При температурі 23 °C.
Джерела
- Greenwood N. N., Earnshaw A. Chemistry of the Elements. — 2nd. — Oxford : Butterworth-Heinemann, 1997. — P. 516-523. — ISBN 0-7506-3365-4. (англ.)
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ / Р. А. Лидин. — 3-е. — М. : «Химия», 2000. — 480 с. — ISBN 5-7245-1163-0. (рос.)
- Химический энциклопедический словарь / И. Л. Кнунянц. — М. : Сов. энциклопедия, 1983. — 792 с. (рос.)