П-нітроанілін
Пара-нітроанілін — хімічна сполука з класу ароматичних амінів і нітросполук. Формула . Жовта тверда речовина.
| Структурна формула | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
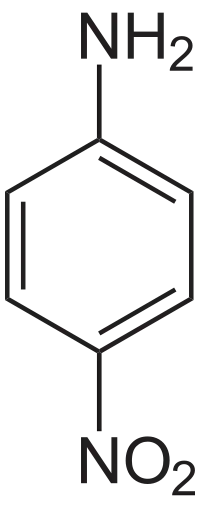 | ||||||||||||||||
| Загальна інформація | ||||||||||||||||
| Преференційна назва ІЮПАК | ||||||||||||||||
| Систематична назва ІЮПАК | 4-Нітроанілін | |||||||||||||||
| Інші назви |
П-нітроанілін, пара-нітроанілін, 4-нітробензенамін | |||||||||||||||
| Хімічна формула | C6H6N2O2 | |||||||||||||||
| 3D Структура (JSmol) | Інтерактивне зображення | |||||||||||||||
| Зовнішні ідентифікатори / Бази даних | ||||||||||||||||
| ||||||||||||||||
| Властивості | ||||||||||||||||
| Молярна маса | 138,13 г/моль | |||||||||||||||
| Агрегатний стан |
Твердий | |||||||||||||||
| Зовнішній вигляд |
Тверда жовта речовина | |||||||||||||||
| Густина |
1,44 г/см3 (20 °C) | |||||||||||||||
| Температура плавлення |
147 °C | |||||||||||||||
| Температура кипіння |
336 °C | |||||||||||||||
| Розчинність |
0,5 г/л (вода, 20 °C) | |||||||||||||||
| Безпека | ||||||||||||||||
| Маркування згідно системі УГС
Небезпека | ||||||||||||||||
| H-фрази | H: H301, H311, H331, H373, H412 | |||||||||||||||
| P-фрази | P: P273, P280, P304+P340, P302+P352, P308+P310 | |||||||||||||||
| LD50 |
750 мг/кг (щур, орально) | |||||||||||||||
| Наскільки це можливо, значення величин подані в одиницях системи SI. Якщо не вказано іншого, усі дані відносяться до стандартного стану. | ||||||||||||||||

Отримання
Отримують амінуванням п-хлоронітробензену. Температура реакції — 195 °C, тиск — 4,5 МПа.[1]
Також отримують нітруванням аніліну з попереднім захистом аміногрупи від окисненея: анілін → ацетанілід → пара-нітроацетанілід → пара-нітроанілін:
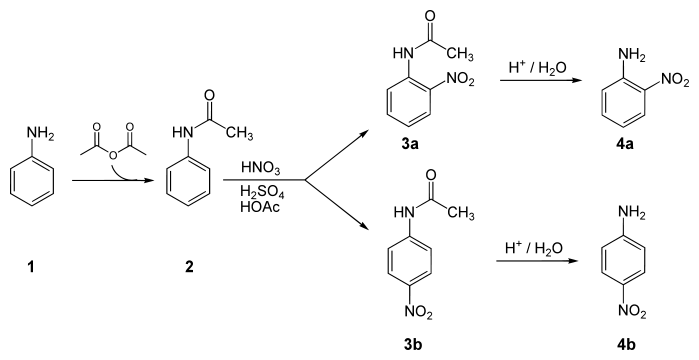
Хімічні властивості
При температурі 170° — 210°C взаємодіє з концентрованою сульфатною кислотою. При цьому суміш значно збільшується в об`ємі і утворюється твердий продукт, який не горить і майже не окиснюється.[2]
Як і інші первинні ароматичні аміни, 4-нітроанілін може діазотуватися. Діазотований пара-нітроанілін при реакції з 2-нафтолом утворює азобарвник Пара червоний:[3]
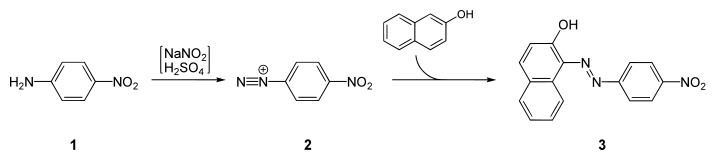

Посилання
Примітки
- Booth, Gerald (15 червня 2000). У Wiley-VCH Verlag GmbH & Co. KGaA. Nitro Compounds, Aromatic. Ullmann's Encyclopedia of Industrial Chemistry (англ.). Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. с. a17_411. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a17_411.
- Poshkus, A. C.; Parker, J. A. (1970-08). Studies on nitroaniline–sulfuric acid compositions: Aphrogenic pyrostats. Journal of Applied Polymer Science 14 (8). с. 2049–2064. doi:10.1002/app.1970.070140813. Процитовано 31 січня 2021.
- Al-Rubaie, L. Abd-Alredha R.; Mhessn, R. Jameel (2012). Synthesis and Characterization of Azo Dye Para Red and New Derivatives. E-Journal of Chemistry (англ.) 9 (1). с. 465–470. ISSN 0973-4945. doi:10.1155/2012/206076. Процитовано 31 січня 2021.

