Ціаніди
Ціані́ди (ціанисті метали) — солі синильної кислоти. У практичному відношенні особливо важливі ціаніди лужних металів — калію, натрію, що одержуються різними способами, наприклад прожарюванням суміші коксу і поташу в атмосфері азоту. Найбільше значення має ціанід калію (ціанистий калій).
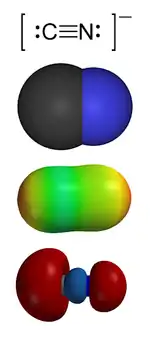
Зверху вниз:
1. Структура валентних зв'язків
2. Об'ємна модель
3. Поверхня електростатичного потенціалу
4. 'Carbon lone pair' HOMO
Як солі дуже слабкої кислоти, ціаніди у воді в сильному ступені зазнають гідролізу:
Тому розчини мають лужну реакцію і сильно пахнуть синильною кислотою.
Отримання
Отримують ціаніди, в результаті взаємодії основ, металів, та інших солей з синильною кислотою:
Ціаніди калію і натрію володіють здатністю розчиняти у присутності кисню повітря срібло і золото. На цьому засновано їх застосування для вилучення вказаних металів з руд, крім того, вони використовуються в органічному синтезі, при гальванічному золоченні і срібленні, у фотографії тощо.
Джерела
- В. І. Саранчук, М. О. Ільяшов, В. В. Ошовський, В. С. Білецький. Хімія і фізика горючих копалин. — Донецьк: Східний видавничий дім, 2008. — с. 600. ISBN 978-966-317-024-4
