NOx
NOx (укр. ен-о-ікс, англ. nox) — загальне позначення для оксидів азоту NO та NO2 в контексті їхньої ролі як забруднювачів атмосфери.
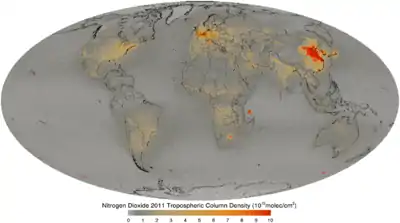
Основним компонентом NOx є оксид NO, який згодом окиснюється до NO2. У великих концентрація суміш газів має жовтувато-коричневий колір (це добре спостерігається у містах, що потерпають від смогу), оскільки поглинає видиме випромінювання в діапазоні поблизу 400 нм.
Фотохімічні перетворення оксидів NOx в атмосфері призводять до появи фотохімічного смогу.
Утворення
Оксиди NOx утворюються за трьома основними шляхами при високотемпературному спалювання палива на повітрі.
Термальний механізм
NO є продуктом спалювання атмосферного азоту у полум'ї при високих температурах (термальний NO):
Сумарна взаємодія:
Що вищою є температура полум'я, то більше оксиду утворюється.
Швидкий механізм
Згідно «швидкого» механізму утворення, паливо внаслідок піролізу утворює вуглеводневі радикали (наприклад, CH), котрі взаємодіють із азотом і окиснюються у полум'ї до NOx та інших часток:
Частина утвореного «швидкого» NO згодом окиснюється до NO2 під дією пероксидного радикалу:
Аналогічно можуть протікати і реакції руйнування NO2:
Також відомі наукові роботи, в яких описується інакший механізм взаємодії вуглеводневого радикалу з азотом:[1]
Паливний механізм
Деяка частина NO утворюється при окисненні нітрогеновмісних компонентів палива (так званий паливний NO). У природному газі та багатьох промислових паливах вміст нітрогену малий, тому і викиди NOx у них не є значними. А от більш поширені рідкі вуглеводневі палива містять близько 0,01—0,5% нітрогену і при спалюванні можуть вносити від 20 до 80% від загальних обсягів NOx після згоряння.
Реакції в атмосфері
При надходженні до атмосфери, NO градієнтно окиснюється до NO2 (від кількох хвилин до годин, в залежності від концентрації присутніх забруднювачів). Окиснення відбувається при взаємодії з озоном або пероксидним радикалом, а також пряма повільна реакція з киснем:
Проте NO2 є нестійким до ультрафіолетового випромінювання (A-типу) — під його дією відбувається зворотня реакція розкладання:
Саме через це концентрація NO2 сягає свого максимуму вранці і поступово зменшується протягом сонячного дня.
Оксиди NOx беруть участь в утворенні компонентів фотохімічного смогу — озону та нітратної кислоти:
- суміш оксиду NO і летких органічних сполук (ЛОС) фотохімічно окиснюється киснем до суміші O3, HNO3 та інших органічних речовин;
- атомарний оксиген, отриманий розкладанням NO2 під дією світла, сполучається з киснем:
- нітратна кислота утворюється внаслідок взаємодії оксиду NO2 із гідроксидним радикалом або вологою:
Зменшення викидів
| Сфера | Обсяг викидів, кт | Внесок, % |
|---|---|---|
| Сільське господарство | 184 871 | 1,80 |
| Комерція і побут | 1 309 461 | 12,80 |
| Виробництво і передача енергії | 2 298 969 | 22,50 |
| Використання енергії у промисловості | 1 289 151 | 12,60 |
| Промислові процеси | 242 783 | 2,40 |
| Дорожній транспорт | 4 142 743 | 40,50 |
| Інший транспорт | 751 399 | 7,30 |
| Відходи | 12 404 | 0,10 |
У процесах, де проводиться спалювання різних видів палива, чи на азотних виробництвах застосовують очисні системи, котрі дозволяють знизити обсяги викидів NOx.
Селективне каталітичне відновлення
Селективне каталітичне відновлення (англ. selective catalytic reduction, SCR) засноване на реакції відновлення оксидів NOx амоніаком до азоту і води:
Реакції проходять на поверхні каталізатору за температури вище 232 °C і в надлишку кисню. До найбільш поширених каталізаторів відносяться оксид V2O5, нанесений на поверхню TiO2 (ефективна температура 300—450 °C), молекулярні цеоліти (300—600 °C), а також дорогоцінні метали (200—300 °C), які однак застосовуються досить рідко через велику ймовірність їхнього отруєння.
Неселективне каталітичне відновлення
Неселективне каталітичне відновлення (англ. non-selective catalytic reduction, NSCR) проводиться за участі водню, вуглеводнів, монооксиду вуглецю в умовах недостатньої кількості кисню. У присутності каталізатора оксиди NOx відновлюються CO до азоту і CO2. Як каталізатор найчастіше застосовують суміш родію і платини, також використовуються матеріали на основі паладію. Температурний режим відновлення — 350—800 °C, із найбільш ефективним проміжком 426—650 °C.
Зазвичай ступінь перетворення NOx складає близько 80—95%. До основних проблем цього методу відносять отруєння каталізаторів домішками нафтопродуктами, як-от цинку та фосфору, і слабкорегульовану систему контролю процесу.
Системи такого типу, так звані каталітичні конвертери, встановлюються автовиробниками у випускні системи транспортних засобів попереду глушника. Використовуючи поверхню, модифіковану паладієм та родієм, конвертер розкладає утворені оксиди азоту до простих речовин із використанням залишків неповного згоряння палива (CO, H2).
Примітки
- Moskaleva L. V. The spin-conserved reaction CH+N2→H+NCN: A major pathway to prompt no studied by quantum/statistical theory calculations and kinetic modeling of rate constant / Lin, M. C. // Proceedings of the Combustion Institute. — 2000. — Т. 28, вип. 2. — С. 2393—2401. — DOI:. (англ.)
- How do different sectors and processes contribute to emissions of NOx?. eea.europa.eu. European Environment Agency. 29 січня 2014 (оновлено 24 лютого 2015). Процитовано 28 червня 2015. (англ.)
Джерела
- Baird, C., Cann, M. Environmental Chemistry. — 5th. — New York : W. H. Freeman and Company, 2012. — P. 76—101. — ISBN 978-1-4292-7704-4. (англ.)
- Tsirulnikov, L., Guarco, J., Webster, T. Burners for Industrial Boilers // Industrial Burners Handbook / Baukal Jr., Charles E., editor. — Boca Raton, FL : CRC Press, 2004. — ISBN 0-8493-1386-4. (англ.)
- Allen, David T. Air Pollution // Kirk-Othmer Encyclopedia of Chemical Technology. — 4th. — New York : John Wiley & Sons, 2004. — Vol. 1. — P. 372. — ISBN 978-0-471-48517-9. — DOI: (англ.)
- Berglund, Ronald L. Exhaust Control, Industrial // Kirk-Othmer Encyclopedia of Chemical Technology. — 4th. — New York : John Wiley & Sons, 2004. — Vol. 9. — P. 510—512. — ISBN 978-0-471-48517-9. — DOI: (англ.)