Оксид азоту(IV)
Окси́д азо́ту(IV), нітроге́н(IV) окси́д, діокси́д азо́ту — неорганічна сполука складу NO2. За звичайних умов є газом червоно-бурого кольору, з характерним гострим запахом або жовтуватою рідиною. Газ є сумішшю оксиду NO2 та його димеру N2O4. Ця суміш при 21,15 °С згущується на прозору жовту рідину, а при -11,2°С — замерзає в безбарвну масу. При температурі 140 °C діоксид азоту складається тільки з молекул NO2, він дуже темного, майже чорного кольору.
| Оксид азоту(IV) | |
|---|---|
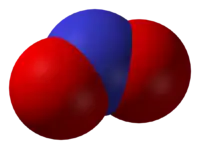 | |
 | |
| Інші назви | бурий газ |
| Ідентифікатори | |
| Номер CAS | 10102-44-0 |
| Номер EINECS | 233-272-6 |
| Назва MeSH | D01.362.635.600, D01.625.550.525 і D01.650.550.587.625 |
| ChEBI | 33101 |
| RTECS | QW9800000 |
| SMILES |
N(=O)[O][1] |
| InChI |
InChI=1S/NO2/c2-1-3 |
| Номер Гмеліна | 976 |
| Властивості | |
| Молекулярна формула | NO2 |
| Молярна маса | 46,0055 г/моль |
| Зовнішній вигляд | бурий газ або жовтувата рідина |
| Густина | 2,0527 г/л (газ) 1,491 г/см³ (рідина, 0 °C) 1,536 г/см (твердий) |
| Тпл | -11,2 °C |
| Ткип | 21,1 °C |
| В'язкість | 0,532 мПа·с (0 °C) 0,402 мПа·с (25 °C) |
| Структура | |
| Дипольний момент | 0,316 ± 0,010 D |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
33,2 кДж/моль |
| Ст. ентропія S |
240,1 Дж/(моль·K) |
| Теплоємність, c |
37,2 Дж/(моль·K) |
| Небезпеки | |
| Індекс ЄС | 007-002-00-0 |
| Класифікація ЄС | |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Отримання
Промислове отримання оксиду NO2 пролягає в окисненні повітрям аміаку та продукту реакції — оксиду NO:
У лабораторії NO2 зазвичай отримують дією концентрованої нітратної кислоти на мідь:
Також його можна отримати термічним розкладанням нітрату свинцю, однак при проведенні реакції слід дотримуватися обережності:
Хімічні властивості
Зріджений оксид NO2 частково димеризується в N2O4 (у діапазоні температур −11,2…20,7 °C):
При температурі понад 150 °C оксид азоту(IV) починає розкладатися
У воді NO2 диспропорціонує з утворенням нітратної кислоти та, в залежності від умов, оксидів N2O3 або NO:
При пропусканні оксиду крізь луги утворюється суміш нітратів та нітритів, а при окисненні реакційної суміші — тільки нітрати:
Діоксид азоту відновлюється воднем у присутності каталізаторів (платини, нікелю):
Діоксид азоту проявляє себе як дуже сильний окисник. Так, він легко окиснює значну кількість неметалів, металів, а також їхніх сполук:
Небезпека
Токсичність
Діоксид азоту дуже отруйний при вдиханні. Однак, інгаляцій зазвичай можна уникнути, адже його легко виявити по запаху, навіть при низьких концентраціях. В лабораторіях одним з джерел NO2 є димна азотна кислота, яка розкладається при температурі вище 0 °С. Одним з симптомів отруєння є набряк легенів, який, як правило, з'являється через кілька годин після вдихання низьких, але потенційно небезпечних доз NO2. Крім того, низькі концентрації (4 проміле) можуть призвести до затримки дихання . Існує ряд доказів, які свідчать, що довгостроковий вплив NO2 при концентраціях вище 40—100 мкг/м³ може знизити функцію легенів і збільшити ризик виникнення респіраторних захворювань[2].
Забруднення
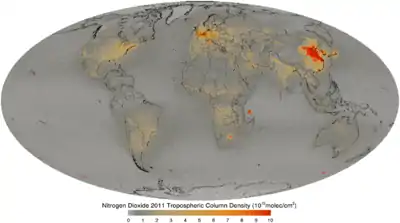
Найбільшими джерелами NO2 є двигуни внутрішнього згоряння,[3] теплові електростанції і, в меншій мірі, заводи з переробки целюлози. Бутанові газові обігрівачі та печі є також джерелами NO2. У побуті, гасові обігрівачі та газові обігрівачі є джерелами діоксиду азоту. Діоксид азоту утворюється, також, і в результаті ядерних випробувань, і відповідає за червоний колір грибовидної хмари.
Разом із оксидом NO (так звані оксиди NOx), діоксид азоту є одним з найбільших забруднювачів атмосфери, в декількох районах землі його концентрація досягає 30 мкг/м³, що лише на декілька одиниць менше ніж гранично допустима концентрація. Діоксид азоту відіграє важливу роль в хімії атмосфери, в тому числі в утворенні тропосферного озону. У 2005 році учені з Університету Каліфорнії припускали взаємозв'язок між рівнем NO2 і синдромом раптової дитячої смертності[4].
Діоксид азоту також утворюється під час грози. Такий процес називають атмосферною фіксацією азоту. Дощ, який утворюється при таких бурях, містить певну кількість азотних добрив.
Примітки
- Nitrogen peroxide
- Health Aspects of Air Pollution with Particulate Matter,Ozone and Nitrogen Dioxide. Всесвітня організація охорони здоров'я. 13–15 January 2003. с. 48. Процитовано 19 листопада 2011.
- Son, Busoon; Wonho Yang, Patrick Breysse, Taewoong Chung and Youngshin Lee (March 2004). Estimation of occupational and nonoccupational nitrogen dioxide exposure for Korean taxi drivers using a microenvironmental model. Environmental Research 94 (3): 291–296. PMID 15016597. doi:10.1016/j.envres.2003.08.004. Архів оригіналу за 5 квітня 2011. Процитовано 25 лютого 2008.
- Sids Linked to Nitrogen Dioxide Pollution. Архів оригіналу за 24 червня 2013. Процитовано 25 лютого 2008.
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Handbook of Preparative Inorganic Chemistry / G. Brauer. — 2nd. — New York : Academic Press, 1963. — Vol. 1. — 1859 p. (англ.)
- Thiemann M., Scheibler E., Wiegand K. W. Nitric Acid, Nitrous Acid, and Nitrogen Oxides // Ullmann's Encyclopedia of Industrial Chemistry. — 6th. — Weinheim : Wiley-VCH, 2005. — P. 44—45. — DOI: (англ.)
- Реми Г. Курс неорганической химии / А. В. Новоселова. — М. : ИИЛ, 1963. — Т. 1. — 922 с. (рос.)
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ / Р. А. Лидин. — 3-е. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0. (рос.)
- Деркач Ф. А. Хімія. — Львів : Львівський університет, 1968. — 312 с.