Бринцидофовір
Бринцидовір (англ. Brincidofovir, відомий також як CMX001) — експериментальний синтетичний противірусний препарат, що був розроблений американською компанією Chimerix, що розміщена у місті Дюрем у штаті Північна Кароліна.
 | |
| Систематична назва (IUPAC) | |
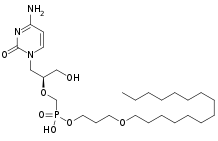
| [(2S)-1-(4-amino-2-oxopyrimidin-1-yl)-3-hydroxypropan-2-yl]oxymethyl-(3-hexadecoxypropoxy)phosphinic acid | |
| Ідентифікатори | |
| Номер CAS | |
| Код ATC | ? |
| PubChem | |
| Хімічні дані | |
| Формула | C27H52N3O7P |
| Мол. маса | 561,70 г/моль |
| SMILES | & |
| Фармакокінетичні дані | |
| Біодоступність | НД |
| Метаболізм | НД |
| Період напіврозпаду | НД |
| Виділення | НД |
| Терапевтичні застереження | |
| Кат. вагітності | |
| Лег. статус |
? (US) |
| Використання | перорально |
Спектр активності та механізм дії
Бринцидофовір був розроблений для лікування тих хвороб, які спричинюють цитомегаловірус, аденовіруси, вірус натуральної віспи і збудник гарячки Ебола.[1] По своєму механізму дії бринцидофовір є проліками цидофовіру та належить до групи нуклеозидних аналогів.[2] Після перорального застосування ліпідна складова препарату покращує проходження цидофовіру всередину клітин та забезпечує високу внутрішньоклітинну та плазмову концентрацію активного метаболіту цидофовіру, що дозволяє підвищувати його ефективність проти ДНК-вмісних вірусів із високою біодоступністю при пероральному прийомі.[3]
У дослідженнях на тваринах бринцидофовір виявляв активність проти цитомегаловірусу, аденовірусів, BK-вірусу[4], вірусів натуральної віспи і простого герпесу.[2][5] Згідно попередніх результатів досліджень in vitro, бринцидофовір виявляє активність також проти вірусу гарячки Ебола, що можна вважати до деякої міри парадоксальним явищем, тому що вірус гарячки Ебола не містить ДНК, а лише РНК.[6]
Застосування
Уперше бринцидофовір був застосований як експериментальний препарат проти аденовірусної інфекції у березні 2014 року для лікування семирічного американського хлопчика зі зниженим імунітетом після тривалого лікування раку за наполяганням батьків дитини. Після короткотривалого прийому препарату стан хлопчика значно покращився, і, згідно клінічних обстежень, вірусне навантаження у клітинах хворого уже після трьох доз препарату значно зменшилось. Ці дані прискорили отримання дозволу компанією «Chimerix» від FDA на подальші клічні випробування препарату.[7] Після дослідження безпечності застосування препарату у більше чим 1000 осіб, бринцидофовір був допущений до ІІІ фази клінічних досліджень по застосування препарату проти цитомегаловірусу та аденовірусу, яка триває у 2014 році.[1] Згідно результатів попередніх клінічних досліджень, бринцидофовір дозволений для застосування проти аденовірусів, цитомегаловірусу та вірусу натуральної віспи.[8]
6 жовтня 2014 року компанія «Chimerix» отримала дозвіл від FDA на невідкладні дослідження ефективності бринцидофовіру проти вірусу гарячки Ебола. Бринцидофовір був застосований у першого пацієнта із діагнозом гарячки Ебола у Сполучених Штатах Америки[9] Хворий почав приймати препарат на шостий день після госпіталізації. Незважаючи на проведене лікування, стан хворого продовжував залишатися важким, і він помер за чотири доби після початку застосування препарату.[10][11] Бринцидофовір був застосований також у лікуванні іншого пацієнта із гарячкою Ебола, що знаходився на лікуванні у Медичному Центрі Небраски. У цьому випадку хворому вдалось перебороти захворювання, і він був виписаний із лікарні 22 жовтня 2014 року.[12]
16 жовтня компанія «Chimerix» оголосила про дозвіл FDA на початок ІІ фази клінічних досліджень що до ефективності, толерантності та безпечності бринцидофовіру при застосуванні проти вірусу гарячки Ебола. Компанія заявила, що готова надати препарат негайно для продовження клінічних досліджень.[13]
На грудень 2014 року заплановано початок програми дослідження експериментальних ліків та експериментальної сироватки проти гарячки Ебола у Гвінеї. До програми дослідження ефективності експериментальних ліків включені два препарати — фавіпіравір та бринцидофовір. Попередньо заплановано, що дослідження бринцидофовіру будуть проводитись під наглядом учених із Оксфордського університету та міжнародного консорціуму ISARIC. Планується, що результати дослідження будуть опубліковані у лютому 2015 року.[14]
Примітки
- http://www.chimerix.com/discovery-clinical-trials/brincidofovir/brincidofovir-for-ebola/ Архівовано 9 грудня 2014 у Wayback Machine. (англ.)
- Архівована копія. Архів оригіналу за 9 грудня 2014. Процитовано 6 грудня 2014.
- http://informahealthcare.com/doi/abs/10.1586/14787210.2014.948847 (англ.)
- вірус з роду Polyomavirus
- Quenelle, Debra C.; Lampert, Bernhardt; Collins, Deborah J.; Rice, Terri L.; Painter, George R.; Kern, Earl R. (2010). Efficacy of CMX001 against Herpes Simplex Virus Infections in Mice and Correlations with Drug Distribution Studies. The Journal of Infectious Diseases 202 (10): 1492–9. PMC 2957530. PMID 20923374. doi:10.1086/656717. (англ.)
- David Kroll (7 жовтня 2014). Chimerix's Brincidofovir Given To Dallas, Nebraska Ebola Patients. forbes.com. (англ.)
- http://medportal.ru/mednovosti/news/2014/03/25/159josh (рос.)
- http://ir.chimerix.com/releasedetail.cfm?releaseid=874647 Архівовано 8 жовтня 2014 у Wayback Machine. (англ.)
- Dallas Ebola Patient Receives Experimental Drug. The Huffington Post. 6 Жовтня 2014. Процитовано 8 Жовтня 2014. (англ.)
- Thomas Duncan, the Texas Ebola patient, has died. Washington Post. Процитовано 8 Жовтня 2014. (англ.)
- Dallas Ebola patient waited nearly a week for experimental drug; family claims bias (англ.)
- http://www.nbcnews.com/storyline/ebola-virus-outbreak/young-healthy-how-nbc-news-freelancer-ashoka-mukpo-survived-ebola-n231681
- Chimerix to Conduct Ebola Drug Trial: Drug Company Gets FDA Approval to Start Trial Immediately in Infected Patients (англ.)
- http://vsyapravda.com/category/pub_obchestvo/likhoradka_ebola_eksperimentalnye_lekarstva_favipiravir_i_brintsidofovir_ispytayut_v_dekabre_2014_goda-1.423717 (рос.)