Гігрин
Гігрин — алкалоїд, відноситься до похідних піролідину. У структурі молекули містить просте піролідинове кільце. За звичайних умов гігрин є безбарвною рідиною. Добувається із коки — Erythroxelon Coca Lam.
| Гігрин | |
|---|---|
 Структурна формула гігрину |
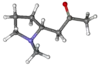 Просторова модель молекули гігрину |
| Назва за IUPAC | (R)-1-(1-метилпіролідин-2-ил)-пропан-2-он |
| Систематична назва | Гігрин |
| Ідентифікатори | |
| Номер CAS | 496-49-1 |
| PubChem | 440933 |
| Номер EINECS | 207-822-0 |
| KEGG | C06179 |
| ChEBI | CHEBI:46750 |
| SMILES |
CC(=O)C[C@H]1CCCN1C |
| InChI |
1S/C8H15NO/c1-7(10)6-8-4-3-5-9(8)2/h8H,3-6H2,1-2H3/t8-/m1/s1 |
| Номер Бельштейна | 80977 |
| Властивості | |
| Молекулярна формула | C8H15NO |
| Молярна маса | 141,21 г/моль |
| Молекулярна маса | 141 а. о. м. |
| Зовнішній вигляд | рідина |
| Густина | 0,935 г/см3 |
| Ткип | 193–195 °C |
| Оптична активність [α]D | 1,30 ° |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Історія
Алкалоїд був відкритий вченими Валером і Лоссеном у 1862 році в листках однієї із різновидностей коки, відомої під назвою «куско»[1]. Ця рослина в дикому вигляді росте у Південній Америці.
У 1939 році гігрин був виділений Г. В. Лазур'євським із одного із видів [берізка|берізки] – Convolvus hammadae V. Petr[1].
Фізичні властивості
Гігрин — це безбарвна рідина з температурою кипіння 193—195 ºС при звичайному тиску або 92—94 ºС при тиску 20 мм[1]. Проявляє слабкий лівий обертовий момент. Леткий з водяною парою.
Будова та хімічні властивості
Утворення оксиму з гігрину свідчить про те, що в його молекулі атом Оксигену знаходиться у вигляді карбонільної групи. Гігрин є сильною третинною основою[1].
При окисненні гігрину хромовою кислотою отримують кислоту складу . Її називають гігриновою кислотою. При сухій перегонці вона розкладається на і N-метилпіролідин. Звідси стає зрозуміло, що ця кислота – це N-метилпіролідинкарбонова кислота[1]:

Так як теоретично можливими є дві піроліднкарбонові кислоти – α і β, то будова гігринової кислоти залишалася невідомою поки її не добули синтетичним шляхом. Для цього з Na-малонового ефіру і було отримано бромпропіламіновий ефір, який бромуванням за методом Зелінського–Фольгарта було перетворено в α-бромпохідне. Це похідне при дії метиламіну дало метиламід N-метил-α-α-піролідинкарбрнової кислоти. Омиленням останнього було отримано N-метил-α-піролідинкарбонова кислота, яка виявилась ідентичною з гігриновою[2]
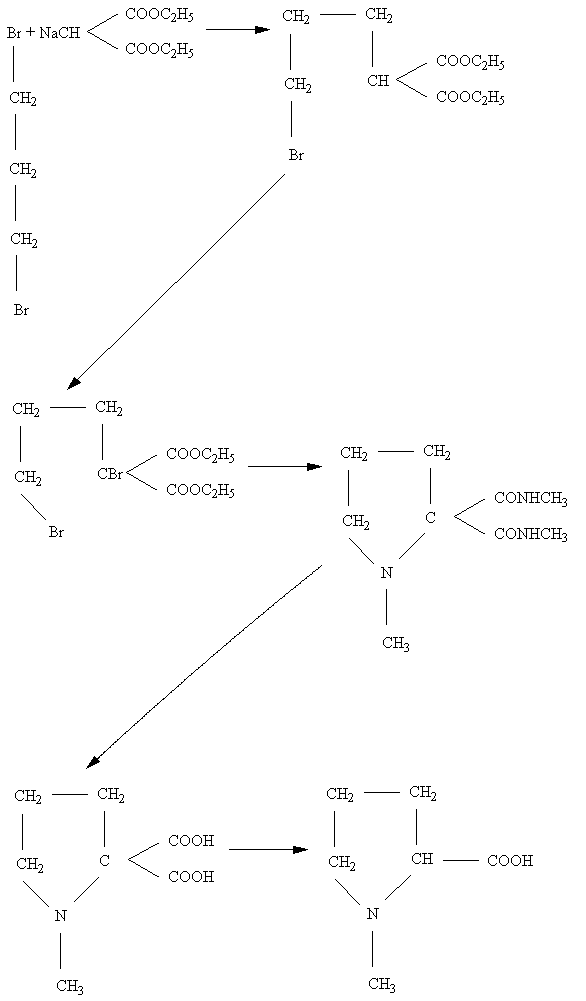
Порівнюючи між собою склад гігринової кислоти і гігрину, а також беручи до уваги кетонний характер останнього, легко передбачити, що цей алкалоїд повинен бути одним із кетонів, що відповідає гігриновій кислоті, а саме[2]:
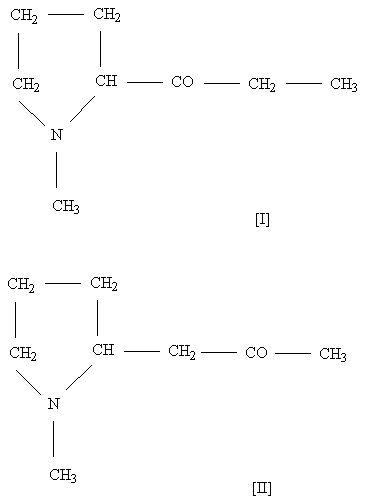
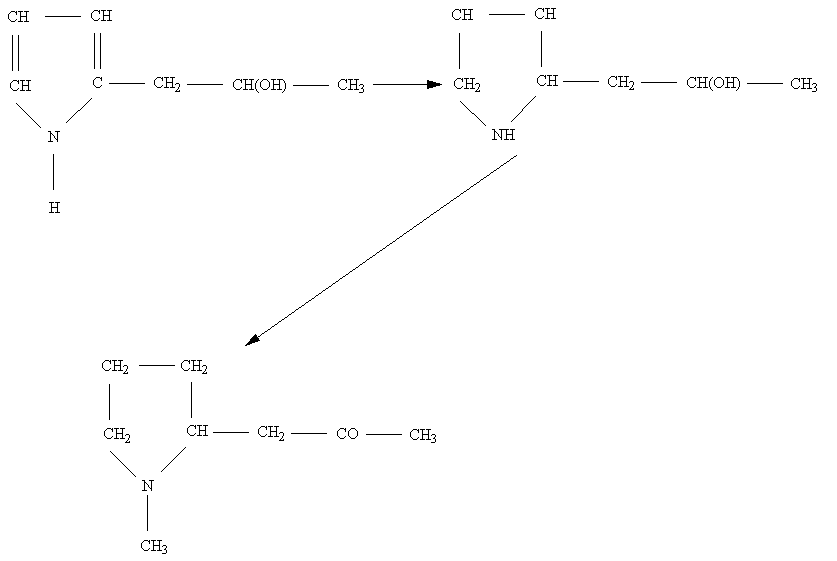
Питання будови гігрину було вирішено шляхом синтезу, який показав, що йому відповідає друга формула. Магнійорганічне похідне піролу дає при конденсації з епоксипропаном вторинний спирт[2]:

При гідрогенізації цієї речовини отримують відповідне похідне піролідину. При дії на останнє формальдегіду відбувається цікава реакція, що полягає в одночасному метилюванні Нітрогену і окисненні спиртової групи в кетонну. При цьому утворюється основа, ідентична до гігрину (реакція К. Гесса)[3]:
Примітки
- Орехов А. П., Химия алкалоидов, 33 (1955) (рос.).
- Орехов А. П., Химия алкалоидов, 34 (1955) (рос.).
- Орехов А. П., Химия алкалоидов, 35 (1955) (рос.).
Джерела
- Орехов А.П. Химия алкалоидов. — 2. — Москва : Академии наук СССР, 1955. — 864 с. — 6000 прим. (рос.)