Гіперфорин
Гіперфорин — речовина рослинного походження, що синтезується низкою представників роду Hypericum, зокрема Hypericum perforatum (звіробій). [2] Гіперфорин може бути причетний до деяких фармакологічних ефектів звіробою зокрема, до його антидепресантних ефектів. [3] [4] [5]
 | |
 | |
| Систематична назва (IUPAC) | |
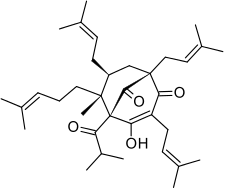
| (1R,5S,6R,7S)-4-Hydroxy-6-methyl-1,3,7-tris(3-methylbut-2-en-1-yl)-6-(4-methylpent-3-en-1-yl)-5-(2-methylpropanoyl)bicyclo[3.3.1]non-3-ene-2,9-dion | |
| Ідентифікатори | |
| Номер CAS | |
| Код ATC | none |
| PubChem | |
| DrugBank | |
| Хімічні дані | |
| Формула | C35H52O4 |
| Мол. маса | ? |
| SMILES | & |
| Фізичні дані | |
| Т плавлення | 79–80 °C (Помилка виразу: незрозумілий розділовий знак «–» °F) |
| Розчинність у воді | 0.66 мг/мл (20 °C) |
| Фармакокінетичні дані | |
| Біодоступність | ? |
| Метаболізм | Печінка та CYP3A & CYP2B |
| Період напіврозпаду | ? |
| Виділення | ? |
| Терапевтичні застереження | |
| Кат. вагітності |
? |
| Лег. статус |
OTC (US) unscheduled in most countries, with the notable exception of Ireland (Rx-only)[1] |
| Залежність | Nil |
| Використання | Oral |
Поширення
Гіперфорин в значних кількостях наразі виявлений лише у звіробої продірявленому Hypericum perforatum та деяких інших споріднених видах, зокрема Hypericum calycinum. [2] Він накопичується в олійних залозах, маточках і плодах, ймовірно, виконуючи в рослині захисну функцію . [6] Перші екстракції сполуки з природного матеріалу проводили етанолом. Вихід речовини в стосунку до маси сирого екстракту становив 1:7, проте це була суміш гіперфорину та адгіперфорину. [3] [7] [8] В подальшому метод екстракції було модернізовано з використанням ліпофільної рідинної екстракції вуглекислим газом СО2, при цьому вихід гіперфорину у відношенні до сирого екстракту становив 1:3.
Інші види Hypericum містять низьку кількість гіперфорину. [9]
Хімічні властивості
Гіперфорин є пренільованим похідним флороглюцину. [3] [4] Структуру гіперфорину було з’ясовано дослідницькою групою Інституту біоорганічної хімії ім. Шемякіна ( Академія наук СРСР ) та опубліковано у 1975 р. [10] [11] У 2010 році повідомлялося про повний синтез неприродного енантіомеру гіперфорину, який вимагав приблизно 50 синтетичних перетворень. [12] Також у 2010 році було здійснено тотальний енантіоселективний синтез правильного енантіомеру. Ретросинтетичний аналіз спирався на структурну симетрію гіперфорину та його біосинтетичний шлях. [13]
Гіперфорин нестійкий в присутності світла та кисню. [14] Часті окислені форми містять гемікеталь / гетероциклічний міст C3-C9 або утворюють похідні фурану / пірану. [7] [8]
Фармакокінетика
Деякі фармакокінетичні дані щодо гіперфорину доступні для екстракту, що містить 5% гіперфорину. Максимальні рівні в плазмі ( C <sub id="mwWg">max</sub> ) у добровольців були досягнуті через 3,5 години після введення екстракту, що містить 14,8 мг гіперфорину. Біологічний період напіввиведення (t 1/2 ) і середній час перебування склали відповідно 9 годин і 12 годин, за розрахунковою концентрацією в плазмі стаціонарного стану 100 нг / мл (близько 180 нМ) по 3 дози на добу. В межах нормально застосовуваних доз в плазмі крові спостерігалися лінійні концентрації речовини, накопичення не відбувалось. [15]
Фармакодинаміка
Гіперфорин може бути складовою, відповідальною за антидепресантні та анксіолітичні властивості екстрактів звіробою . [2] [16] In vitro він діяв як інгібітор зворотного захоплення моноамінів (МРТ), включаючи серотонін, норадреналін, дофамін, а також GABA та глутамату, зі значеннями IC 50 0,05-0,10 мкг / мл для всіх сполук, за винятком глутамату, який знаходиться в межах 0,5 мкг / мл [17].
| Природні та напівсинтетичні аналоги Гіперфорину | |||||
 Адгіперфорин |
 Аристофорін |
 Гіперфориновий триметоксибензоат |
 Тетрагідрогіперфорин |
 Октагідрогіперфорин |
 Гіперфориновий нікотинат |
| Адгіперфорин | Аристофорін | Гіперфориновий триметоксибензоат | Тетрагідрогіперфорин | Октагідрогіперфорин | Гіперфориновий нікотинат |
Список літератури
- St John's Wort available again. Irishhealth.com (2015-10-13). Retrieved on 2020-02-11.
- Hyperforin. PubChem, US National Library of Medicine. 8 вересня 2018. Процитовано 13 вересня 2018.
- Gaid, Mariam; Biedermann, Eline; Füller, Jendrik; Haas, Paul; Behrends, Sönke; Krull, Rainer; Scholl, Stephan; Wittstock, Ute та ін. (2018). Biotechnological production of hyperforin for pharmaceutical formulation. Eur. J. Pharm. Biopharm. 126: 10–26. PMID 28377273. doi:10.1016/j.ejpb.2017.03.024.
- Ciochina, Roxana; Grossman, Robert B. (2006). Polycyclic Polyprenylated Acylphloroglucinols. Chem. Rev. 106 (9): 3963–3986. PMID 16967926. doi:10.1021/cr0500582.
- Roz, N.; Rehavi, M. (2004). Hyperforin depletes synaptic vesicles content and induces compartmental redistribution of nerve ending monoamines. Life Sci. 75 (23): 2841–2850. PMID 15464835. doi:10.1016/j.lfs.2004.08.004.
- Beerhues L (2006). Hyperforin. Phytochemistry 67 (20): 2201–7. PMID 16973193. doi:10.1016/j.phytochem.2006.08.017.
- Vajs, V.; Vugdelija, S.; Trifunović, S.; Karadžić, I.; Juranić, N.; MacUra, S.; Milosavljević, S. (2003). Further degradation product of hyperforin from Hypericum perforatum (St. John's Wort). Fitoterapia 74 (5): 439–444. PMID 12837358. doi:10.1016/S0367-326X(03)00114-X.
- Verotta, Luisella; Appendino, Giovanni; Belloro, Emanuela; Jakupovic, Jasmin; Bombardelli, Ezio (1999). Furohyperforin, a Prenylated Phloroglucinol from St. John's Wort (Hypericumperforatum). J. Nat. Prod. 1999 62 (5): 770–772. PMID 10346967. doi:10.1021/np980470v.
- Phytochemical analysis of nine Hypericum L. species from Serbia and the F.Y.R. Macedonia. Die Pharmazie 61 (3): 251–2. March 2006. PMID 16599273. Проігноровано невідомий параметр
|vauthors=(довідка) - Bystrov NS; Gupta ShR; Dobrynin VN; Kolosov MN; Chernov BK (January 1976). [Structure of the antibiotic hyperforin]. Doklady Akademii Nauk SSSR (Russian) 226 (1): 88–90. PMID 1248360.
- [The structure of hyperforin]. Tetrahedron Letters 16 (32): 2791–2794. 1975. doi:10.1016/S0040-4039(00)75241-5. Проігноровано невідомий параметр
|vauthors=(довідка) - Catalytic Asymmetric Total Synthesis of ent-Hyperforin. Angew Chem Int Ed 49 (6): 1103–6. February 2010. PMID 20063336. doi:10.1002/anie.200906678. Проігноровано невідомий параметр
|vauthors=(довідка) - Enantioselective Total Synthesis of Hyperforin. J Am Chem Soc (Submitted manuscript) 135 (2): 644–7. December 2012. PMID 23270309. doi:10.1021/ja312150d. Проігноровано невідомий параметр
|vauthors=(довідка) - Liu, F; Pan, C; Drumm, P; Ang, CY (February 2005). Liquid chromatography-mass spectrometry studies of St. John's wort methanol extraction: active constituents and their transformation. Journal of Pharmaceutical and Biomedical Analysis 37 (2): 303–12. PMID 15708671. doi:10.1016/j.jpba.2004.10.034.
- Biber, A; Fischer, H; Römer, A; Chatterjee, SS (June 1998). Oral bioavailability of hyperforin from hypericum extracts in rats and human volunteers. Pharmacopsychiatry 31 (Suppl 1): 36–43. PMID 9684946. doi:10.1055/s-2007-979344.
- Newall, Carol A.; Joanne Barnes; Anderson, Linda R. (2002). Herbal medicines: a guide for healthcare professionals. London: Pharmaceutical Press. ISBN 978-0-85369-474-8.
- Hyperforin as a possible antidepressant component of hypericum extracts. Life Sci. 63 (6): 499–510. 1998. PMID 9718074. doi:10.1016/S0024-3205(98)00299-9. Проігноровано невідомий параметр
|vauthors=(довідка)