Кислота Каро
Кислота́ Каро́ (перо́ксомо́носульфа́тна кислота́, надсульфа́тна кислота́) — неорганічна сполука, що належить до класу надкислот.
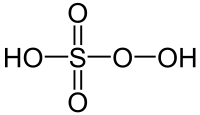
| Пероксомоносульфатна кислота | |
|---|---|
 | |
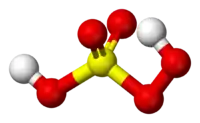 Шаро-стрижнева модель молекули | |
| Інші назви | Кислота Каро надсульфатна кислота Пероксомоносульфатна кислота |
| Ідентифікатори | |
| Номер CAS | 7722-86-3 |
| PubChem | 2754594 |
| Номер EINECS | 231-766-6 |
| ChEBI | 29286 |
| SMILES |
O=S(=O)(O)OO |
| InChI |
1/H2O5S/c1-5-6(2,3)4/h1H, (H,2,3,4) |
| Номер Гмеліна | 101039 |
| Властивості | |
| Молекулярна формула | H2SO5 |
| Молярна маса | 114,04 г/моль |
| Зовнішній вигляд | Кристали без кольору |
| Густина | 1,7—1,8 г/см3, тверде тіло[1] |
| Ткип | розкладається |
| Розчинність (вода) | добре розчинна |
| Структура | |
| Координаційна геометрія |
тетраедрична |
| Небезпеки | |
| Головні небезпеки | |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Зовнішній вигляд
Безбарвні кристали. Температура плавлення 45 °C.
Історія відкриття
Її відкрив німецький хімік Генріх Каро в кінці XIX століття.
Отримання
- Реакція хлорсульфонової кислоти і пероксиду водню:
- Реакція персульфату калію і сульфатної кислоти[2]:
- Взаємодією концентрованих пероксиду водню і сульфатної кислоти:
Хімічні властивості
- Окисляє анілін до нітробензену.
- Окисляє йодид іон до йоду.
- З ацетоном дає перекис ацетону.
Токсикологія і безпека
Пероксомоносульфатна кислота є сильним окисником, і багато органічних речовин при контакті з нею спалахують.
Застосування
Пероксомоносульфатну кислоту вживають для дезінфекції (наприклад, басейнів), а її солі металів з лугами застосовують при делігніфікації деревини.
Амонійні, калійні і натрієві солі кислоти Каро служать як ініціатори радикальної полімеризації у травленні, покращенні ґрунту і знебарвленні масел. Пероксомоносульфат калію KOSO 2OOH використовується як окислювач.
Примітки
- http://web.archive.org/web/20060819183428/http://www.solvayinterox.com.au/MSDS/MSDS%20-%20Caros%20Acid.pdf
- Карякін Ю. В., Ангелов И. И. Чистые химические вещества М., Химия, 1974 с 178–179
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
