Умбеліферон
Умбеліферон (англ. Umbelliferone; 7-гідроксикумарин, скіметин) — жовтуваті кристали, добре розчинні у етанолі, хлороформі і оцтової кислоти, погано розчинні у воді та диетиловому ефірі.
| Умбеліферон | |
|---|---|
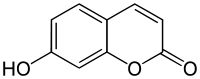 Хімічна структура умбеліферону | |
 | |
| Інші назви | 7-гідроксикумарин, гідрангін, скіметин, бета-умбеліферон |
| Ідентифікатори | |
| Номер CAS | 93-35-6 |
| PubChem | 5281426 |
| Номер EINECS | 202-240-3 |
| KEGG | C09315 |
| ChEBI | 27510 |
| SMILES |
c1cc(cc2c1ccc(=O)o2)O |
| InChI |
1/C9H6O3/c10-7-3-1-6-2-4-9(11)12-8(6)5-7/h1-5,10H |
| Номер Бельштейна | 127683 |
| Номер Гмеліна | 1220112 |
| Властивості | |
| Молекулярна формула | C9H6O3 |
| Молярна маса | 162,14 г/моль |
| Зовнішній вигляд | жовтувато-білі кристали, порошок без запаху |
| Тпл | 230 |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Умбеліферон вперше був виявлений у рослинах родини Umbelliferae окружкові, звідки й отримав свою назву. Міститься у значній кількості видів рослин і є ключовим метаболітом в біосинтезі різних природних кумаринів, піранокумаринів і фурокумаринів.
Синтез і властивості
Класичний метод синтезу умбеліферону — конденсація Пехмана яблучної кислоти і резорцину в присутності сірчаної кислоти[1], реакція йде через декарбоксилювання in situ яблучної кислоти з утворенням формілоцтової кислоти, яка потім реагує з резорцином.
Подібно до інших кумаринів, умбеліферон інтенсивно поглинає в ультрафіолетовій області, поглинання посилюється при утворенні феноляту, який обумовлює яскраво-блакитну флуоресценцію лужних розчинів умбеліферону, завдяки чому він використовується як кислотно-основний флуоресцентний індикатор при рН 6,5-8,0.
Знаходження в природі і біосинтез
Умбеліферон в досить значних кількостях міститься в рослинах родин окружкових, айстрових і підродини рутових; може бути виділений із продуктів сухої перегонки окружкових рослин родів Ferula, Angelica і Heracleum. Крім вільного умбеліферону в рослинах містяться його глікозиди і прості етери із сексвітерпеновими спиртами («терпенові кумарини», переважно в рослинах роду Ferula).
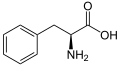
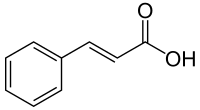
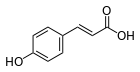
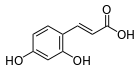
Біосинтез йде за фенілпропаноідним шляхом із фенілаланіну, з якого синтезується корична кислота, піддається гидроксилюванню в положення 4 під дією ферменту циннамат-4-гідрокислази. Утворена в результаті p-кумарова кислота гідроксилюється за положенням 2 при каталізі циннаміт/кумарат-2-гідроксилази з утворенням 2,4-дигідроксикумарової (умбелової) кислоти. Внутрішньомолекулярне ацилювання 2-гідроксигрупи карбоксилом умбелової кислоти призводить до утворення лактона — умбелліферону[2]:
Примітки
- George, Ernest; J. Moir. The Preparation of Umbelliferone // Transactions of the Royal Society of South Africa. — 1925. — Т. 13, № 3 (15 August). — С. 255—257. — ISSN 0035-919X. — DOI:. Процитовано 2013-08-02.
- Pathway: umbelliferone biosynthesis // MetaCyc