Мікросателітна нестабільність
Мікросателітна нестабільність (Microsatellite instability, MSI) - це стан генетичної гіперзмінюваності (схильність до мутації), що є наслідком хибної репарації помилково спарених нуклеотидів (mismatch repair, MMR). Наявність MSI є фенотипним проявом того, що MMR нормально не функціонує.
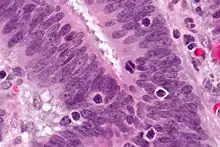
MMR виправляє помилки, що спонтанно виникають під час реплікації ДНК (невідповідність нуклеотидних основ або короткі вставки та делеції). Білки, які беруть участь у ММR, виправляють помилки полімерази, утворюючи комплекс, який зв’язується з невідповідною ділянкою ДНК, вирізає помилку та вставляє правильну послідовність на своє місце.[1] Клітини з аномально функціонуючим MMR не можуть виправити помилки, що виникають під час реплікації ДНК, і, отже, накопичують їх. Це спричиняє утворення нових мікросателітних фрагментів. Аналізи на основі полімеразної ланцюгової реакції (ПЛР) можуть виявити ці нові мікросателіти та надати докази наявності MSI.
Мікросателіти - це повторні послідовності ДНК. Ці послідовності можуть бути складені з повторюваних одиниць довжиною від однієї до шести пар основ. Хоча довжина мікросателітів сильно відрізняється від особи до особи і формує індивідуальний «відбиток пальців» ДНК, у кожної людини є мікросателіти певної довжини. Найпоширеніший мікросателіт у людини - це двонуклеотидне повторення нуклеотидів С і А, яке у геномі зустрічається десятки тисяч разів. Мікросателіти також відомі як повтори простих послідовностей (simple sequence repeats, SSR).
Структура
Структура мікросателітної нестабільності складається з повторюваних нуклеотидів, найчастіше зустрічаються повтори GT/CA.[2]
Дослідники ще не підтвердили точне визначення структури MSI. Хоча всі погоджуються, що мікросателіти є повторюваними послідовностями, тривалість послідовностей залишається під питанням. Деякі дослідження говорять про те, що MSI - це короткі тандемні повторення послідовностей ДНК від однієї до шести пар основ по всьому геному, в той час як інші дослідження припускають, що їх діапазон може бути від двох до п'яти.[3]
Хоча дослідники не погоджуються щодо конкретного порогу кількості тандемних повторень, які формують мікросателіт, існує консенсус щодо їх відносного розміру. Довші послідовності називаються мінісателітами, а ще довші послідовності називаються сайтами сателітної ДНК. Одні вчені виділяють серед цих трьох категорій мінімальну кількість пар основ, а інші використовують мінімальну кількість повторюваних одиниць. Більшість повторів відбувається в ділянках, що не транслюються, зокрема інтронах. Однак мікросателіти, що зустрічаються в кодуючих ділянках, часто гальмують наступний ланцюг подій. Мікросателіти складають приблизно три відсотки геному людини або більше мільйона фрагментів ДНК. Щільність мікросателітів збільшується з розміром геному і спостерігається вдвічі більше на кінцях плечей хромосоми, ніж у тілах хромосоми.[4]
Форма та функція
Мікросателітна нестабільність була відкрита в 1970-80-х роках. Першим захворюванням людини, яке пов'язали з MSI, була ксеродерма. Ця хвороба є результатом мутацій двох алелів, що беруть участь у екцизійній репарації нуклеотидів.
У широкому сенсі MSI є результатом нездатності білків системи репарації помилково спарених нуклеотидів виправити помилку реплікації ДНК. Реплікація ДНК відбувається у синтетичній фазі клітинного циклу; помилка, що створює ділянку MSI, відбувається під час другого етапу реплікації. Оригінальний ланцюжок залишається неушкодженим, але дочірний ланцюжок має мутацію зсуву рамки через "прослизання" ДНК-полімерази. Зокрема, ДНК-полімераза ковзає, створюючи тимчасовий цикл вставки-делеції, який зазвичай розпізнається білками MMR. Однак, коли білки MMR не функціонують належним чином, як у випадку з MSI, цей цикл призводить до мутації зсуву рамки, або шляхом вставки, або делеції, утворюючи нефункціональні білки.[5]
MSI є унікальним для ДНК поліморфізмів тим, що помилки реплікації різняться за довжиною нуклеотидів, а не за послідовністю. Швидкість і напрям мутацій у результаті MSI, є головними компонентами у визначенні генетичних відмінностей. На сьогоднішній день вчені погоджуються, що коефіцієнти мутації різняться в положенні локусів. Чим більше довжина MSI, тим більша швидкість мутації.[4]
Хоча більшість мутацій MSI є результатом зсуву рамки, іноді вони виникають внаслідок гіперметилювання промотору hMLH1 (білка MMR). Гіперметилювання відбувається, коли до нуклеотиду ДНК додається метильна група, що призводить до сайленсінгу генів, що і призводить до MSI.[6]
Дослідники показали, що окислювальне пошкодження спричиняє мутацію зсуву рамки, утворюючи таким чином MSI, але їм ще доведеться розкрити точний механізм цього явища. Було показано, що чим більшому окислювальному стресу піддається система, тим більше шансів появи мутації. Крім того, каталаза зменшує шанси мутацій, тоді як мідь і нікель збільшують їх, збільшуючи відновлення пероксидів. Деякі дослідники вважають, що окислювальний стрес на конкретних локусах призводить до зупинки ДНК-полімерази на цих ділянках, створюючи середовище для "прослизання" ДНК.[7]
Спочатку науковці вважали, що MSI є випадковим процесом, але є дані, що дозволяють припустити, що MSI цілеспрямовано уражає певні гени, список яких зростає. Приклади включають в себе ген рецептора трансформуючого фактора росту бета і ген BAX. Ураження кожної мішені призводить до появи різних фенотипів та патологій.[8]
Клінічне значення
Мікросателітна нестабільність пов’язана з раком товстої кишки, шлунка, ендометрію, яєчників, гепатобіліарного тракту, сечовивідних шляхів, мозку та шкіри. MSI найбільш поширена у зв'язку з раком товстої кишки. Щороку в світі спостерігається понад 500 000 випадків цієї пухлини. За результатами дослідження понад 7000 пацієнтів, розділених за типом мікросателітної нестабільності у пухлинах на групи з високою мікросателітною нестабільністю (MSI-H), низькою нестабільністю (MSI-L) або стабільну групу (MSS), особи з пухлинами MSI-H мали на 15% більш позитивний прогноз виживаності порівняно з MSI-L або MSS пухлинами.[9]
Колоректальні пухлини з мікросателітною нестабільністю виявляються в правій товстій кишці, пов'язані з малою диференціацією, мають високу муциногенну активність, більшу інфільтрацію лімфоцитами, та наявністю реакції, подібної до хвороби Крона (Крон-подібна). Пухлини з високою мікросателітною нестабільністю, демонструють меншу частоту метастазування, ніж інші варіанти колоректального раку. Як продемонстровано попередніми дослідженнями, пухлини з високою мікросателітною нестабільністю частіше маніфестують на II стадії, ніж на ІІІ.[3]
Вчені дослідили зв'язок MSI з вакуолярними білками сортування (VPS). Як і MSI, VPS пов'язані з раком шлунка та товстої кишки. Одне дослідження повідомляє, що білки VPS були пов'язані з MSI-H пухлинами, але не з MSI-L пухлинами, таким чином, обмежуючи зв'язок VPS з MSI-H пухлинами.[10]
Крім того, дослідники погоджуються, що статус MSI-H підтверджує діагноз синдрому Лінча, дає прогноз відсутності метастазування та дозволяє менш агресивні схеми лікування. Синдром Лінча асоціюється з мікросателітною нестабільністю і збільшує ризик раку товстої кишки, ендометрію, яєчників, шлунка, тонкої кишки, гепатобіліарного тракту, сечовивідних шляхів, мозку та шкіри.[3]
В одному з досліджень за участі понад 120 пацієнтів із синдромом Лінча, Крон-подібна реакція була пов'язана з MSI, та "пухлинно-специфічними неопептидами, що утворюються під час канцерогенезу MSI-H". У цьому дослідженні далі підтверджено, що "наявність антиметастатичного імунного захисту у пацієнтів з Крон-подібною реакцією та MSI-H може пояснити те, що ад'ювантна хіміотерапія 5-фторурацилом не має сприятливих чи навіть несприятливих наслідків у цій популяції". Дослідники припускають, що дія лімфоцитів проти MSI-H при Крон-подібній реакції запобігає метастазуванню пухлини.[11]
Пухлини з мікросателітною нестабільністю у 15% випадків спорадичного колоректального раку є результатом гіперметилювання промотору гена MLH 1, тоді як пухлини з MSI при синдромі Лінча викликані мутацією зародкової лінії в MLH 1, MSH 2, MSH 6 та PMS2.[3]
Є докази, що МСІ може бути причиною себорейних карцином. Себорейні карциноми - є підтипом синдрому Муіра-Торре. МСІ мінливо виражений при синдромі Муіра-Торре, найчастіше при супутніх патологіях у пацієнтів з раком товстої кишки. Крім того, протеїни MMR MLH 1, MSH 2, MSH6 та PMS2 мають важливе значення при періокулярній себорейній карциномі, яка спостерігається на повіці, і складає 40% випадків усіх себорейних карцином.[12]
У травні 2017 року FDA схвалив імунотерапевтичний препарат під назвою Keytruda® (pembrolizumab) (інгібітор PD-1) для пацієнтів з нерезектабельними або метастатичними солідними пухлинами, що мають високий рівень мікросателітної нестабільності (MSI-H) або дефіцит репарації помилково спарених нуклеотидів (dMMR), у випадку якщо хвороба прогресувала після попереднього лікування. Це показання не залежить від результатів оцінки експресії PD-L1, типу тканини та локалізації пухлини.[13]
Діагностика мікросателітної нестабільності
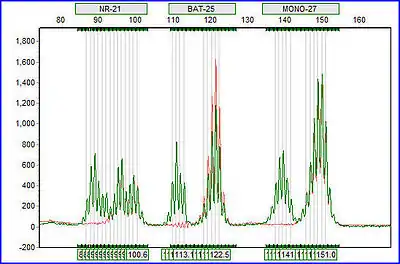
MSI є добрим маркером для визначення синдрому Лінча та визначення прогнозу лікування раку. У 1996 році в Національному інституті раку (NCI) відбувся міжнародний семінар з синдрому Лінча, який призвів до розробки «Настанов Бетесди (Bethesda Guidelines)» та визначення локусів для тестування на MSI. Під час цього першого семінару NCI було встановлено п’ять мікросателітних маркерів, необхідних для визначення наявності MSI: два мононуклеотиди, BAT25 і BAT26, і три динуклеотидні повторення, D2S123, D5S346 і D17S250. Пухлини вважаються такими, що є результатом мікросателітної нестабільності при високому рівні мікросателітної нестабільності (MSI-H), якщо присутні більше 30% маркерів MSI (2 або більше з 5 локусів). Пухлини, вважаються такими, що мають низький рівень мікросателіної нестабільності (MSI-L), при наявності менш ніж 30% маркерів MSI. Пухлини MSI-L класифікуються як пухлини альтернативної етіології. Кілька досліджень показують, що пацієнти з MSI-H пухлинами найкраще реагують на хірургічне лікування, а не на хіміотерапію та хірургічне втручання, тим самим запобіється зайва хіміотерапія.[3]

Через шість років, під час другого семінару NCI з перегляду синдрому Лінча в 2002 році, Настанови Бетесда були переглянуті (опубліковані в 2004 р.[14]), було рекомендувано нові критерії тестування на MSI. Зокрема, вони визначили п'ять мононуклеотидних локусів як були краще за суміш локусів моно та динуклеотидів, оскільки динуклеотидні локуси можуть удаватися, коли насправді вони відсутні, тим самим збільшуючи ймовірність хибнопозитивного результату MSI-H.
Перший доступний у продажу набір для діагностики MSI був випущений корпорацією Promega, Медісон, Вісконсін, під назвою Система аналізу мікросателітносї нестабільності 1.2 (RUO). З 2004 р. Promega MSI RUO широко застосовується, і понад 120 рецензованих публікацій посилаються на нього, як на золотий стандарт у визначенні статусу мікросателітної нестабільності пухлинної тканини.
Останнім часом на ринок успішно виходять інші системи для виявлення MSI на основі ПЛР в режимі реального часу . Однокроковий формат застосування із замкненою ємністю, висока точність та чутливість продуктів на основі ПЛР у реальному часі без будь-якого додаткового аналізу після ампліфікації ПЛР порівняно із традиційними (ПЛР з подальшим фрагментальним аналізом) вважаються їх безспірними перевагами.
Стійкість пухлини до хіміотерапії забезпечуюється різними механізмами. Прямі механізми містять шляхи метаболізації препарату, тоді як непрямі - шляхи, що реагують на лікування хіміотерапією. Механізм ексцезійної репарації ДНК відіграє істотну роль у відновленні ураження клітин, спричиненого хіміотерапевтичними засобами, такими як 5-фторурацил.[15]
Відкриття з 2010 року
Дослідники відкрили інший вид мікросателіної нестабільності, який називають підвищеними змінами мікросателітів у вибраних повторах тетрануклеотидів (elevated microsatellite alterations at selected tetranucleotide repeats, EMAST). Однак EMAST унікальний тим, що він походить не від MMR, і зазвичай асоціюється з мутаціями TP53 .[5]
EMAST спостерігається при різних видах раку, включаючи рак легень, голови та шиї, колоректальний, рак шкіри, сечовидільного тракту та репродуктивних органів. Органи зовнішньої локалізації мають більший потенціал для EMAST. Деякі дослідники вважають, що EMAST може бути наслідком мутагенезу. Наявність EMAST у межах біоптату, негативних за пухлинними клітинами вказують на підозру рецидиву захворювання у пацієнтів.[16]
Список літератури
- Ehrlich, ред. (2000). DNA alterations in cancer: genetic and epigenetic changes. Natick, MA: Eaton Publ. с. 178. ISBN 978-1-881299-19-6.
- Schlötterer, Christian; Harr, Bettina (March 2004). Microsatellite Instability. eLS. ISBN 978-0470016176. doi:10.1038/npg.els.0000840.
- Role of microsatellite instability in the management of colorectal cancers. Digestive and Liver Disease 45 (6): 441–9. June 2013. PMID 23195666. doi:10.1016/j.dld.2012.10.006. Проігноровано невідомий параметр
|vauthors=(довідка) - Microsatellites: simple sequences with complex evolution. Nature Reviews. Genetics 5 (6): 435–45. June 2004. PMID 15153996. doi:10.1038/nrg1348. Проігноровано невідомий параметр
|vauthors=(довідка) - Microsatellite instability in colorectal cancer. Gastroenterology 138 (6): 2073–2087.e3. June 2010. PMC 3037515. PMID 20420947. doi:10.1053/j.gastro.2009.12.064. Проігноровано невідомий параметр
|vauthors=(довідка) - Microsatellites within genes: structure, function, and evolution. Molecular Biology and Evolution 21 (6): 991–1007. June 2004. PMID 14963101. doi:10.1093/molbev/msh073. Проігноровано невідомий параметр
|vauthors=(довідка) - Induction of microsatellite instability by oxidative DNA damage. Proceedings of the National Academy of Sciences of the United States of America 95 (21): 12468–73. October 1998. Bibcode:1998PNAS...9512468J. PMC 22854. PMID 9770509. doi:10.1073/pnas.95.21.12468. Проігноровано невідомий параметр
|vauthors=(довідка) - Carcinogenesis and microsatellite instability: the interrelationship between genetics and epigenetics. Carcinogenesis 29 (4): 673–80. April 2008. PMID 17942460. doi:10.1093/carcin/bgm228. Проігноровано невідомий параметр
|vauthors=(довідка) - Systematic review of microsatellite instability and colorectal cancer prognosis. Journal of Clinical Oncology 23 (3): 609–18. January 2005. PMID 15659508. doi:10.1200/JCO.2005.01.086. Проігноровано невідомий параметр
|vauthors=(довідка) - Frameshift mutations of vacuolar protein sorting genes in gastric and colorectal cancers with microsatellite instability. Human Pathology 43 (1): 40–7. January 2012. PMID 21733561. doi:10.1016/j.humpath.2010.03.015. Проігноровано невідомий параметр
|vauthors=(довідка) - Microsatellite instability in colorectal cancer is associated with local lymphocyte infiltration and low frequency of distant metastases. British Journal of Cancer 92 (9): 1746–53. May 2005. PMC 2362037. PMID 15856045. doi:10.1038/sj.bjc.6602534. Проігноровано невідомий параметр
|vauthors=(довідка) - DNA mismatch repair defects and microsatellite instability status in periocular sebaceous carcinoma. American Journal of Ophthalmology 157 (3): 640–7.e1–2. March 2014. PMID 24321472. doi:10.1016/j.ajo.2013.12.002. Проігноровано невідомий параметр
|vauthors=(довідка) - Research, Center for Drug Evaluation and. Approved Drugs - FDA grants accelerated approval to pembrolizumab for first tissue/site agnostic indication. www.fda.gov (англ.). Процитовано 24 травня 2017.
- Revised Bethesda Guidelines for hereditary nonpolyposis colorectal cancer (Lynch syndrome) and microsatellite instability. Journal of the National Cancer Institute 96 (4): 261–8. February 2004. PMC 2933058. PMID 14970275. doi:10.1093/jnci/djh034. Проігноровано невідомий параметр
|vauthors=(довідка) - Gene expression variations in microsatellite stable and unstable colon cancer cells. The Journal of Surgical Research 174 (1): 1–6. May 2012. PMC 3210903. PMID 21816436. doi:10.1016/j.jss.2011.06.016. Проігноровано невідомий параметр
|vauthors=(довідка) - Dietary fat intake and risk of epithelial ovarian cancer by tumour histology. British Journal of Cancer 110 (5): 1392–401. March 2014. PMC 3950866. PMID 24473401. doi:10.1038/bjc.2014.16. Проігноровано невідомий параметр
|vauthors=(довідка)
