Нітрат амонію
Нітра́т амо́нію — неорганічна сполука складу NH4NO3, сіль нітратної кислоти. Білі гігроскопічні кристали, добре розчинні у воді; проявляє властивості окисника (при нагріванні).
| Нітрат амонію | |
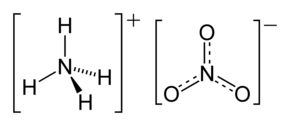 | |
 | |
| Маса | 1,3E−25 кг[1] |
|---|---|
| З матеріалу | Аміак і Нітратна кислота |
| Хімічна формула | H₄N₂O₃[1] і NH₄NO₃[2] |
| Канонічна формула SMILES | [NH4+].[N+](=O)([O-])[O-][1] |
| Температура плавлення | 169,6 °C |
| Точка кипіння | 235 °C |
| Температура розкладання | 210 °C |
| Класифікація та маркування безпеки | NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response і CLPd[3] |
| | |
Під назвою амоні́йна селі́тра широко використовується як нітрогеновмісне добриво, яке містить 34-35% нітрогену. Окрім того, нітрат амонію використовують для виготовлення вибухових речовин.
Отримання
Нітрат амонію синтезують взаємодією аміаку та нітратної кислоти:
Найпотужнішими виробниками аміачної селітри в Україні є ВАТ «Рівнеазот» (Рівне), ВАТ «Азот» (Черкаси), ВАТ «Азот» (Сєвєродонецьк) та «Концерн Стирол» (Горлівка).
Випускається у вигляді круглих гранул або голчастих чи лускоподібних кристалів білого чи жовтуватого кольору, добре розчинних у воді. Постачається насипом, у мішках по 50 кг та у біґ-беґах по 500 або 1000 кг.
Хімічні властивості
При нагріванні близько 170 °С розкладається на оксид азоту(I) та воду:
При підвищенні температури сполука розкладається із виділенням азоту та оксиду азоту(II):
Застосування
Добрива
Амонійна селітра — найпоширеніше з мінеральних добрив. На кислих ґрунтах доцільно використовувати суміш аміачної селітри з карбонатом кальцію — вапняково-аміачну селітру.
Вибухові речовини
Нітрат амонію — слабка вибухова речовина. Детонує від капсуля-детонатора лише при заряді діаметром понад 80 мм, а при меншому діаметрі — від проміжного детонатора. Використовується як складова частина промислових вибухових речовин (амонітів, амоналів). Перевагами є дешевизна, простота отримання, значна сировинна база, повний перехід у газоподібний стан під час вибуху.
Примітки
- 6484-52-2
- https://pubchem.ncbi.nlm.nih.gov/compound/22985#section=Molecular-Formula
- Ammonium nitrate
Джерела
- Українська радянська енциклопедія : у 12 т. / гол. ред. М. П. Бажан ; редкол.: О. К. Антонов та ін. — 2-ге вид. — К. : Головна редакція УРЕ, 1974–1985.
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2007. — Т. 2 : Л — Р. — 670 с. — ISBN 57740-0828-2.
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ / Р. А. Лидин. — 3-е. — М. : Химия, 2000. — 480 с. — ISBN 5-7245-1163-0. (рос.)