Оритаванцин
Оритаванцин (англ. Oritavancin) — напівсинтетичний антибіотик з групи глікопептидних антибіотиків для парентерального застосування. Він застосовується для лікування важких інфекцій шкіри, спричинених грам-позитивними бактеріями. За хімічною структурою оритаванцин є ліпоглікопептидом, подібним до ванкоміцину.[1] FDA та Європейське агентство з лікарських засобів схвалили оритаванцин для лікування інфекцій шкіри та придатків шкіри.[2][3]
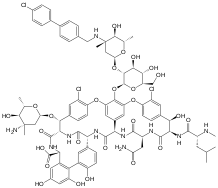 | |
| Систематична назва (IUPAC) | |
| (4R)-22-O-(3-Amino-2,3,6-trideoxy-3-C-methyl-α-L-arabinohexopyranosyl)-N3-(p-(p-chlorophenyl)benzyl)vancomycin | |
| Ідентифікатори | |
| Номер CAS | |
| Код ATC | J01 |
| PubChem | |
| DrugBank | |
| Хімічні дані | |
| Формула | C86H97Cl3N10O26 |
| Мол. маса | 1793,12 г/моль |
| SMILES | & |
| Фармакокінетичні дані | |
| Біодоступність | 100% |
| Метаболізм | не метаболізує |
| Період напіврозпаду | 245 год. |
| Виділення | нирковий, фекалії |
| Терапевтичні застереження | |
| Кат. вагітності |
? |
| Лег. статус | |
| Використання | в/в |
Історія
Оритаванцин синтезований у лабораторії компанії «Eli Lilly», яка й розпочала клінічні дослідження препарату. Подальші дослідження та маркетинг препарату проводили дочірні компанії «Eli Lilly» «InterMune» з 2001 року, а потім «Targanta Therapeutics» з кінця 2005 року.[4] У грудні 2008 року FDA відхилила заявку на схвалення оритаванцину без проведення додаткових клінічних досліджень, після чого заявку на реєстрацію оритаванцину в ЄС було відкликано.
У 2009 році «Medicines Company» придбала права на виробництво та маркетинг оритаванцину, забезпечила проведення нових клінічних досліджень препарату, та подала нову заявку на схвалення оритаванцину до FDA у лютому 2014 року.[5] 6 серпня 2014 року FDA схвалило оритаванцин для лікування інфекцій шкіри.[2]
19 березня 2015 року оритаванцин отримав схвалення для клінічного застосування на території ЄС для лікування інфекцій шкіри в дорослих.[6]
Фармакологічні властивості
Оритаванцин — напівсинтетичний антибіотик з групи глікопептидних антибіотиків. Механізм дії препарату полягає у руйнуванні стінки грампозитивних бактерій унаслідок дії на структури бактеріальної стінки 4-хлор-біфенілметильної групи.[7] Оритаванцин також порушує синтез клітинної стінки шляхом інгібування полімеризації пептидогліканів клітинної стінки та інгібування зшивання структур клітинної стінки шляхом порушення трансгліколізації та транспептидації.[8][9] За своїми антибактеріальними властивостями оритаванцин близький до інших глікопептидних антибіотиків, зокрем ванкоміцину, який натепер є основним препаратом для лікування важких інфекцій шкіри в Європі та США.[10] До препарату in vitro чутливі грампозитивні аеробні та анаеробні мікроорганізми: стафілококи (в тому числі метициллінорезистентні), стрептококи (у тому числі пневмококи), ентерококи[11][9] Clostridium difficile, Clostridium perfringens , Peptostreptococcus spp., та Propionibacterium spp.[12][13] Оритаванцин за даними клінічних досліджень є ефективнішим проти Clostridium difficile, ніж метронідазол і ванкоміцин.[14] За даними клінічних досліджень, проведених методом моделювання на лабораторних мишах, оритаванцин є ефективним проти Bacillus anthracis, збудника сибірки.[15]
Фармакокінетика
Після парентерального введення оритавацин повільно розподіляється в організмі, біодоступність складає 100 % після внутрішньовенного введення. Препарат добре (на 85 %) зв'язується з білками плазми крові. Оритаванцин не метаболізується в організмі, виділяється з організму в незміненому вигляді переважно нирками, частково з фекаліями. Період напіввиведення антибіотику становить 245 годин.[9][16]
Клінічні дослідження
У 2003 році представлені результати ключових клінічних досліджень ІІІ фази, в яких досліджувалась ефективність щоденного внутрішньовенного введення оритаванцину для лікування гострих бактеріальних інфекцій шкіри та придатків шкіри. У цих дослідженнях досягнута первинна контрольна точка, оскільки оритаванцин виявляв ефективність протягом коротшого часу, ніж препарати порівняння ванкоміцин та цефалексин. Оритаванцин мав статистично значимий кращий профіль безпеки з відносним зниженням загальної частоти побічних ефектів на 19 % у порівнянні з ванкоміцином та цефалексином у другому розширеному ключовому клінічному дослідженні.[17]
Примітки
- Domenech O, Francius G, Tulkens PM, Van Bambeke F, Dufrêne Y, Mingeot-Leclercq MP (Вересень 2009). Interactions of oritavancin, a new lipoglycopeptide derived from vancomycin, with phospholipid bilayers: Effect on membrane permeability and nanoscale lipid membrane organization. Biochimica et Biophysica Acta (BBA) - Biomembranes 1788 (9): 1832–40. PMID 19450541. doi:10.1016/j.bbamem.2009.05.003. (англ.)
- News Release (6 серпня 2014). FDA approves Orbactiv to treat skin infections. FDA. (англ.)
- Orbactiv. 17 вересня 2018. (англ.)
- Tomoko Okudaira (9 травня 2014). The Daily Biopharmaceutical News Source. BioWorld. Процитовано 6 червня 2014. (англ.)
- Biotechs pick up slack in antibiotics development. 17 травня 2011. (англ.)
- EPAR summary: Orbactiv. European Medicines Agency. 2016. (англ.)
- Belley A, McKay GA, Arhin FF, Sarmiento I, Beaulieu S, Fadhil I, Parr TR, Moeck G (Грудень 2010). Oritavancin disrupts membrane integrity of Staphylococcus aureus and vancomycin-resistant enterococci to effect rapid bacterial killing. Antimicrobial Agents and Chemotherapy 54 (12): 5369–71. PMC 2981232. PMID 20876372. doi:10.1128/AAC.00760-10. (англ.)
- Zhanel GG, Schweizer F, Karlowsky JA (Квітень 2012). Oritavancin: mechanism of action. Clinical Infectious Diseases. 54 Suppl 3: S214–9. PMID 22431851. doi:10.1093/cid/cir920. (англ.)
- Oritavancin (англ.)
- Scheinfeld N (Січень 2007). A comparison of available and investigational antibiotics for complicated skin infections and treatment-resistant Staphylococcus aureus and enterococcus. Journal of Drugs in Dermatology 6 (1): 97–103. PMID 17373167. (англ.)
- Targanta Press Release September 19, 2007 Архівовано 13 липня 2011 у Wayback Machine. (англ.)
- Mendes RE, Woosley LN, Farrell DJ, Sader HS, Jones RN (Березень 2012). Oritavancin activity against vancomycin-susceptible and vancomycin-resistant Enterococci with molecularly characterized glycopeptide resistance genes recovered from bacteremic patients, 2009-2010. Antimicrobial Agents and Chemotherapy 56 (3): 1639–42. PMC 3294904. PMID 22183169. doi:10.1128/AAC.06067-11. (англ.)
- Mendes RE, Sader HS, Flamm RK, Jones RN (Червень 2014). Activity of oritavancin tested against uncommonly isolated Gram-positive pathogens responsible for documented infections in hospitals worldwide. The Journal of Antimicrobial Chemotherapy 69 (6): 1579–81. PMID 24505091. doi:10.1093/jac/dku016. (англ.)
- Targanta Press Release September 19, 2007 Архівовано 13 липня 2011 у Wayback Machine. (англ.)
- Targanta Press Release May 24, 2007 Архівовано 13 липня 2011 у Wayback Machine. (англ.)
- Oritavancin. DrugBank (англ.)
- InterMune Press Release September 15, 2003 (англ.)