Трансферини
Трансфери́ни — група залізозв'язуючих глікопротеїнів плазми крові, які контролюють вміст вільного заліза в біологічних рідинах.[1] У людини трансферин кодується геном TF.[2]
| Трансферин | |
|---|---|
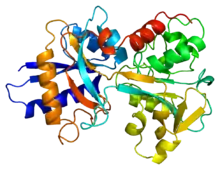 | |
| Ідентифікатори | |
| Символ | TF |
| Інші символи | PRO1557; PRO2086; TFQTL1 |
| Інші ідентифікатори | Pfam: |
| Інша інформація | |
Незважаючи на те що трансферинове залізо складає лише 0,1 % (4 мг) від загальної кількості заліза в організмі, воно утворює найбільш життєво важливий пул заліза з найшвидшою швидкістю обороту (25 мг/24 год). Трансферин має молекулярну масу близько 80 кДа, містить два сайти зв'язування для іонів Fe(III). Константа зв'язування іонів Fe(III) трансферинами є дуже високою (1020 M−1 при pH 7,4),[3] але сильно знижується при переході до кислих значень pH.
Механізм транспорту
Трансферин що несе на собі іони заліза, проникає в клітини за допомогою спеціального рецептору, що має назву транферриновий рецептор (TfR). Трансфериновий рецептор розташований на поверхні відповідних клітин, таких як, наприклад, прекурсори еритроцитів. Трансферин, приєднаний до трансферинового рецептору, інтерналізується у везикулу шляхом рецептор-опосередкованого ендоцитозу. pH у везикулі знижується завдяки йонним насосам (H+-АТФази) до значень близько 5,5, що призводить до вивільнення заліза із трансферину. Рецептор із трансферином потім транспортується назад на поверхню клітини, готовий до переносу наступних йонів.
Ген, що кодує трансферин у людини, розташований на хромосомній ділянці 3q21.[2]
Структура
Людський трансферин містить поліпептидний ланцюг що складається з 679 амінокислотних залишків та двох вуглеводних ланцюгів. До складу протеїну входять альфа-спіралі та бета-листи що утворюють два домени.[4] N- та C-термінальні послідовності представлені глобулярними ділянками, між якими розташований сайт зв'язування заліза.
Амінокислотами, які зв'язують залізо. є два тирозини, один гістидин та одна аспарагінова кислота. Для того щоб іон заліза зв'язався із сайтом, потрібен додатковий аніон, бажано карбонат (CO32−).[4]
Трансфериновий рецептор утворює гомодимер.[5] У людини кожен мономер складається з 760 амінокислот. Кожен мономер складається з трьох доменів: протеазного, спірального, та вершинного (англ. apical). Тривимірна структура трансферинового рецептору нагадує метелика.[4]
 Трансферин зв'язаний зі своїм рецептором
Трансферин зв'язаний зі своїм рецептором Трансфериновий рецептор
Трансфериновий рецептор
Розподіл в тканинах
Печінка є головним місцем синтезу трансферину, хоча він також продукується в інших тканинах та органах, включаючи головний мозок. Головною функцією трансферину є транспортування заліза від локацій його абсорбції в дванадцятипалій кишці та макрофагів крові в інші місця організму. Трансферин відіграє ключову роль у процесі формування нових еритроцитів.[5] Трансфериновий рецептор допомагає підтримувати гомеостаз заліза в клітині контролюючи транспортування трансферин-зв'язаного заліза.[5]
Роль у патогенезі
Підвищений рівень трансферину в крові асоційований з анемією та вагітністю. Знижений рівень трансферину в крові може виникати при захворюваннях, асоційованих з розбалансуванням гомеостазу заліза, а також білковій недостатності. Повна відсутність трансферину спостерігається при рідкісній генетичній хворобі — атрансферинемії, що призводить до анемії та гемосидерозу та згодом до відмови серця й інших наслідків.
Інші ефекти
Вуглеводно-дефіцитний трансферин з'являється в крові при надлишковому вживанні алкоголю.[6]
Посилання
- Crichton RR, Charloteaux-Wauters M (May 1987). Iron transport and storage. European Journal of Biochemistry / FEBS 164 (3). с. 485–506. PMID 3032619. doi:10.1111/j.1432-1033.1987.tb11155.x.
- Yang F, Lum JB, McGill JR, Moore CM, Naylor SL, van Bragt PH, Baldwin WD, Bowman BH (May 1984). Human transferrin: cDNA characterization and chromosomal localization. Proceedings of the National Academy of Sciences of the United States of America 81 (9). с. 2752–6. PMC 345148. PMID 6585826. doi:10.1073/pnas.81.9.2752.
- Aisen P, Leibman A, Zweier J (Mar 1978). Stoichiometric and site characteristics of the binding of iron to human transferrin. The Journal of Biological Chemistry 253 (6). с. 1930–7. PMID 204636.
- Transferrin Structure. St. Edward's University. 18 липня 2005. Архів оригіналу за 11 грудня 2012. Процитовано 24 квітня 2009.
- Macedo MF, de Sousa M (Mar 2008). Transferrin and the transferrin receptor: of magic bullets and other concerns. Inflammation & Allergy Drug Targets 7 (1). с. 41–52. PMID 18473900. doi:10.2174/187152808784165162. Архів оригіналу за 18 січня 2017. Процитовано 9 травня 2019.
- Sharpe PC (Nov 2001). Biochemical detection and monitoring of alcohol abuse and abstinence. Annals of Clinical Biochemistry 38 (Pt 6). с. 652–64. PMID 11732647. doi:10.1258/0004563011901064.[недоступне посилання з травня 2019]