Фенолокислоти
Фенолокислоти – похідні ароматичних вуглеводнів, у молекулах яких атоми гідрогену бензольного ядра заміщені на карбоксильні (–СООН) і гідроксильні (–ОН) групи. Їх іноді розглядають як ароматичні кислоти, в молекулах яких атом гідрогену бензольного ядра заміщений на гідроксильні групи. Фенолокислоти одночасно мають властивості карбонових кислот і фенолів. Крім того, для них характерні властивості, зумовлені наявністю в молекулі обох видів функціональних груп і бензольного ядра.
Фізичні властивості
Фенолокислоти являють собою тверді кристалічні речовини. Фенолокислоти, які мають у своєму складі один фенольний гідроксил, порівняно малорозчинні у холодній воді,однак добре розчиняються в гарячій воді та багатьох органічних розчинниках . Зі збільшенням числа фенольних гідроксилів розчинність фенолокислот збільшується.
Поширення в природі
Фенолокислоти дуже поширені у природі, тому їх можна добути з природної сировини такі як глід криваво-червоний, горобина чорноплідна, прополіс. Фенолокислоти є основним компонентом(55-85%) залишку від перегонки деревної смоли(пек деревний).
Синтез
Нерідко для добування фенолокислот користуються синтетичними способами. Зокрема, 2-оксибензойну (саліцилову) кислоту добувають з феноляту натрію і вуглекислого газу в автоклавах при 180 °С з наступною обробкою продукту реакції хлоридною кислотою (синтез Кольбе):
C6H5ONa + С02 180 С → С6Н4(ONa)COOH; С6Н4(ONa)COOH + НС1 → С6Н4(ОН)СООН + NaCl
Хімічні властивості
Фенолокислоти одночасно мають властивості карбонових кислот і фенолів. Крім того, для них характерні властивості, зумовлені наявністю в молекулі обох видів функціональних груп і бензольного ядра.
Розкладання при нагріванні
Фенолокислоти при нагріванні розкладаються з утворенням фенольних сполук та вуглекислого газу.
Наприклад, при нагріванні саліцилова кислота розкладається на фенол і вуглекислий газ:
НОС6Н4СООН → С5Н6ОН + СО2 саліцилова кислота фенол вуглекислий газ
Галова кислота при нагріванні втрачає карбоксильну групу й перетворюється на трьохатомний фенол – пірогалол.
Реакція естерифіції(за карбоксильною групою)
Фенолокислоти як і карбонові кислоти, завдяки наявності карбоксильної групи утворювати естери.
Наприклад, утворення естеру саліцилової кислоти - ацетилсаліцилової кислоти:
НОС6Н4СООН + Н3С-С(=О)-О-(О=)С-СН3 → С6Н4(СООН)-О-СО-СН3 + СН3СООН саліцилова кислота ацетатний естер ацетилсаліцилова кислота оцтова кислота
При утворенні естеру галової кислоти одна молекула галової кислоти реагує своїм карбоксилом, інша – фенільним гідроксилом.
Китайський танін є глюкозидом дигалової кислоти та глюкози.
Утворення солей
Фенолокислоти, як і карбонові кислоти утворюють солі.
Наприклад, утворення саліцилату натрію при взаємодії саліцилової кислоти та їдкого натру:
НОС6Н4СООН + NaOH → НОС6Н4COONa + Н2О саліцилова кислота саліцилат натрію
Реакція з хлоридом феруму(III) (за фенольною групою)
Нерідко виникає необхідність у виявленні наявності саліцилової кислоти та інших фенолокислот в консервованих продуктах. Тоді у пробірку поміщають 0,1– 0,3 досліджуваного розчину, додають 4-5 мл води і кілька крапель 1 % розчину хлориду феруму (III). Виникає фіолетове забарвлення. На відміну від фенолу, воно може з'явитися і в спиртовому розчині кислоти. Забарвлення виникає в результаті утворення комплексних солей при взаємодії фенольних груп шести молекул фенолокислоти з молекулою FeCl3. Саліцилова кислота легко взаємодіє з хлоридом феруму (III) і утворює продукт реакції синьо-чорного кольору (чорнило).
Реакція нуклеофільного заміщення з галогенами
Наявність у молекулі фенолокислот фенольних груп (–ОН) дає їм змогу вступати в реакції заміщення атомів гідрогену бензольного ядра на галогени за звичайних умов. Бензойна кислота та звичайні ароматичні кислоти в такі реакції не вступають.
Наприклад, бромування саліцилової кислоти:
НОС6Н4СООН + Br2 → НО(Br)С6Н3СООН + НОС6Н3(Br)СООН + 2HBr саліцилова кислота п-бромсаліцилова кислота о-бромсаліцилова кислота
Фенольна група в молекулі саліцилової кислоти діє як замісник першого роду – спрямовує атомні групи та окремі атоми на заміщення атомів гідрогену бензольного ядра в о- і п-положення відносно себе.
Типові представники фенолокислот та їх похідні, їхнє використання в медицині та промисловості
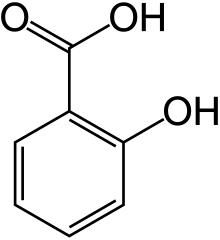
2-Оксибензойна або саліцилова кислота – типова фенолокислота, її іноді називають оксибензойною кислотою, C6H4(OH)COOH. Солі й естери саліцилової кислоти – саліцилати. Вперше була добута з естерів, що містяться в тканинах деяких рослин, – гаультерової ефірної олії Gaultheria procumbens. Саліцилова кислота – тверда кристалічна речовина. Має бактерицидну дію. Її солі та естери широко використовують у медицині й ветеринарії як лікарські препарати. Саліцилову кислоту широко використовують для виробництва лікарських засобів (наприклад, ацетилсаліцилової кислоти, фенілсаліцилату), протравних барвників, фунгіцидів (наприклад, саліциланіліду), пахучих речовин (метилсаліцилату, бензилсаліцилату), антисептиків у харчовій промисловості, при консервуванні, як реагент для колориметричного визначення в розчинах феруму й купруму, як кислотно-основний індикатор при люмінесцентному аналізі (при рН=2,5....4,6 та за наявності кислоти з'являється синя люмінесценція) тощо.
3,4,5-Триоксибензойна, або галова кислота – фенолокислота, що містить у складі своєї молекули одну карбоксильну (–СООН) і три гідроксильні (–ОН) групи. Має в'яжучий смак і є складовою частиною молекул дубильних речовин, зокрема головної з них – таніну, якого багато в корі дуба і особливо в чорнильних горішках. До складу молекули таніну галова кислота входить у вигляді дигалової кислоти, що є естером, утвореним двома молекулами галової кислоти.
Танін – аморфний порошок жовтуватого кольору, добре розчиняється у воді, сильно в'яжучий на смак. У медицині й ветеринарії його використовують як в'яжучий препарат. Він використовується також у шкіряній промисловості для дублення шкір і хутряних виробів. У хімічному аналізі його застосовують як алкалоїдний реактив.
Саліцилат натрію – кристалічна речовина,сіль саліцилової кислоти, добре розчиняється у воді й органічних розчинниках, використовується в медицині і ветеринарії як протиревматичний і жарознижувальний засіб, сировина для добування інших лікарських засобів.
Ацетилсаліцилова кислота – біла кристалічна речовина, естер саліцилової кислоти. Застосовується в медицині й ветеринарії як жарознижувальний, протизапальний, антиревматичний і антиневралгічний засіб. У тканинах організму відбувається поступовий гідроліз ацетилсаліцилової до саліцилової і ацетатної кислот, що лежить в основі механізму дії медикаменту.
Фенілсаліцилат, або салол (мусол) НОС6Н4(СО)ОС6Н5, – кристалічна речовина, похідна саліцилової кислоти. Використовується в медицині й ветеринарії як дезінфекційний засіб при лікуванні деяких кишкових захворювань, а також при суглобовому ревматизмі.
Див. також
Джерела
- Тюкавкина А. Н., Бауков Ю. И. Биоорганическая химия. — 3-е, перераб. и доп. — М. : «Дрофа», 2004. — С. ?. — ISBN 5-7107-7420-0. (рос.)
Література
- Фармацевтична хімія : [арх. 11 березня 2021] : підручник / ред. П. О. Безуглий. — Вінниця : Нова Книга, 2008. — 560 с. — ISBN 978-966-382-113-9. (С.?)
