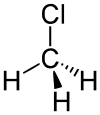
Хлорометан
Хлорметан, метил хлорид, CH3Cl — органічна речовина належить до групи галогеналканів. Вперше був отриманий французькими вченими Жаном-Батистом Андре Дюма і Еженом Пеліго в 1835 році кип'ятінням суміші метанолу, сірчаної кислоти і хлориду натрію. Аналогічний спосіб використовується і в наші дні.
| Хлорометан | |
|---|---|
 |
 |
| Назва за IUPAC | хлорметан |
| Інші назви | монохлорметан, метилхлорид, фреон 40 |
| Ідентифікатори | |
| Абревіатури | R 40, UN 1063 |
| Номер CAS | 74-87-3 |
| PubChem | 6327 |
| Номер EINECS | 200-817-4 |
| KEGG | C19446 |
| ChEBI | 36014 |
| RTECS | PA6300000 |
| SMILES |
ClC |
| InChI |
1/CH3Cl/c1-2/h1H3 |
| Номер Бельштейна | 1696839 |
| Номер Гмеліна | 24898 |
| Властивості | |
| Молекулярна формула | CH3Cl |
| Молярна маса | 50,49 г/моль |
| Зовнішній вигляд | безбарвний газ |
| Запах | слабко солодкий |
| Густина | 2,22 кг/м³ (0 °C) |
| Тпл | −97,7 °C (176 K) |
| Ткип | -24,2 °C (249 K) |
| Розчинність (вода) | 5,325 г/л |
| Тиск насиченої пари | 490 кПа (20 °C) |
| Структура | |
| Геометрія | sp³ |
| Небезпеки | |
| Класифікація ЄС | |
| R-фрази | R10, R40, Шаблон:R48/20 |
| S-фрази | S9, S16, S33 |
| NFPA 704 |
 4
2
0
|
| Температура спалаху | -46 °C |
| Температура самозаймання | 625 °C |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Фізичні властивості
Хлорметан безбарвний легко летючий прозорий газ з солодкуватим запахом. Завдяки слабкому запаху можна легко не помітити токсичної або вибухонебезпечної концентрації.
Молекулярна маса - 50,49 г/моль;
Температура плавлення -96,7 °C;
Температура кипіння -23,76 °C;
Густина — 2,31;
Тиск насиченої пари: 4 кПа (-80 °C); 53,32 кПа (-38 °C); 0,26 МПа (0 °C); 0,498 МПа (20 °C); 3,44 МПа (100 °C);
Показник заломлення: nD−23,7 1,3712;
Критична температура: tкрит 143,1 °С;
Критичний тиск ркрит 6,678 МПа.
Виробництво
Велика кількість хлорметану виробляється природно в океані дією сонячного світла на біомасу і хлору в морській піні. Проте, весь хлорметан, який використовується зараз в промисловості вироблено синтетично. Велика частина хлорметану отримана реакцією метанолу з хлороводнем, згідно з наступною хімічною реакцією
CH3OH + HCl → CH3Cl + H2O
Це може бути здійснено пропусканням хлороводню через киплячий метанол разом з хлоридом цинку як каталізатором або пропусканням суміші метанолу та хлороводню через окис алюмінію при 350 °C.
Менші кількості хлорметану виробляють нагріванням суміші метану і хлору до 400 °C. Однак, цей метод дає суміш з більш хлорованих похідних метану (дихлорметан, хлороформ, тетрахлорметан) і використовується тоді, коли необхідні ці речовини.
Застосування
Хлорметан був поширеним холодоагентом. Але таке його застосування припинили через токсичність і пожежонебезпеку. Хлорметан використовували як добавки до бензину на основі свинцю. Найважливіше використання хлорметану зараз як хімічного напівпродукту у виробництві силіконових полімерів. Менші кількості використовуються як розчинники при виробництві бутилкаучуку і очищенні бензину. Хлорметан використовується як метилюючий або хлоруючий агент в органічній хімії. Він знаходить також безліч різних застосувань: видалення жирних забруднень, слідів смол, як ракетне паливо, для отримання пінополістиролу. Як локальне знеболювальне, як інтермедіант при синтезі ліків, як носій в низькотемпературній полімеризації, як рідина для термометричного і термостатичного обладнання, як гербіцид.
Джерела
- Трегер Ю. А., Карташов Л. М., Кришталь Н. Ф., Основные хлорорганические растворители, М., 1984(рос.)