Йодометан
Йодометан (метил йодид) ― йодоорганічна сполука з класу галоненоалканів і формулою . За стандартних умов є важчою за воду леткою безбарвною рідиною з етерним запахом.[1]
| Структурна формула | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
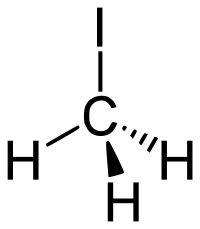 | ||||||||||||||||||||||
| Загальна інформація | ||||||||||||||||||||||
| Преференційна назва ІЮПАК | Йодометан | |||||||||||||||||||||
| Систематична назва ІЮПАК | Йодометан | |||||||||||||||||||||
| Інші назви |
Метил йодид | |||||||||||||||||||||
| Хімічна формула | CH3I | |||||||||||||||||||||
| 3D Структура (JSmol) | Інтерактивне зображення | |||||||||||||||||||||
| Зовнішні ідентифікатори / Бази даних | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Властивості | ||||||||||||||||||||||
| Молярна маса | 141,94 г/моль [1] | |||||||||||||||||||||
| Агрегатний стан |
рідина [1] | |||||||||||||||||||||
| Густина |
2,28 г/см3 (20 °C) [1] | |||||||||||||||||||||
| Температура плавлення |
-66 °C [1] | |||||||||||||||||||||
| Температура кипіння |
42 °C [1] | |||||||||||||||||||||
| Температура самозаймання |
355 °C [1] | |||||||||||||||||||||
| Розчинність |
8,66 г/л (20 °C) [1] | |||||||||||||||||||||
| Безпека | ||||||||||||||||||||||
| Маркування згідно системі УГС
Небезпека | ||||||||||||||||||||||
| H-фрази | H: H301+H331, H312, H315, H319, H335, H351, H410 | |||||||||||||||||||||
| P-фрази | P: P273, P302+P352, P304+P340, P305+P351+P338, P308+P310 | |||||||||||||||||||||
| EUH-фрази | EUH: Заходи безпеки відсутні | |||||||||||||||||||||
| LD50 |
76 мг/кг (щур, орально) [1] | |||||||||||||||||||||
| Вибухонебезпечність | ||||||||||||||||||||||
| Наскільки це можливо, значення величин подані в одиницях системи SI. Якщо не вказано іншого, усі дані відносяться до стандартного стану. | ||||||||||||||||||||||
Отримання
Отримують йодуванням метанолу йодом у присутності червоного фосфору чи реакцією диметилсульфату з калій йоидидом:[2]
Хімічні властивості
Є алкілюючим агентом, вступає у реакції нуклеофільного заміщення активніше за інших галогенметанів через порівняно малу енергію зв'язку між атомами карбону та йоду.[3] Наприклад, алкілює аміак:
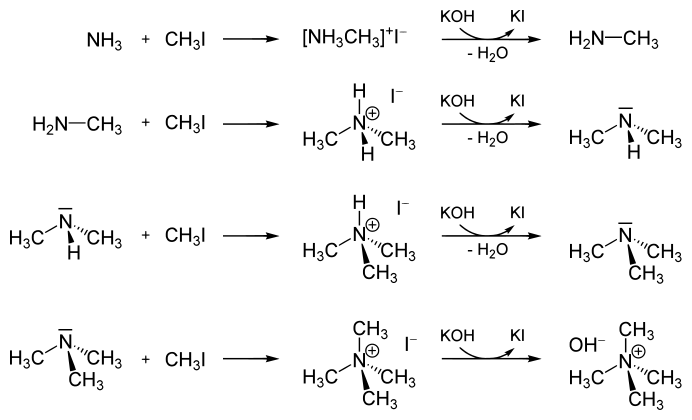
При відновленні алюмогідридом літію чи борогідридом натрію утворюється метан:[3]
Джерела
- GESTIS Substance Database. gestis-database.dguv.de. Процитовано 3 грудня 2021.
- Organic Syntheses Procedure. www.orgsyn.org (англ.). Процитовано 3 грудня 2021.
- Ластухін Ю. О., Воронов С. А. Органічна хімія. — Вид. 2-ге, перероб. і доп. — Львів : Центр Європи, 2001. — ISBN 966-7022-19-6.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.


