Реакції нуклеофільного заміщення
Реакції нуклеофільного заміщення (англ. nucleophilic substitution reactions) — фундаментальний клас реакцій в органічній хімії, природа якого полягає у взаємодії нуклеофільного реагенту з органічною сполукою типу R–X (R — алкільний або арильний залишок з позитивною електронною густиною, а X — відхідна група), в результаті чого відхідна група заміщується нуклеофілом:[1]
Якщо в якості нуклеофільного реагенту виступає розчинник, то такий тип реакції називається сольволіз. Випадки нуклеофільного заміщення також зузстрічаються в неорганічній хімії: наприклад, гідроліз хлоридів кремнію, фосфору або сірки є реакціями нуклеофільного заміщення, де в ролі нуклеофілу виступає вода.
Базову інтерпретацію, яка лежить в основі сучасного уявлення про механізми нуклеофільного заміщення, сформулювали Крістофер К. Інґольд та Едвард Д. Х'юз.[2]
Класифікація
Незважаючи на те, що в органічній хімії випадки «чистих» механізмів нуклеофільного заміщення вкрай рідкісні, принципово реакції нуклеофільного заміщення поділяються на ті, що відбуваються на sp3-гібридизованому й на sp2-гібридизованому карбонових центрах. Повну класифікацію всіх механізмів можна приблизно сформулювати наступним чином:[1]
- Нуклеофільне заміщення на насиченому атомі вуглецю:
- Реакції першого порядку (SN1).
- Реакції другого порядку (SN2).
- «Внутрішнє» нуклеофільне заміщення (SNi).
- Алільне нуклеофільне заміщення першого порядку (SN1').
- Алільне нуклеофільне заміщення другого порядку (SN2').
- Нуклеофільне заміщення на ненасиченому атомі вуглецю:
- Механізм приєднання-елімінування (також відомий як «тетраедричний механізм», SNt).
- Нуклеофільне ароматичне заміщення, що включає в себе декілька можливих механізмів.
Реакції SN1 і SN2
Ці два типи реакцій нуклеофільного заміщення є фундаментальними з точки зору теорії Інгольда і Х'юза; вони помітили, що швидкість таких реакцій іноді залежить тільки від концентрації субстрату, а іноді від концентрації як субстрату, так і нуклеофілу. В першому випадку таку реакцію було названо "заміщення, нуклеофільне, першого порядку" (англ. substitution, nucleophilic, first order, SN1), а в другому — "заміщення, нуклеофільне, другого порядку" (англ. substitution, nucleophilic, second order, SN2).[3] Також відносно SN1 і SN2 зустрічається формулювання «унімолекулярна реакція» та «бімолекулярна реакція», відповідно.[4]
В більшості випадків механізм кожної конкретної реакції лежить десь поміж SN1 і SN2; переважність одного чи іншого механізму визначається стабільністю карбокатіону, утвореного із субстрату.[4]
Кінетика й механізм реакцій SN1
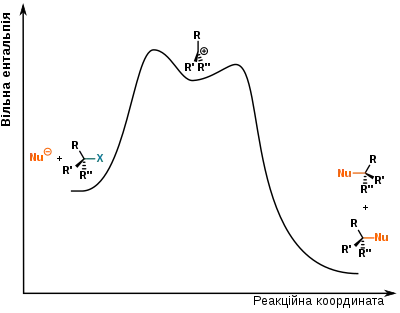
Основною рисою механізму SN1 — «іонізаційного механізму»[4] — є дисоціація субстрату з утворенням карбокатіону; цей крок є унімолекулярним і водночас лімітуючим (швидкістьвизначальним):
Карбокатіон R+ є інтермедіатом, що відзначається на енергетичному профілі реакції; Однак, через те, що карбокатіони є дуже реактивними, концентрація R+ у будь-який момент часу буде дуже низькою, що робить реакцію квазістаціонарною:
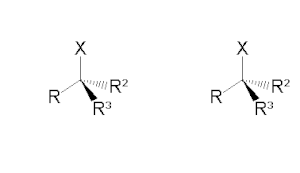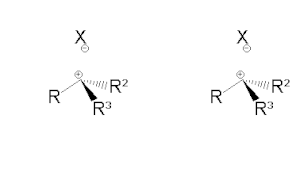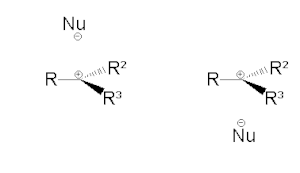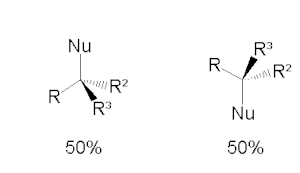
Свідченням про існування карбокатіонного інтермедіату є той факт, що у випадку заміщення на хіральних субстратах продукт являє собою повний або частковий рацемат:
Кінетика й механізм реакцій SN2
Серед простих алкільних груп, первинні алкільні групи (особливо метильна група) ніколи не реагують за механізмом SN1, а тільки за механізмом «прямого заміщення»[4] — SN2. Частково це зумовлено низькою стабільністю карбокатіонів первинних алкілів, а частково — низьким стеричним впливом водневих замісників, які не будуть завадою при нуклеофільній атаці.
Основна риса реакцій типу SN2 — відсутність карбокатіонового інтермедіату (і взагалі інтермедіату як такого). Натомість, у таких реакціях нуклеофіл атакує реактант зі сторони, що є протилежною до відхідної групи; утворення нового зв'язку між нуклеофілом та атомом вуглецю відбувається одночасно з розривом зв'язку між цим атомом та відхідною групою. Результатом заміщення SN2 на хіральному центрі є інверсія хіральної конфігурації цього центра:
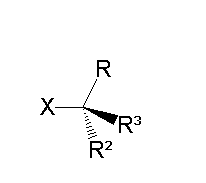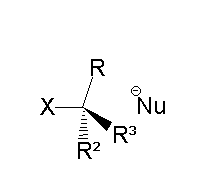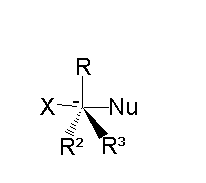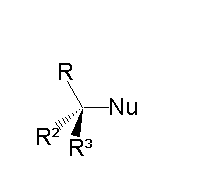
Кінетика реакцій SN2 відноситься до другого порядку. Таким чином, швидкість реакції залежить як від концентрації субстрату, так і від концентрації нуклеофілу:
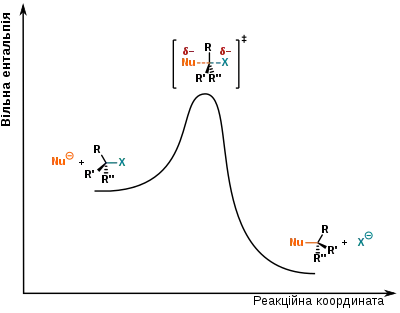
Механістичний опис реакції SN2 можливий за допомогою методу граничних орбіталей: для цього розглядають взаємодію граничної орбіталі нуклеофілу (ВЗМО) із граничною орбіталлю зв'язку C–X субстрату (відповідно, НВМО). Утворення комплексу у перехідному стані зумовлено частковим перекриттям пелюсток ВЗМО нуклеофілу й НВМО субстрату, що мають однакову фазу. Як можна побачити на схемі внизу, тилове наближення нуклеофілу (англ. backside approach) є більш вигідним, аніж фронтальне наближення (англ. frontside approach) через більшу площу перекриття пелюсток відповідних орбіталей, а також через симетричність перехідного стану:[4]

Фактори, за яких переважає механізм SN1 або SN2
Якщо молекула може вступати в реакції нуклеофільного заміщення на насиченому атомі Карбону, то можна виділити декілька загальних факторів, що визначають, за яким із двох механізмів ці реакції будуть відбуватись. Детально ці фактори будуть обговорені нижче. Так, механізм SN1 є переважним, якщо:
- Карбокатіонний інтермедіат має достатню довжину життя, що зумовлено стабілізуючими факторами (структура субстрату, розчинник);
- Концентрація нуклеофілу є низькою.
Механізм SN2 переважає, коли:
- Карбокатіонний інтермедіат не має достатньої стабілізації;
- Суттєву стабілізацію отримує перехідний стан.
Стеричні фактори
У той час, коли первинні галогеноалкани реагують виключно за механізмом SN2, третинні галогеноалкани реагують виключно за механізмом SN1. Це, насамперед, зумовлено зростанням скупченості атомів у перехідному стані SN2. Насичений атом Карбону, на якому проходить заміщення, має чотири замісники із кутом між зв'язками ~109°. У перехідному стані цей атом вже взаємодіє із (формально) п'ятьма атомами (тобто, маємо кути 3×120° і 6×90°); таким чином, чим більше замісники, тим більш енергетично невигідним є механізм SN2.
З іншого боку, механізм SN1 передбачає лише втрату галогеніду, тому замість кутів 4×109° отримуємо 3×120° — тобто, зниження скупченості.[3]
Стабілізація карбокатіону/перехідного стану
Іншим важливим фактором є стабілізація реактивних частинок протягом реакції. Якщо розглядати прості галогеноалкани, то стабільність відповідних карбокатіонів зростає в ряду 1°<2°<3° через зростаючий ефект гіперкон'югації. Однак, роль у стабілізації карбокатіону також приймають сусідні атоми кисню, азоту та ін.; таким чином, α-алкокси- й α-аміногалогеноалкани є гарними субстратами для реакцій SN1:
У той же час, α-галолгено-оксосполуки реагують виключно за механізмом SN2. Пояснити це можна за допомогою методу МО: комбінація розпушуючої орбіталі оксозв'язку π*(C=O) і розпушуючої орбіталі σ*(C–X) утворює НВМО з нижчою енергією, що є набагато більш вигідним для нуклеофільної атаки:[3]

Алільні й бензильні сполуки є гарними субстратами для реакцій SN2, тому що перехідний стан отримує певну стабілізацію через кон'югацію:
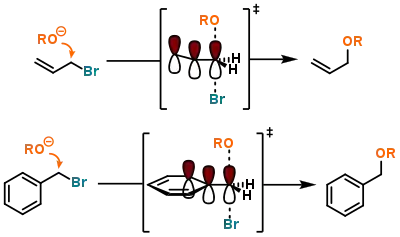
Однак, слід зауважити, що ці сполуки також можуть реагувати за механізмом SN1; для первинних аліл- або бензилгалогенідів немає ніяких підстав унеможливлювати такий перебіг реакції. Але на підвищення вірогідності того чи іншого механізму впливають інші замісники, що також знаходяться в кон'югації з тими ж ненасиченими зв'язками. Так, електронодонорні замісники в пара-положенні стабілізують бензильний карбокатіон і підвищують вірогідність механізму SN1, а електроноакцепторні замісники, навпаки, надають певну дестабілізацію, чим роблять механізм SN1 менш переважним:
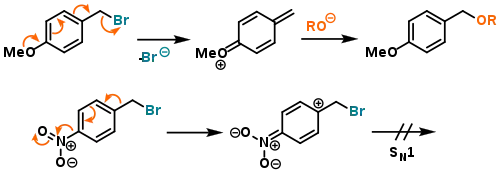
Вибір розчинника
Зазвичай, для проведення реакції SN1 обирають полярний протонний розчинник (вода, спирт або кислота); часто розчинник і є нуклеофілом. Це зумовлено тим, що утворений карбокатіонний інтермедіат разом із відхідною групою є більш полярними, аніж вихідний субстрат, тому потребують додаткової стабілізації як позитивних, так і негативних іонів.
Натомість, реакції SN2 проводять в апротонних розчинниках, які є достатньо полярними, щоб розчинити реактанти. Причина такого вибору полягає в тому, що в «чистих» реакціях SN2 велику роль відіграють розчинності як вихідних реагентів, так і продуктів. Розглянемо, наприклад, реакцію Фінкельштейна:
У цій реакції беруть участь бромоалкан (розчинний в ацетоні) та йодид натрію («жорсткий» катіон, «м'який» аніон; розчинний в ацетоні). Ацетон сольватує катіон натрію, але не може сольватизувати негативно заряджений йодид-іон, що робить останній дуже реакційноздатним. Йодид атакує бромоалкан, утворюючи перехідний комплекс, в якому густина негативного заряду стає меншою, але все одно не отримує належної стабілізації в розчиннику. Той факт, що бромід натрію (бромід є більш «жорсткий» аніон, аніж йодид) не розчиняється в ацетоні, спонукає перехідний комплекс до відщеплення броміду з утворенням цільового продукту — йодоалкану.
Підсумок
Враховуючи всі вищенаведені фактори, можна охарактеризувати основні класи галогенопохідних сполук за їхньою здатністю реагувати за механізмами SN1 і SN2:[4]
| Тип замісника | Реагує за
механізмом SN1 |
Реагує за
механізмом SN2 |
|---|---|---|
| метил | ні | дуже добре |
| первинний алкіл | ні | добре |
| вторинний алкіл | так | так |
| третинний алкіл | дуже добре | ні |
| аліл | так | добре |
| бензил | так | добре |
| α-карбоніл | ні | чудово |
| α-алкокси | чудово | добре |
| α-аміно | чудово | добре |
«Внутрішнє» нуклеофільне заміщення (SNi)
Цей механізм стосується реакцій спиртів з тіонілхлоридом; продукт цієї реакції — алкілхлорид — утворюється з утриманням хіральної конфігурації.
Алільне нуклеофільне заміщення
При проведенні реакцій нуклеофільного заміщення на алільних субстратах в умовах, що створюють перевагу для механізму SN1, спостерігається утворення двох продуктів: нормальний продукт SN1 і продукт алільного перегрупування SN1'. Причиною тому є утворення алільного катіону; за відсутності великого стеричного ефекту замісників по один з боків, нуклеофіл має приблизно однакові шанси для атаки як в положенні 1, так і в положенні 3:[1]
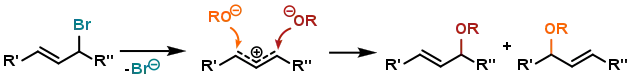
Якщо створити умови для протікання механізму SN2, то алілбромід буде давати класичний продукт реакції SN2. Однак, якщо через стеричні фактори швидкість реакції SN2 більш не є такою високою, нуклеофіл може атакувати субстрат в положенні 3 відносно відхідної групи, результуючи продукт алільного перегрупування за механізмом SN2':[5]

Нуклеофільне заміщення на ненасиченому атомі вуглецю
У випадку нуклеофільного заміщення на sp2-гібридизованому атомі вуглецю реакція в більшості випадків більше не відбувається за механізмами SN1 і SN2; натомість, подвійний зв'язок уможливлює реакції приєднання та елімінування. Таким чином, для цього типу реакцій є характерним механізм приєднання-елімінування, також відомий як тетраедричний механізм (SNt):[1]
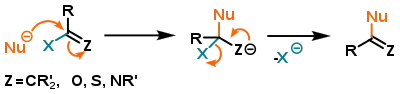
Найбільше значення цей механізм має для сполук, де атом вуглецю подвійно пов'язаний з гетероатомом, особливо якщо мова йдеться про похідні карбонових кислот. Детальніше нуклеофільне заміщення на похідних карбонових кислот («ацилювання») описане в окремій статті.
Однак, тетраедричний механізм також зустрічається серед реакцій вінілгалогенідів. Через те, що, на відміну від кисню, сірки чи азоту, вуглець (група CR'2 на схемі зверху) не може стабілізувати негативний заряд, важливим фактором є електронні властивості замісників R': так, електронодонорні групи дестабілізують карбаніонний інтермедіат, в той час як електроноакцепторні групи стабілізують його:[1][4]

В деяких випадках мезомерна стабілізація негативно зарядженого інтермедіату за рахунок електроноакцепторних груп є настільки сильною, що він не вступає спонтанно в реакцію елімінування й може мути виділений (як, наприклад, при гідролізі тетрахлорохінону):[6]
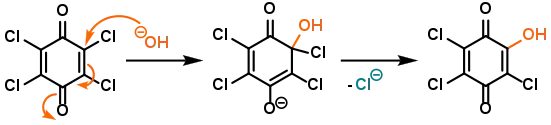
Дуже цікава реактивність спостерігається в тих випадках, коли електроноакцепторна група водночас може служити й відхідною групою: у випадку реакції вінілідендіхлориду з арилсульфідом нуклеофіл атакує позицію, що є сусідньою до хлоридних замісників.[7] Більш того, в залежності від кількості еквівалентів лугу, можна ізолювати продукт приєднання В, продукт подальшого елімінування С або ж продукт подвійного нуклеофільного заміщення Е:
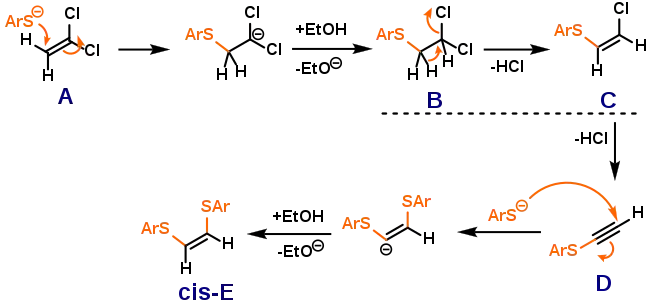
Крім того, факт отримання виключно цис-стереоізомеру Е говорить про те, що друге нуклеофільне заміщення відбувається за механізмом елімінування-приєднання.[1]
Див. також
- Нуклеофільні реагенти
- Відхідна група
- Реакція Міцунобу
- Нуклеофільне ацильне заміщення
- Нуклеофільне ароматичне заміщення
Примітки
- Smith, Michael B.; March, Jerry (27 грудня 2006). March's Advanced Organic Chemistry. Hoboken, NJ, USA: John Wiley & Sons, Inc. ISBN 978-0-470-08496-0.
- Ingold, C.K. (1969). Structure and mechanism in organic chemistry. Cornell University Press. OCLC 901922521.
- Clayden, Jonathan. (2004). Organic chemistry. Oxford University Press. ISBN 0-19-850346-6. OCLC 442120139.
- Carey, Francis A. (2013). Advanced Organic Chemistry : Part a: Structure and Mechanisms.. Springer. ISBN 978-1-4613-9795-3. OCLC 1059416763.
- Magid, Ronald M. (1 січня 1980). Nucleophilic and organometallic displacement reactions of allylic compounds: stereo-and regiochemistry. Tetrahedron (англ.) 36 (13). с. 1901–1930. ISSN 0040-4020. doi:10.1016/0040-4020(80)80203-1.
- Hancock, James W.; Morrell, Charles E.; Rhum, David (1962-01). Trichlorohydroxyquinone. Tetrahedron Letters 3 (22). с. 987–988. ISSN 0040-4039. doi:10.1016/s0040-4039(00)70943-9.
- Truce, William E.; Boudakian, Max M. (1956-06). Stereospecific Reactions of Nucleophilic Agents with Acetylenes and Vinyl-type Halides. II. The Mechanism of the Base-catalyzed Reaction of Vinylidene Chloride with Thiols. Journal of the American Chemical Society (англ.) 78 (12). с. 2748–2751. ISSN 0002-7863. doi:10.1021/ja01593a027.
