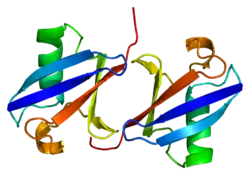
Рибосомний білок S27a
Рибосомний білок S27a (англ. Ribosomal protein S27a) – білок, який кодується геном RPS27A, розташованим у людей на короткому плечі 2-ї хромосоми. [3] Довжина поліпептидного ланцюга білка становить 156 амінокислот, а молекулярна маса — 17 965[4].
Послідовність амінокислот
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MQIFVKTLTG | KTITLEVEPS | DTIENVKAKI | QDKEGIPPDQ | QRLIFAGKQL | ||||
| EDGRTLSDYN | IQKESTLHLV | LRLRGGAKKR | KKKSYTTPKK | NKHKRKKVKL | ||||
| AVLKYYKVDE | NGKISRLRRE | CPSDECGAGV | FMASHFDRHY | CGKCCLTYCF | ||||
| NKPEDK |
Цей білок за функціями належить до рибонуклеопротеїнів, рибосомних білків. Білок має сайт для зв'язування з іонами металів, іоном цинку. Локалізований у цитоплазмі, ядрі.
Література
- Adams S.M., Sharp M.G., Walker R.A., Brammar W.J., Varley J.M. (1992). Differential expression of translation-associated genes in benign and malignant human breast tumours.. Br. J. Cancer 65: 65 — 71. PubMed DOI:10.1038/bjc.1992.12
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC).. Genome Res. 14: 2121 — 2127. 2004. PubMed DOI:10.1101/gr.2596504
- Schlesinger D.H., Goldstein G. (1975). Molecular conservation of 74 amino acid sequence of ubiquitin between cattle and man.. Nature 255: 423 — 424. PubMed DOI:10.1038/255423a0
- Huang F., Kirkpatrick D., Jiang X., Gygi S.P., Sorkin A. (2006). Differential regulation of EGF receptor internalization and degradation by multiubiquitination within the kinase domain.. Mol. Cell 21: 737 — 748. PubMed DOI:10.1016/j.molcel.2006.02.018
- Okumura F., Hatakeyama S., Matsumoto M., Kamura T., Nakayama K. (2004). Functional regulation of FEZ1 by the U-box-type ubiquitin ligase E4B contributes to neuritogenesis.. J. Biol. Chem. 279: 53533 — 53543. PubMed DOI:10.1074/jbc.M402916200
- Komander D. (2009). The emerging complexity of protein ubiquitination.. Biochem. Soc. Trans. 37: 937 — 953. PubMed DOI:10.1042/BST0370937
Примітки
- Human PubMed Reference:.
- Mouse PubMed Reference:.
- HUGO Gene Nomenclature Commitee, HGNC:10417 (англ.). Процитовано 27 лютого 2017.
- UniProt, P62979 (англ.). Процитовано 27 лютого 2017.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.