Телапревір
Телапревір — синтетичний противірусний препарат з групи інгібіторів протеази для прийому всередину. Телапревір розроблений сумісно у співпраці компаній «Vertex Pharmaceuticals» і «Johnson & Johnson».
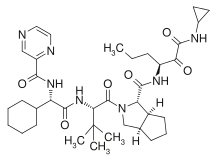 | |
| Систематична назва (IUPAC) | |
| (1S,3aR,6aS)-2-[(2S)-2-[[(2S)-2-Cyclohexyl-2-(pyrazine-2-carbonylamino)acetyl]amino]-3,3-dimethylbutanoyl]-N-[(3S)-1-(cyclopropylamino)-1,2-dioxohexan-3-yl]-3,3a,4,5,6,6a-hexahydro-1H-cyclopenta[c]pyrrole-1-carboxamide | |
| Ідентифікатори | |
| Номер CAS | |
| Код ATC | J05 |
| PubChem | |
| Хімічні дані | |
| Формула | C36H53N7O6 |
| Мол. маса | 679,85 г/моль |
| Фармакокінетичні дані | |
| Біодоступність | ~100% |
| Метаболізм | гепатичний |
| Період напіврозпаду | 9-11 год. |
| Виділення | фекалії,нирковий |
| Терапевтичні застереження | |
| Кат. вагітності |
B(США) |
| Лег. статус | |
| Використання | перорально |
Фармакологічні властивості
Телапревір — синтетичний противірусний препарат з групи інгібіторів протеази. Механізм дії препарату полягає у інгібуванні активного центру ферменту вірусу гепатиту С — протеази шляхом зв'язування з активним серином ферменту за допомогою функціональної групи α-кетоаміду, що приводить до гальмування реплікації вірусу в уражених клітинах. У травні 2011 року телапревір схвалений FDA для лікування хронічного вірусного гепатиту С 1-го генотипу в складі комбінованої терапії.[1] У 2011 році препарат був схвалений для лікування хронічного вірусного гепатиту С в Європі.[2] У березні 2014 року телапревір зареєстрований в Україні.
Фармакокінетика
Телапревір при прийомі всередину відносно повільно всмоктується, максимальна концентрація в крові досягається протягом 4—5 годин, після прийому жирної їжі всмоктування препарату покращується. Біодоступність телапревіру досліджена погано, імовірно може становити 100%. Телапревір добре зв'язується з білками плазми крові. Невідомо, чи препарат проникає через гематоенцефалічний бар'єр. Телапревір проникає через плацентарний бар'єр. Невідомо, чи препарат виділяється в грудне молоко. Препарат метаболізується в печінці, виводиться з організму переважно з калом (82%) у вигляді неактивних метаболітів, виводиться з організму частково нирками (1%). Період напіввиведення телапревіру складає при тривалому прийомі 9—11 годин, цей час може змінюватися при печінковій та нирковій недостатності.
Показання до застосування
Телапревір застосовується при лікуванні хронічного вірусного гепатиту С 1-го типу в комбінації з рибавірином та пегільованим альфа-інтерфероном у дорослих хворих без ознак печінкової недостатності.
Побічна дія
При застосуванні телапревіру можуть спостерігатись наступні побічні ефекти:
- З боку шкірних покривів — дуже часто (більше 10%) висипання на шкірі, свербіж шкіри; часто (1—10%) набряк обличчя, екзема, дерматит; нечасто (0,1—1%) кропив'янка; рідко (0,01—0,1%) синдром Стівенса-Джонсона, синдром Лаєлла.
- З боку травної системи — дуже часто (більше 10%) нудота, блювання, діарея, геморой, прокталгія; часто кандидоз ротової порожнини, анальний свербіж, ректальні кровотечі, анальна тріщина; нечасто (0,1—1%) проктит.
- З боку нервової системи — часто (1—10%) дисгевзія, втрати свідомості; нечасто (0,1—1%) ретинопатія.
- Інші побічні ефекти — часто (1—10%)гіпотиреоз; нечасто (0,1—1%) подагра.
- Зміни в лабораторних аналізах — дуже часто (більше 10%) анемія; часто (1—10%) лейкопенія, нейтропенія, тромбоцитопенія, лімфопенія, гіперурикемія, гіпертригліцеридемія, гіпокаліємія, підвищення рівня білірубіну в крові, підвищення рівня креатиніну в крові.
Протипоказання
Телапревір протипоказаний при підвищеній чутливості до препарату. Телапревір не застосовують при вагітності, годуванні грудьми та у віці менше 18 років та більше 65 років. Препарат не застосовується разом із астемізолом, цизапридом, терфенадином, мідазоламом, пімозидом, бепридилом, аміодароном, алкалоїдами ріжків, пропафеноном, рифампіцином, симвастатином, силденафілом, алфузозином, ловастатином, карбамазепіном, препаратами звіробою. З обережністю препарат застосовується при подовженні інтервалу QT на ЕКГ.
Форми випуску
Телапревір випускається у вигляді таблеток по 0,375 г.
Примітки
- FDA Approves Telaprevir for HCV. 23 травня 2011. Архів оригіналу за 15 лютого 2013. Процитовано 22 травня 2014. (англ.)
- http://verticalfund.org/uk/u-ieuropi-shvaleno-preparat-insivo-dlya-likuvannya-gepatitu-c
