ФДЕ5 інгібітори
Інгібітор фосфодіестерази — це препарат, який блокує один або більше з п'яти підтипів ферменту фосфодіестерази (ФДЕ), тим самим запобігаючи інактивації внутрішньоклітинних вторинних посередників, циклічного аденозинмонофосфату (цАМФ) і циклічного гуанозинмонофосфату (цГМФ) ФДЕ підтип(и). Повсюдна присутність цього ферменту означає, що неспецифічні інгібітори мають широкий спектр дії, причому дії на серце та легені одними з перших знайшли терапевтичне застосування.

Історія
Різні форми або підтипи фосфодіестерази спочатку були виділені з мозку щурів на початку 1970-х років[1][2] і незабаром було показано, що вони вибірково пригнічуються в мозку та інших тканинах різними препаратами.[3][4] Потенціал селективних інгібіторів фосфодіестерази як терапевтичних засобів був передбачений ще в 1977 році Вайсом і Хейтом.[5] Тим часом це передбачення виявилося вірним у різних сферах.
Класифікація
Неселективні інгібітори ФДЕ
Метиловані Ксантини та похідні:[6]
- кофеїн, незначний стимулятор
- амінофілін(Aminophylline)
- ІБМК (3-ізобутил-1-метилксантин), використовуваний як інструмент дослідження у фармакологічних дослідженнях
- Параксантин
- пентоксифілін, препарат, який має потенціал для посилення кровообігу і може мати застосування при лікуванні цукрового діабету, фіброзних розладів, ураження периферичних нервів та мікросудинних ушкоджень[7]
- теобромін
- теофілін, бронходилататор
Метильовані ксантини чинять подвійну дію, як:
- конкурентоспроможні неселективні інгібітори фосфодіестерази[6] які підвищують внутрішньоклітинний цАМФ, активують ПКА (PKA — Protein kinase A), пригнічують синтез TNF-альфа[7][8] і лейкотрієнів[9], а також зменшують запалення та вроджений імунітет[9] та
- неселективні антагоністи аденозинових рецепторів[10]
Але різні аналоги демонструють різну дію на численних підтипах, і широкий спектр синтетичних похідних ксантину (деякі неметильовані) були розроблені для пошуку сполук з більшою селективністю щодо ферменту фосфодіестерази або підтипів рецепторів аденозину.[11][12][13][14][15][16][17][18][19][20][21]
Селективні інгібітори ФДЕ2
- EHNA (erythro-9-(2-hydroxy-3-nonyl)adenine)
- BAY 60-7550 (2-[(3,4-dimethoxyphenyl)methyl]-7-[(1R)-1-hydroxyethyl]-4-phenylbutyl]-5-methyl-imidazo[5,1-f][1,2,4]triazin-4(1H)-one)
- Оксиндол
- ПДП (PDP) (9-(6-Phenyl-2-oxohex-3-yl)-2-(3,4-dimethoxybenzyl)-purin-6-one)
Селективні інгібітори ФДЕ3
- Інамринон, мілринон та еноксимон використовуються клінічно для короткочасного лікування серцевої недостатності. Ці препарати імітують симпатичну стимуляцію і збільшують серцевий викид.
- Анагрелід[22]
- Цилостазол використовується для лікування переміжної кульгавості.
- Пімобендан схвалений FDA для ветеринарного застосування для лікування серцевої недостатності у тварин.
ФДЕ3 іноді називають фосфодіестераза, інгібована цГМФ.
Селективні інгібітори ФДЕ4
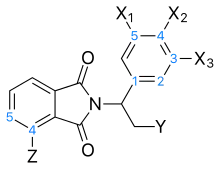
- Месембренон, алкалоїд з трави Sceletium tortuosum
- Роліпрам, що використовується як дослідний засіб у фармакологічних дослідженнях
- Ібуділаст, нейропротекторний і бронхолітичний препарат, що використовується в основному для лікування астми та інсульту. Він найбільшою мірою пригнічує ФДЕ4, але також демонструє значне пригнічення інших підтипів ФДЕ, тому діє як селективний інгібітор ФДЕ4 або неселективний інгібітор фосфодіестерази, залежно від дози.
- Пікламіласт, більш потужний інгібітор, ніж ролипрам.[23]
- Лютеолін, добавка, отримана з арахісу, яка також володіє властивостями IGF-1.[24]
- Дротаверин, що використовується для полегшення болю при нирковій коліці, а також для прискорення розширення шийки матки під час пологів
- Рофлуміласт, показаний людям із тяжкою ХОЗЛ для запобігання погіршення таких симптомів, як кашель та надлишок слизу[25]
- Апреміласт, використовується для лікування псоріазу та псоріатичного артриту.
- Crisaborole, використовується для лікування атопічного дерматиту.
ФДЕ4 є основним ферментом, що метаболізує цАМФ, який міститься в клітинах запалення та імунітету. Інгібітори ФДЕ4 мають доведений потенціал як протизапальні препарати, особливо при запальних легеневих захворюваннях, таких як астма, ХОЗЛ та риніт. Вони пригнічують вивільнення цитокінів та інших запальних сигналів, а також пригнічують вироблення активних форм кисню. Інгібітори ФДЕ4 можуть мати антидепресивну дію[26] а також нещодавно були запропоновані для використання як антипсихотичні засоби.[27][28]
26 жовтня 2009 року Університет Пенсільванії повідомив, що дослідники з їхньої установи виявили зв'язок між підвищеним рівнем ФДЕ4 (і, отже, зниженим рівнем цАМФ) у мишей, позбавлених сну. Лікування інгібітором ФДЕ4 підвищувало дефіцитний рівень цАМФ і відновило деякі функції пам'яті на основі гіпокампу.[29]
Селективні інгібітори ФДЕ5
- Силденафіл, тадалафіл, варденафіл, а також новіші уденафіл і аванафіл селективно інгібують ФДЕ5, який є цГМФ-специфічним і відповідає за деградацію цГМФ в кавернозному тілі . Ці інгібітори фосфодіестерази використовуються в основному як засоби для лікування еректильної дисфункції, а також для деяких інших медичних застосувань, таких як лікування легеневої гіпертензії .
- Дипіридамол також інгібує ФДЕ5. Це дає додаткову користь при одночасному застосуванні з NO або статинами.
Селективні інгібітори ФДЕ7
Недавні дослідження показали, хіназолін інгібітор типу ФДЕ7, чинить сильну протизапальну і нейрозахисну дії.[30]
Селективні інгібітори ФДЕ9
Параксантин, основний метаболіт кофеїну (84 % у людей),[31] є ще одним цГМФ-специфічним інгібітором фосфодіестерази, який інгібує ФДЕ9, цГМФ, який віддає перевагу фосфодіестеразі.[32][33] ФДЕ9 експресується так само високо, як ФДЕ5 в кавернозному тілі.[34]
Селективні інгібітори ФДЕ10
Повідомляється, що папаверин, алкалоїд опію, діє як інгібітор ФДЕ10.[35][36] ФДЕ10А майже виключно експресується в смугастому тілі, а подальше збільшення цАМФ і цГМФ після інгібування ФДЕ10А (наприклад, папаверином) є «новим терапевтичним шляхом у відкритті антипсихотичних засобів».[37]
Примітки
- Thompson WJ, Appleman MM (1971). Multiple cyclic nucleotide phosphodiesterase activities from rat brain. Biochemistry 10 (2): 311–6. PMID 4321663. doi:10.1021/bi00778a018.
- Uzunov P.; Weiss B. (1972). Separation of multiple molecular forms of cyclic adenosine 3',5'-monophosphate phosphodiesterase in rat cerebellum by polyacrylamide gel electrophoresis. Biochim. Biophys. Acta 284 (1): 220–226. PMID 4342220. doi:10.1016/0005-2744(72)90060-5.
- Weiss B (1975). Differential activation and inhibition of the multiple forms of cyclic nucleotide phosphodiesterase. Adv. Cycl. Nucl. Res. 5: 195–211. PMID 165666.
- Fertel R, Weiss B (1976). Properties and drug responsiveness of cyclic nucleotide phosphodiesterases of rat lung. Mol. Pharmacol. 12 (4): 678–687. PMID 183099.
- Weiss B.; Hait W.N. (1977). Selective cyclic nucleotide phosphodiesterase inhibitors as potential therapeutic agents. Annu. Rev. Pharmacol. Toxicol. 17: 441–477. PMID 17360. doi:10.1146/annurev.pa.17.040177.002301.
- Essayan DM. (2001). Cyclic nucleotide phosphodiesterases.. The Journal of Allergy and Clinical Immunology 108 (5): 671–80. PMID 11692087. doi:10.1067/mai.2001.119555.
- Deree J, Martins JO, Melbostad H, Loomis WH, Coimbra R (2008). Insights into the Regulation of TNF-α Production in Human Mononuclear Cells: The Effects of Non-Specific Phosphodiesterase Inhibition. Clinics (Sao Paulo) 63 (3): 321–8. PMC 2664230. PMID 18568240. doi:10.1590/S1807-59322008000300006.
- Marques LJ, Zheng L, Poulakis N, Guzman J, Costabel U (February 1999). Pentoxifylline inhibits TNF-alpha production from human alveolar macrophages. Am. J. Respir. Crit. Care Med. 159 (2): 508–11. PMID 9927365. doi:10.1164/ajrccm.159.2.9804085.
- Peters-Golden M, Canetti C, Mancuso P, Coffey MJ (2005). Leukotrienes: underappreciated mediators of innate immune responses. Journal of Immunology 174 (2): 589–94. PMID 15634873. doi:10.4049/jimmunol.174.2.589.
- Daly JW, Jacobson KA, Ukena D (1987). Adenosine receptors: development of selective agonists and antagonists. Prog Clin Biol Res 230 (1): 41–63. PMID 3588607.
- MacCorquodale, DW (July 1929). The Synthesis of Some Alkylxanthines1,2. Journal of the American Chemical Society 51 (7): 2245–2251. doi:10.1021/ja01382a042.
- Daly JW, Padgett WL, Shamim MT (July 1986). Analogues of caffeine and theophylline: effect of structural alterations on affinity at adenosine receptors. Journal of Medicinal Chemistry 29 (7): 1305–8. PMID 3806581. doi:10.1021/jm00157a035.
- Daly JW, Jacobson KA, Ukena D (1987). Adenosine receptors: development of selective agonists and antagonists. Progress in Clinical and Biological Research 230: 41–63. PMID 3588607.
- Choi OH, Shamim MT, Padgett WL, Daly JW (1988). Caffeine and theophylline analogues: correlation of behavioral effects with activity as adenosine receptor antagonists and as phosphodiesterase inhibitors. Life Sciences 43 (5): 387–98. PMID 2456442. doi:10.1016/0024-3205(88)90517-6.
- Shamim MT, Ukena D, Padgett WL, Daly JW (June 1989). Effects of 8-phenyl and 8-cycloalkyl substituents on the activity of mono-, di-, and trisubstituted alkylxanthines with substitution at the 1-, 3-, and 7-positions. Journal of Medicinal Chemistry 32 (6): 1231–7. PMID 2724296. doi:10.1021/jm00126a014.
- Daly JW, Hide I, Müller CE, Shamim M (1991). Caffeine analogs: structure-activity relationships at adenosine receptors. Pharmacology 42 (6): 309–21. PMID 1658821. doi:10.1159/000138813.
- Ukena D, Schudt C, Sybrecht GW (February 1993). Adenosine receptor-blocking xanthines as inhibitors of phosphodiesterase isozymes. Biochemical Pharmacology 45 (4): 847–51. PMID 7680859. doi:10.1016/0006-2952(93)90168-V.
- Daly JW (July 2000). Alkylxanthines as research tools. Journal of the Autonomic Nervous System 81 (1–3): 44–52. PMID 10869699. doi:10.1016/S0165-1838(00)00110-7.
- Daly JW (August 2007). Caffeine analogs: biomedical impact. Cellular and Molecular Life Sciences 64 (16): 2153–69. PMID 17514358. doi:10.1007/s00018-007-7051-9.
- González MP, Terán C, Teijeira M (May 2008). Search for new antagonist ligands for adenosine receptors from QSAR point of view. How close are we?. Medicinal Research Reviews 28 (3): 329–71. PMID 17668454. doi:10.1002/med.20108.
- Baraldi PG, Tabrizi MA, Gessi S, Borea PA (January 2008). Adenosine receptor antagonists: translating medicinal chemistry and pharmacology into clinical utility. Chemical Reviews 108 (1): 238–63. PMID 18181659. doi:10.1021/cr0682195.
- Lim YH, Lee YY, Kim JH, Shin J, Lee JU, Kim KS, Kim SK, Kim JH, Lim HK (2010). Development of acute myocardial infarction in a young female patient with essential thrombocythemia treated with anagrelide: a case report. Korean J Hematol 45 (2): 136–8. PMC 2983030. PMID 21120194. doi:10.5045/kjh.2010.45.2.136.
- de Visser YP, Walther FJ, Laghmani EH, van Wijngaarden S, Nieuwland K, Wagenaar GT (2008). Phosphodiesterase-4 inhibition attenuates pulmonary inflammation in neonatal lung injury. Eur Respir J 31 (3): 633–644. PMID 18094015. doi:10.1183/09031936.00071307.
- Yu MC, Chen JH, Lai CY, Han CY, Ko WC (2009). Luteolin, a non-selective competitive inhibitor of phosphodiesterases 1–5, displaced [(3)H]-rolipram from high-affinity rolipram binding sites and reversed xylazine/ketamine-induced anesthesia. Eur J Pharmacol 627 (1–3): 269–75. PMID 19853596. doi:10.1016/j.ejphar.2009.10.031.
- Powered by Skipta technology, PharmacistSociety.com is the social network for verified Pharmacists to communicate and collaborate.. pharmacistsociety.skipta.com. Архів оригіналу за 19 квітня 2012. Процитовано 1 травня 2018.
- Bobon D, Breulet M, Gerard-Vandenhove MA, Guiot-Goffioul F, Plomteux G, Sastre-y-Hernandez M, Schratzer M, Troisfontaines B, von Frenckell R, Wachtel H (1988). Is phosphodiesterase inhibition a new mechanism of antidepressant action? A double blind double-dummy study between rolipram and desipramine in hospitalized major and/or endogenous depressives. Eur Arch Psychiatry Neurol Sci 238 (1): 2–6. PMID 3063534. doi:10.1007/BF00381071.
- Maxwell CR, Kanes SJ, Abel T, Siegel SJ (2004). Phosphodiesterase inhibitors: a novel mechanism for receptor-independent antipsychotic medications. Neuroscience 129 (1): 101–7. PMID 15489033. doi:10.1016/j.neuroscience.2004.07.038.
- Kanes SJ, Tokarczyk J, Siegel SJ, Bilker W, Abel T, Kelly MP (2006). Rolipram: A specific phosphodiesterase 4 inhibitor with potential antipsychotic activity. Neuroscience 144 (1): 239–46. PMC 3313447. PMID 17081698. doi:10.1016/j.neuroscience.2006.09.026.
- Vecsey CG, Baillie GS, Jaganath D, Havekes R, Daniels A, Wimmer M, Huang T, Brown KM, Li XY, Descalzi G, Kim SS, Chen T, Shang YZ, Zhuo M, Houslay MD, Abel T (2009). Sleep deprivation impairs cAMP signaling in the hippocampus. Nature 461 (7267): 1122–1125. Bibcode:2009Natur.461.1122V. PMC 2783639. PMID 19847264. doi:10.1038/nature08488.
- Redondo, M.; Zarruk, JG.; Ceballos, P.; Pérez, DI.; Pérez, C.; Perez-Castillo, A.; Moro, MA.; Brea, J. та ін. (Jan 2012). Neuroprotective efficacy of quinazoline type phosphodiesterase 7 inhibitors in cellular cultures and experimental stroke model. Eur J Med Chem 47 (1): 175–85. PMID 22100138. doi:10.1016/j.ejmech.2011.10.040.
- Guerreiro, Serge; Toulorge, Damien; Hirsch, Etienne; Marien, Marc; Sokoloff, Pierre; Michel, Patrick P. (October 2008). Paraxanthine, the primary metabolite of caffeine, provides protection against dopaminergic cell death via stimulation of ryanodine receptor channels. Molecular Pharmacology 74 (4): 980–989. ISSN 1521-0111. PMID 18621927. doi:10.1124/mol.108.048207.
- Paraxanthine.
- Orrú, Marco; Guitart, Xavier; Karcz-Kubicha, Marzena; Solinas, Marcello; Justinova, Zuzana; Barodia, Sandeep Kumar; Zanoveli, Janaina; Cortes, Antoni та ін. (April 2013). Psychostimulant pharmacological profile of paraxanthine, the main metabolite of caffeine in humans. Neuropharmacology 67C: 476–484. ISSN 0028-3908. PMC 3562388. PMID 23261866. doi:10.1016/j.neuropharm.2012.11.029.
- da Silva, F H; Pereira, M N; Franco-Penteado, C F; De Nucci, G; Antunes, E; Claudino, M A (March 2013). Phosphodiesterase-9 (PDE9) inhibition with BAY 73-6691 increases corpus cavernosum relaxations mediated by nitric oxide–cyclic GMP pathway in mice. International Journal of Impotence Research 25 (2): 69–73. ISSN 0955-9930. PMID 23034509. doi:10.1038/ijir.2012.35.
- Weber M, Breier M, Ko D, Thangaraj N, Marzan DE, Swerdlow NR (May 2009). Evaluating the antipsychotic profile of the preferential PDE10A inhibitor, papaverine. Psychopharmacology 203 (4): 723–35. PMC 2748940. PMID 19066855. doi:10.1007/s00213-008-1419-x.
- Pöch, G.; Kukovetz, W.R. (1971). Papaverine - induced inhibition of phosphodiesterase activity in various mammalian tissues. Life Sciences 10 (3): 133–144. PMID 4325052. doi:10.1016/0024-3205(71)90086-5.
- Effects of phosphodiesterase 10 inhibition on striatal cyclic AMP and peripheral physiology in rats; An Torremans, Abdellah Ahnaou, An Van Hemelrijck, Roel Straetemans, Helena Geys, Greet Vanhoof, Theo F. Meert, and Wilhelmus H. Drinkenburg; Archived copy. Архів оригіналу за 7 жовтня 2011. Процитовано 27 серпня 2011.
Література
- Al-Kuraishy HM, Al-Gareeb AI, Al-Nami MS. Vinpocetine improves oxidative stress and pro-inflammatory mediators in acute kidney injury. International journal of preventive medicine. 2019;10.