α-кетоглутарова кислота
α-Кетоглутарова кислота – хімічна органічна сполука, одне з двох можливих кето-похідних глутарової кислоти. Коли вживається загальна назва «кетоглутарова кислота», майже завжди мається на увазі альфа-похідне. β-Кетоглутарова кислота відрізняється від альфа-ізомеру положенням карбонільної функціональної групи і є значно менш поширеною.
| α-Кетоглутарова кислота | |
|---|---|
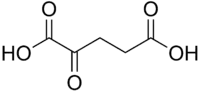 | |
| Систематична назва | 2-оксопентандіоієва кислота |
| Інші назви | 2-кетоглутарова кислота, 2-оксоглутарова кислота |
| Ідентифікатори | |
| Номер CAS | 328-50-7 |
| Номер EINECS | 206-330-3 |
| DrugBank | 08845 |
| KEGG | C00026 |
| ChEBI | 30915 |
| SMILES |
O=C(O)C(=O)CCC(=O)O |
| InChI |
InChI=1S/C5H6O5/c6-3(5(9)10)1-2-4(7)8/h1-2H2,(H,7,8)(H,9,10) |
| Номер Бельштейна | 1705689 |
| Номер Гмеліна | 602480 |
| Властивості | |
| Молекулярна формула | C5H6O5 |
| Молярна маса | 146,1 г/моль |
| Зовнішній вигляд | білі кристали |
| Тпл | 115 °C |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Аніон α-кетоглутарової кислоти, що має назву α-кетоглутарат (α-KG, або також оксо-глутарат), відіграє важливу роль у живих організмах. Він є кетокислотою, що утворюється в результаті дезамінування глутамату. Він також є одним з інтермедіатів циклу трикарбонових кислот.
Біологічна роль
Цикл трикарбонових кислот
α-Кетоглутарат є ключовою проміжною сполукою в циклі трикарбонових кислот. Він розташований після ізоцитрату і передує сукциніл-CoA. Анаперотичні реакції можуть підживлювати цикл в цьому місці шляхом синтезу α-кетоглутарату через трансамінування глутамату або через дію глутаматдегідрогенази на глутамат.
Біосинтез амінокислот
Глутамін біосинтезується з глутамату глутамінсинтазою, яка використовує АТФ для перетворення глутамату на глутамілфосфат; цей інтермедіат зазнає нуклеофільної атаки іоном амонію, в результаті чого утворюється глутамін та неорганічний фосфат.
Транспорт азоту
Кетоглутарова кислота також бере участь у метаболізмі азоту. Вона реагує з азотвісними сполуками, що утворюються в клітині, запобігаючи таким чином перенасичення клітин цими сполуками.
α-Кетоглутарат є одним з найважливіших транспортерів азоту в метаболічних шляхах. Аміносполуки приєднуються до нього (шляхом переамінування) та транспортуються в печінку, де вступають в цикл сечовини.
α-Кетоглутарат трансамінується із утворенням збуджуючого нейромедіатора глутамату. Глутамат в свою чергу може бути декарбоксильований (у присутності вітаміну B6) до іншого нейромедіатора — ГАМК.
Відомо що надлишкове утворення амонію та інших похідних азоту спостерігається при вживанні в їжу великої кількості протеїнів, синдромі Рея, цирозі печінки, а також при порушеннях в циклі сечовини.
Кетоглутарова кислота є важливою для детоксифікації амонію, зокрема в головному мозку.[1][2][3]
Косубстрат окиснення
Виступаючи як косубстрат, кетоглутарат бере участь у реакціях окиснення молекулярним киснем.
Молекулярний кисень (O2) окиснює багато речовин в організмі в реакціях, що каталізуються оксигеназами. В багатьох реакціях α-кетоглутарат допомагає процесу як косубстрат, тобто така сполука, що також зазнає окиснення.
Прикладом такої реакції є окиснення проліну до гідроксипроліну, що є необхідним для утворення колагену.
Антиоксидант
α-Кетоглутарат знижує рівень перекису водню в культурі клітин.[4]
Шляхи біосинтезу
- Окиснювальне декарбоксилювання ізоцитрату ізоцитрат-дегідрогеназою;
- окиснювальне дезамінування глутамінової кислоти глутамат дегідрогеназою.
- з галатуронової ксилоти в Agrobacterium tumefaciens.[5]
Посилання
- Does infectious fever relieve autistic behavior by releasing glutamine from skeletal muscles as provisional fuel?. Архів оригіналу за 19 травня 2014. Процитовано 29 червня 2016.
- Ott, P; Clemmesen, O; Larsen, FS (Jul 2005). Cerebral metabolic disturbances in the brain during acute liver failure: from hyperammonemia to energy failure and proteolysis.. Neurochemistry international 47 (1-2): 13–8. PMID 15921824. doi:10.1016/j.neuint.2005.04.002.
- Hares, P; James, IM; Pearson, RM (May–Jun 1978). Effect of ornithine alpha ketoglutarate (OAKG) on the response of brain metabolism to hypoxia in the dog.. Stroke; a journal of cerebral circulation 9 (3): 222–4. PMID 644619. doi:10.1161/01.STR.9.3.222.
- Long, L; Halliwell, B (2011). Artefacts in cell culture: α-Ketoglutarate can scavenge hydrogen peroxide generated by ascorbate and epigallocatechin gallate in cell culture media.. Biochemical and Biophysical Research Communications 406 (1): 20–24. doi:10.1016/j.bbrc.2011.01.091.
- Richard, Peter; Hilditch, Satu (2009). d-Galacturonic acid catabolism in microorganisms and its biotechnological relevance. Applied Microbiology and Biotechnology 82 (4): 597–604. ISSN 0175-7598. doi:10.1007/s00253-009-1870-6.
