Електрокінетична гідроенергетика
Електрокінетична гідроенергетика (англ. electrokinetic hydropower) – наука та галузь, частина молекулярної гідроенергетики, яка вивчає й використовує електрокінетичні явища в рідинних дисперсних системах з метою вироблення, накопичення, транспортування та розподілу електричної енергії.

У основі електрокінетичної гідроенергетики лежать атомно-молекулярний та йонно-молекулярний (йонно-дисперсний) принципи побудови речовини. Перший принцип характеризує дискретність або перервність будови речовини, другий принцип розкриває стан електролітичних розчинів та взаємодію йонів з молекулами розчинника.
Ключовими поняттями та об'єктами досліджень електрокінетичної гідроенергетики є дисперсні системи, електролітичні розчини, електрокінетичні явища, електрокінетичні технології (способи) та системи (засоби) перетворення потенціальної та кінетичної енергії молекул, атомів, йонів, інших малих частинок речовини в електричну енергію. Як джерела відновлюваної енергії використовуються, в першу чергу, природні середовища, зокрема, гідросфера та процеси, що у ній протікають, а також сили, які супроводжують ці процеси.
Пориста структура, яка керує розподілом зарядів в електрокінетичному процесі формування потенціалу течії, має, в ідеальному випадку, володіти всіма атрибутами міжфазної поверхні, в тому числі, потенціалом Гіббза та здатністю створювати електроосмотичний потік та подвійний електричний шар належної якості. Тож, пори повинні мати усталені розміри та форму, володіти гідроадгезійними властивостями поверхні, які б відповідали молекулярній гідродинаміці процесів. Унікальні подвійні електричні шари утворюються, зокрема, регулярними пористими структурами.
На схемі використані позначення: потік рідинного електроліту FL; CS – капілярна структура; S – тверде тіло; DL – подвійний електричний шар (ПЕШ). ПЕШ на кордоні фаз «тверде тіло – рідина» складається з двох груп йонів. Одна група, в даному випадку, позитивних йонів розташована на поверхні твердого тіла S – це поверхневий заряд. Товщина поверхневої частинии ПЕШ дорівнює z. Друга група негативних йонів перебуває в електроліті ELT. Візуально ПЕШ нагадує розподіл електричних зарядів по Гельмгольцу, проте, реальна його модель значно складніша. Частина шару, яка міститься в рідині, є дзеркальним електричним відображенням поверхневого заряду й складається зі щільної та дифузної частин, бо формується під дією нелінійних фізичних процесів – електростатичного притягання та теплового руху йонів у рідині. Матеріалом для виготовлення стінок капілярів можуть слугувати діелектрики або напівпровідники, в залежності від вибраної схеми електрокінетичного перетворювача.
Електрокінетична технологія молекулярної гідроенергетики (англ. electrokinetic hydropower technology) – спосіб вироблення, накопичення, транспортування та розподілу електричної енергії з відновлюваних джерел енергії, заснований на використанні електрокінетичних явищ в рідинних дисперсних середовищах. Кожна електрокінетична енергетична технологія складається з послідовності певних операцій або процесів, які виконуються за допомогою сукупності технічних засобів, зведених в молекулярні системи енергетики.
Електрокінетична система молекулярної гідроенергетики (англ. electrokinetic hydropower system) – сукупність електрокінетичних технологій та обладнання, заснованих на використанні електрокінетичних явищ в рідинних дисперсних середовищах для вироблення, накопичення, транспортування та розподілу електричної енергії.
Відновлюваний рух йонів, інших заряджених частинок рідинного електроліту може здійснюватися тиском плинної води або ж силами адгезії та поверхневого натягу рідини на кордоні фаз. Електрокінетичні способи отримання електричного струму відносяться до немеханічних, бо в енергетичних перетвореннях, зазвичай, не використовуються громіздкі рухомі елементи (ротори).
На відміну від макроскопічних технологій, які потребують подвійного, а інколи, й потрійного проміжного перетворення одного виду енергії в інший, електрокінетичні енергетичні технології є переважно прямими способами отримання електричного струму. Цікавість до них спричинена, в першу чергу, можливістю створення малогабаритних матричних пристроїв генерації електричної енергії а також співимірних з ними по розмірам та масі накопичувачів енергії, які дозволяють поряд з існуючими використовувати нові джерела відновлюваної енергії, притаманні гідросфері, зокрема, енергію молекул всередині рідини та на кордоні фаз, градієнт солоності води тощо. Адже у світлі досягнень нанотехнологій та біотехнологій на початку третього тисячоліття ми очікуємо використання нових джерел відновлюваної енергії та нових технологій виробництва електричного струму.[1][2]
Історія
Науково-технологічною базою електрокінетичної гідроенергетики є досягнення молекулярної фізики, фізичної хімії, хімії та фізики поверхні, електродинаміки, квантової теорії речовини та поля, термодинаміки і, в кінці кінців, молекулярної гідродинаміки, хімічного інжинірингу та матеріалознавства.
Невпинний прогрес у вивченні електрокінетики спостерігається, починаючи з авангардних дослідів Фердинанда Рейсса,[3] Фрідріха Дорна, Георга Квінке[4] через теорію та моделі подвійного електричного шару Германа Гельмгольца [5], Луї Гуї [6], Девіда Чепмена [7], Отто Штерна [8], Маріана Смолюховського [9] до фізики та хімії поверхні Джозая Гіббза, хімічної кінетики та осмотичного тиску Якоба Вант-Гоффа [10], теорії електролітичної дисоціації Сванте Арреніуса [11], методів статистичної механіки в колоїдній хімії та хімії поверхні Ірвінга Ленгмюра [12], до розуміння диполь-дипольної електростатичної взаємодії між зарядами Віллема Кеезома, міжмолекулярної поляризаційної взаємодії та провідності електролітичних розчинів Петера Дебая, теорії хімічного зв'язку та міжмолекулярних дисперсійних сил Фріца Лондона і, накінець, до практичних аспектів мікогідродинаміки та наногідродинаміки, електроосмосу другого роду Станіслава Духіна та Наталії Міщук, електроосмосу індукованого заряду Мартіна Базанта, Тодда Сквайреса та ін. а також вчених Інституту колоїдної хімії і хімії води ім. А.В. Думанського Національної Академії наук України, зокрема, Володимира Шилова, Миколи Жарких та Іллі Разілова. Серед книг, приурочених цій темі, можна виділити ґрунтовні роботи Анжела Дельгадо та ін. в галузі інтерфейсної електрокінетики [13], Антоніо Рамоса та ін. у галузі діелектрофорезу рідин та частинок, електрокінетики змінного струму, електрозмочування та електрогідродинаміки [14].
У періодичних виданнях з’явилася ціла низка публікацій, присвячених окремим теоретичним та практичним аспектам побудови електрокінетичних пристроїв для генерації електричної енергії. В більшій частині публікацій представлено результати досліджень електрокінетичних енергогенеруючих пристроїв, влаштованих по схемі Квінке з транспортування контрйонів у мікроканалах та наноканалах різної форми та розмірів зовнішнім тиском. Гідродинамічні та електрокінетичні параметри електроліту при його транспортуванні у вузьких каналах доволі адекватно описуються рівняннями Нав'є-Стокса та Пуассона-Больцмана. Транспортування йонів моновалентного електроліту в схемах коміркового типу підпорядковується рівнянню Нернста-Планка, яке встановлює залежність між електрорушійною силою (різницею потенціалів) та йонною концентрацією й дозволяє передбачити максимальний робочий потенціал, що може бути отриманий в результаті електрохімічної взаємодії, коли відомі тиск та температура.
Дисперсні системи в електрокінетичній гідроенергетиці несуть подвійне навантаження, так як вони характеризують як електропровідний розчин, так і пористу структуру, відповідальну за утворення електроосмотичного потоку. Кінетичні та електричні процеси в дисперсних системах визначаються електричними атрибутами молекулярних частинок та міжфазної поверхні, які, зокрема, обумовлюють адгезію, когезію, адсорбцію, поверхневий натяг а також поведінку частинок під впливом електричного поля. Енергетичний стан та параметри електрокінетичної дисперсної системи описуються величиною надлишкової адсорбції Гіббза (поверхневого надлишку розчиненої речовини в поверхневому шарі розчину порівняно з його об’ємною концентрацією), ізотермою адсорбції, наприклад, ізотермою адсорбції Фрейндліха (співвідношенням між кількістю адсорбованої речовини та концентрацією її в розчині при сталій температурі) або ж ізотермою мономолекулярної адсорбції Ленгмюра (залежністю кількості адсорбованого на поверхні газу від його тиску при сталій температурі).
Електрокінетика, як і взаємодія атомів усередині молекули, має кулонівську природу, електростатичні сили лежать і в основі міжмолекулярної взаємодії; тож, досліджувати електрокінетику маємо в сукупності з електростатикою.
Базова схема електрокінетичної системи для виробництва електричного струму
Функціональна та структурна схеми

Електрокінетична система гідроенергетики включає електроліт ELT, приймач-перетворювач RT, зовнішній електричний навантажувальний опір RL та електричний адаптер EA – форма лише й потрібна для того, щоб реалізувати функцію.
Електроліт – розчин, який володіє електропровідністю. Носіями електричного струму в розчинах електролітів є йони, утворені, зазвичай, дисоціацією молекул електроліту. Склад розчинів оцінюється масовою ωS [%], об’ємною φB [%] та молярною χB [%] частками, молярною СB [моль/м3] та масовою ρB [кг/м3] концентраціями а також молярною концентрацією еквівалента CNB. Електрокінетичні процеси, які проходять в системі, змінюють склад та параметри електроліту, ELT1(E1) → ELT2(E2).
Приймач-перетворювач енергії RT є активною чутливою структурою, яка трансформує енергетичні властивості йонів, інших малих заряджених частинок молекулярної системи в електричну енергію ЕE. У загальному випадку приймач-перетворювач енергії RT складається із рушія MV та електрокінетичного перетворювача EK. Рушієм MV може бути джерело відновлюваної енергії, наприклад, тиск плинної води річкових стоків, океанічних течій та припливів гравітаційного походження, який приводить у рух електроліт ELT і створює електроосмотичний потік йонів, інших малих заряджених частинок всередині та на кордоні фаз. У певних випадках джерелом відновлюваної енергії можуть слугувати міжмолекулярні сили адгезії та поверхневого натягу рідини (електроліту) на кордоні фаз. Рушій MV конструктивно є пристроєм, який обертає енергію молекул всередині рідини та на кордоні фаз або ж кінетичну енергію плинної води в енергію спрямованого руху йонів електроліту. Електрокінетичний перетворювач EK трансформує енергетичні властивості йонів, інших малих частинок речовини електроліту, подвійного електричного шару в електричну енергію EE (енергію електричного струму I).
Молекулярна електрокінетична система генерації електричного струму функціонує так. Тиск плинної води p1 [Па] та/або міжмолекулярні сили адгезії та поверхневого натягу рідини на кордоні фаз трансформуються за допомогою рушія MV у спрямований рух рідинного електроліту ELT, який в електрокінетичному перетворювачі EK неперервно деформує подвійний електричний шар (ПЕШ) на кордоні фаз, і йони дифузного шару зміщуються в напрямку потоку рідини. Внаслідок руху зарядів виникає поверхневий струм, і встановлюється різниця потенціалів на кінцях діафрагми. Ця різниця потенціалів, у свою чергу, приводить до появи струму провідності в зворотному напрямку. Різниця потенціалів збільшується, доки ці струми не зрівняються. З цього моменту вона приймає стале значення. Так різниця потенціалів у контурі зовнішнього навантажувального опору RL переростає в енергію електричного струму EC (I). Параметри електричного струму (напруга, сила струму, частота) доводяться в електричному адаптері EA до стандартних значень, і струм спрямовується споживачам та/або в електричну мережу ЕN.
Робочим тілом у електрокінетичних системах енергетики може служити як штучний, так і природний електроліт, наприклад, морська солона вода.
Схеми, конструкції, параметри та характеристики систем електрокінетичної гідроенергетики досліджуються у рамках молекулярної фізики, фізики та хімії поверхні, молекулярної гідродинаміки, термодинаміки та електродинаміки.
Електрокінетичний перетворювач
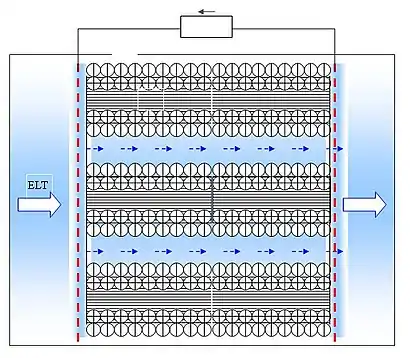
Електрокінетичний перетворювач CPEK є капілярною структурою CS у вигляді циліндричних трубок із діелектричною або напівпровідниковою поверхнею стінок. Ця структура занурена в потік електроліту ELT так, що плинний електроліт під тиском входить у вхідні отвори INL і покидає капілярну структуру через вихідні отвори OUTL, утворюючи електроосмотичний потік EOFL та подвійний електричний шар DL на кордоні фаз «тверде тіло – рідина».
При проходженні електроліту ELT, наприклад, слабкого водного розчину повареної солі H2O + NaCl через капілярну структуру формується відновлюваний електроосмотичний потік EOFL. На кордоні фаз «тверде тіло – електроліт» під дією електростатичного притягання та теплового руху вільних йонів формується міжфазний подвійний електричний шар (ПЕШ) DL, виникає стрибок потенціалу течії. При русі рідини через пористу структуру під дією зовнішньої сили, наприклад під тиском, разом із рідиною рухаються протиіони дифузної частини ПЕШ, формуючи електричний струм течії в напрямку руху рідини. Під впливом струму вздовж пористої структури виникає потенціал течії – різниця потенціалів на вхідному та вихідному електродах ELS. Потенціал течії заставляє протийони дифузної частини ПЕШ рухатися назустріч струму течії, так формуючи струм провідності. У сталому режимі струм течії врівноважується струмом провідності. При русі йони захоплюють із собою молекули рідини. Зчеплення йонів з молекулами рідини відбувається за рахунок водневих зв'язків у молекулах рідини. Тож, рідина починає рухатися в напрямку, протилежному тому, в якому вона рухалася у вихідному стані, в результаті, рух рідини в напрямку дії тиску гальмується. Проявляється ефект електров’язкості – різниця між тією швидкістю, що описується рівняннями механіки рідини без врахування дії ПЕШ, та реальною швидкістю частинок із врахуванням дії ПЕШ.
Різниця потенціалів використовується для утворення електричного струму I на зовнішньому електричному навантажувальному опорі RL. Постійний електричний струм може буде перетворений у змінний в електричному адаптері і доведений до стандартів, придатних для використання споживачами та/або спрямування в електричну мережу.
Енергетичні параметри
При течії електроліту через мембрану під тиском Δp виникає електричний струм. Природа цього струму – захват йонів рухомої частини ПЕШ. Оскільки в рухомій частині ПЕШ є надлишок йонів одного знаку, по одну сторону капілярної стуктури будуть накопичуватися позитивні заряди, а по іншу – від’ємні. В електростатиці використовується поняття електричного потенціалу. Енергетичний стан деякої точки простору, розташованої на відстані r [м] від деякого заряду q [Кл], визначається електричним потенціалом φ [В],
φ = q/(4∙π∙ε0∙εr∙r),
де ε0 – діелектрична проникність у вакуумі, ε0 = 8,8542•10–12 Ф/м.
Потенціал, сформований системою зарядів, визначається як скалярна сума у скалярному полі окремих потенціалів, або ж як векторна сума у векторному полі. Потенціальна енергія системи нерухомих зарядів, що формують електростатичне поле, дорівнює енергії взаємодії цих зарядів.
Накопичення зарядів по різниу сторону капілярної стуктури приводить до появи різниці потенціалів між ними та зумовлює протікання струму I в об’ємі електроліту. Накопичення зарядів та збільшення різниці потенціалів продовжуватимуться, допоки відбудеться повна компенсація конвекційного струму. Цьому стаціонарному стану відповідає різниця потенціалів Δφs, що називається потенціалом течії.
Силою, яка рухає рідину, звичайно є різниця тисків Δр = р2 – р1 [Па], де р1 [Па] – тиск на вході структури, р2 [Па] – тиск на виході структури. У стані рівноваги сила фільтраційного струму ISTR дорівнює силі зворотного струму IRV, тобто ISTR = IRV [А]. Фільтраційний струм ISTR дорівнює сумі зарядів, які проходять в одиницю часу, й визначається об’ємними витратами рідини dV/dt.
Питомі обємні витрати ламінарного потоку рідини dV/dt у циліндричному капілярі, згідно закону Хагена-Пуазейля, пропорційні перепаду тиску ∆p [Па] на одиницю довжини капіляра LСP [м] ,
dV/dt = QV = k•[(p2 – p1)/LСP]•d4,
де QV [м3•с–1] – обємні витрати рідини, яка протікає за 1 с через поперечний перетин циліндричної трубки, p1 [Па] та p2 [Па] – тиски рідини на вході трубки та в певній точці, dСP – діаметр трубки [м], dСP = 2•rСP, LСP [м] – довжина тубки, μ [Па•с] – коефіцієнт динамічної в’язкості; k – коефіцієнт, який пов'язаний з коефіцієнтом динамічної в’язкості μ, згідно Джорджу Стоксу k = π/(128•μ). Закон, який встановлює залежність об’ємних витрат рідини від перепаду тиску ∆p на одиницю довжини капіляра, вперше був сформульований німецьким інженером і будівельником Готтхільфом Генріхом Хагеном у 1839 році]. Та вже у 1841 році він був повторно виведений французьким фізиком і фізіологом Жаном Леонардом Пуазёйлем, який детально досліджував різні капілярні системи, в тому числі, й живого організму.
Один з методів визначення параметрів електрокінетичної системи полягає у застосуванні закону Ома в інтегральній формі,
U = Rx•I ,
де Rx [Ом] – електричний опір електроосмотичної структури, заповненої рідиною, I [А] – сила електричного струму.
Електричний опір електроосмотичної структури Rx [Ом] можна визначити за класичною формулою
Rx = (1/χEL)•(LCP/АCP,
де χEL [См•м–1] – питома електропровідність структури, величина, зворотна питомому електричному опору ρEL, χEL = 1/ρEL.
Питома електропровідність структури χEL складається з поверхневої χS та об’ємної χV провідностей електроліту,
χEL = χS + χV.
Як електроліт може бути використаний водний розчин солі NaCl. На кордоні електроліту та капілярної структури утворюється ПЕШ, протяжність екрануючого шару Дебая в ньому звичайно становить 1-100 нм. ПЕШ можна розглядати як конденсатор з невисоким дзета-потенціалом ζ = 0,01-0,1 В. Його величина дорівнює різниці потенціалу поверхні та потенціалу за ПЕШ.
Дзета-потенціал одного капіляра можна знайти через потенціал течії та силу струму течії за допомогою рівняння Смолюховського. Щоб знайти дзета-потенціал капілярної структури, можна скористатися електропровідністю χ. Потенціал течії U, сила струму течії I і дзета -потенціал ζ зв’язані між собою через різницю тисків Δр відношеннями
U/Δр = – ε0•εr•ζ/(μ•χEL);
I/Δр = – ε0•εr•ACS•ζ/(μ•LCS),
де μ [Па•с] – в'язкість, χEL [См•м–1] – електропровідність, АCS [м2] – площа поперечного перетину капілярної структури, LCS [м] – довжина капілярної структури, LCS/АCS – постійна структури.
Розробники та користувачі замкнутої системи виробництва електричного струму мають більш широкі можливості вибору електроліту з потрібними електрохімічними параметрами.
Класифікація
Електрокінетичні технології та системи енергетики можна класифікувати за фізичними принципами отримання електричного струму, за способами нагнітання електроосмотичного потоку та за природою (походженням) електроліту. Для отримання електричної енергії електрокінетичні технології та системи енергетики можуть використовувати потенціал течії (протікання), електрохімічний потенціал Нернста або ж електрокінетичний спосіб нагнітання зонної структури напівпровідника.
Робочим тілом у електрокінетичних системах енергетики може служити як штучний, так і природний електроліт, наприклад, морська солона вода. Енергетичні системи, в яких використовується штучний електроліт, звичайно є конструкціями закритого типу (із замкнутим циклом обертання електроліту), де електроліт не контактує із зовнішнім середовищем. До таких об’єктів належать, зокрема, багатоелементна мембранна система генерації електричного струму з мобілізацією електросмотичного потоку тиском плинної води. Типовими конструкціями з електролітом природного походження є офшорна та приморська електрокінетичні системи, для яких природним розчином електроліту є морська солона вода на основі йонів хлористого натрію, а моря та океани є натуральними резервуарами цього розчину.
Перспективними технологіями та системами електрокінетичної гідроенергетики є електрокінетичний реверсивний енергогенеруючий пристрій клітинного типу, в якому активний розчин електроліту циркулює пористою структурою між двома еластичними комірками, котрі поперемінно змінюють свій об’єм під тиском плинної води, офшорні та приморські електрокінетичнім енергетичні системи, для яких природним розчином електроліту є морська солона вода на основі йонів хлористого натрію, а моря та океани слугують натуральними резервуарами цього розчину.
В офшорних системах нагнітання електроліту, зазвичай, здійснюється тиском океанічної течії.
У приморській (береговій) електрокінетичній системі нагнітання електроліту здійснюється силами адгезії і поверхневого натягу та/або силами осмотичного тиску. Як розчин електроліту в системі використовується та ж морська вода, резервуаром якої є моря та океани, а капілярною структурою слугує звичайний пісок, який в необмежених кількостях розсипаний на морських узбережжях.
Джерела
- Сидоров В.І. (2018). Від макроскопічних до молекулярних технологій відновлюваної енергії. Промислова електроенергетика та електротехніка – № 3. – С. 34-42. (Укр.).
- Сидоров, В.І. (2020). Електрокінетична енергетика в кн. Молекулярна енергетика. Теорія та технічні рішення. (Укр.). Черкаси: Вертикаль, видавець Кандич С.Г. с. 486. ISBN 978-617-7475-79-7.
- Navier, C. L. M. H. (1833.). Résumé des leçons données à l'École des ponts et chaussées sur l'application de la mécanique à l'Établissement des constructions et des machines, tome 2, Deuxième partie, leçons sur le mouvement et la résistance des fluides, la conduite et la distribution des eaux, Troisième partie, leçons sur l'établissement des machines(Фр.). Paris: chez Carilian-Gœury.
- Navier, C. L. M. H. (1833.). Résumé des leçons données à l'École des ponts et chaussées sur l'application de la mécanique à l'Établissement des constructions et des machines, tome 1, Première partie contenant des leçons sur la résistance des matériaux, et sur l'établissement des constructions en terre, en maçonnerie et en charpente (Фр.). Paris: chez Carilian-Gœury.
- Stokes, G. G. (1864). On the discontinuity of arbitrary constants which appear in divergent developments. Transactions of the Cambridge Philosophical Society. – Vol. 10. Part I. – Р. 105-124, 125-128. (Англ.).
- Stokes, G. G. (1856). On the numerical calculation of a class of definite integrals and infinite series. Transactions of the Cambridge Philosophical Society. – Vol. 9. Part I. – Р. 166-188.
- Gibbs, J. W. (1876). On the Equilibrium of Heterogeneous Substances. Transactions of the Connecticut Academy of Sciences (Англ.).
- Van der Waals, J. D. (1873). Over de Continuiteit van den Gas- en Vloeistoftoestand (on the continuity of the gas and liquid state). PhD thesis (Нім.). Leiden, The Netherlands.
- Keesom, W.H. The second virial coefficient for rigid cpherical molecules whose mutual attraction is equivalent to that of a quadruplet placed at its center // Proc. R. Acad. Sci. - 1915.– Vol. 18. – Р. 636-646.
- Debye, P. Zur Theorie der spezifischen Waerme // Annalen der Pyisik. Leipzig. – 1912. - 39(4). - P. 789-839.
- Heitler, W. and London, F. Wechselwirkung neutraler Atome und homöopolare Bindung nach der Quantenmechanik // Zeitschrift für Physik. — 1927. — 44. — Р. 455472.
- Jones, J. E. On the Determination of Molecular Fields. I. From the Variation of the Viscosity of a Gas with Temperature // Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. — 1924. — 106 (738). — Р. 441—462.
- Jones, J. E. On the Determination of Molecular Fields. II. From the Equation of State of a Gas // Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. — 1924. — 106 (738). — Р. 463.
- Jones, J. E., Ingham, А. Е. On the Calculation of Certain Crystal Potential Constants, and on the Cubic Crystal of Least Potential Energy // Proceedings of the Royal Society. A. — 1925. — 107. — Р. 636—653.
- Garner, W. E., Lennard-Jones, J. E. Molecular Spectra and Molecular Structure. A general discussion // Transactions of the Faraday Society. — 1929. — Т. 25. — Р. 611—627.
- Lennard-Jones, J. E. The electronic structure of some diatomic molecules // Transactions of the Faraday Siciety. 1929. - Vol. 25. - P. 668-686.
- Lennard-Jones, J. E. Wave Functions of Many-Electron Atoms // Mathematical Proceedings of the Cambridge Philosophical Society. — 1931. — 27 (3). — Р. 469.
- Lennard-Jones, J. E. The electronic structure and the interaction of some simple radicals // Transactions of the Faraday Society. — 1934. — Vol. 30. — Р. 70-148
- Lennard-Jones, J. E. The Electronic Structure of Some Polyenes and Aromatic Molecules. I. The Nature of the Links by the Method of Molecular Orbitals // Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. — 1937. — 158 (894). — Р. 280.
- Lennard-Jones, J. E. The Molecular Orbital Theory of Chemical Valency. I. The Determination of Molecular Orbitals. Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. — 1949. — 198 (1052).
- Hall, G. G., Lennard-Jones, J. E. The Molecular Orbital Theory of Chemical Valency. III. Properties of Molecular Orbitals // Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. — 1950. — 202 (1069). — Р. 155.
- Tabeling, P. Introduction à la microfluidique. – Belin, 2003. – 254 р.
- Squires, T. M., Quake S. R. Microfluidics: Fluid physics at the nanoliter scale // Reviews of Modern Physics. – 2005. – Vol. 77. – Р. 977-1026.
- Bruus, H. Theoretical Microfluidics. - Oxford University Press. 2008. - 346 p.
- Berthier, J. Micro-Drops and Digital Microfluidics – Norvich, NY: William Andrew Inc., 2008. – 441 p.
- Galindo-Rosales, F. J. (Ed.). Complex Fluid-Flows in Microfluidics / Springer International publisher AG, 2018. – 111 p.
- Reuss, F. F. (1808). Notice sur un nouvel effet de l'électricité galvanique. // Mémoires de la Societé Impériale des Naturalistes de Moscou. Mémoires de la Societé Impériale des Naturalistes de Moscou. – Vol. 2. – Р. 327-337. (Фр.).
- Quincke, G. H. (1859). Ueber eine neue Art electrischer Ströme. Ann. Phys. Chem. – Vol. 107. – Р. 1-47. (Нім.).
- Helmholtz, H. (1879). Studien über electrische Grenzschichten. Annalen der Physik. – Vol. 243, Issue 7. – Р. 337-382. (Нім.).
- Gouy, M. (1910). Sur la constitution de la charge électrique à la surface d'un électrolyte. J. de Physique Théorique et Appliquée. – Vol. 9. – Р. 457-468. (Фр.).
- Chapman, D. J. (1913). A contribution to the theory of electrocapillarity. Philos. Mag. – Vol. 25. – Р. 475-481. (Англ.).
- Stern, O. (1924). Zur Theorie der elektrolytischen Doppelschicht. Zeitschrift für Elektrochemie. – Vol. 30. – Р. 508-516.(Нім.).
- Contribution à la théorie de l’endosmose électrique et de quelques phénomènes corrélatifs. Bulletin international de l’Académie des Sciences de Cracovie. – Vol. 8. – Р. 182-200. (Фр.). 1903.
- Hoff, J. H. van't. (1884). Etudes de dynamique chimique (Фр.). Amsterdam: Frederik Muller Publisher. с. 242.
- Arrhenius, S. (1896). On the Influence of Carbonic Acid in the Air upon the Temperature of the Ground. London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science (fifth series). – April. – Vol. 41. – Р. 237-275. (англ.).
- Arrhenius, S. (1884). Recherches sur la conductivité galvanique des électrolytes, doctoral dissertation (Фр.). Stockholm: Royal publishing house, P.A. Norstedt & söner. с. 89.
- Langmuir, I. (1906). The Constitution and Fundamental Properties of Solids and Liquids: II. Liquids. Journal of the American Chemical Society. – Vol. 39 (9). – Р. 1848-1906. (англ.).
- Squires, T. M. and Bazant, M. Z. Breaking symmetries in induced-charge electro-osmosis and electrophoresis // J. Fluid Mech. — 2006. — Vol. 560. — Р. 65-101.
- Духин, С. С., Шилов, В. Н. Диэлектрические явления и двойной слой в дисперсных системах и полиэлектролитах. — Киев: Наук. думка, 1972. — 246 с.
- Dukhin, S. S. & Derjaguin, B. V. Electrokinetic Phenomena. — New York: John Wiley and Sons, 1974.
- Delgado, A. V. Interfacial Electrokinetics and Electrophoresis. — New York, NY: Marcel Dekker, Inc., 2002. — 991 p.
- Ramos, A. (Ed.). Electrokinetics and Electrohydrodynamics in Microsystems – Wien, New York: Springer, 2011. – 300 p.
- Burgreen, D. and Nakache, F. R. Efficiency of Pumping and Power Generation in Ultrafine Electrokinetic Systems J. Appl. Mech. – 1965. – 32 (3). – P. 675-679.
- Chun, M. S., Lee, T. S., and Choi, N. W. Microfluidic Analysis of Electrokinetic Streaming Potential Induced by Microflows of Monovalent Electrolyte Solution Journal of Micromechanics and Microengineering. – 2005. – Vol. 1, № 4. – P. 710-719.
- Van der Heyden, F. H. et al. Power Generation by Pressure-Driven Transport of Ions in Nanofluidic Channels Nano Letters. – 2007. – Vol. 7, № 4. – P. 1022-1025.
- Ren, Y. and Stein, D. Slip-Enhanced Electrokinetic Energy Conversion in Nanofluidic Channels Nanotechnology. – 2008. – Vol. 19, № 19. – Art. № 195707.
Примітки
- Сидоров, В.І. (2020). Електрокінетична гідроенергетика в кн. Молекулярна енергетика. Теорія та технічні рішення. (Укр.). Черкаси: Вертикаль, видавець Кандич С.Г. с. 486. ISBN ISBN 978-617-7475-79-7.
- Сидоров, В.І. (2018). Від макроскопічних до молекулярних технологій відновлюваної енергії. Промислова електроенергетика та електротехніка. – № 3. – С. 34-42 (Укр.).
- Reuss, F. F. (1808). Notice sur un nouvel effet de l'électricité galvanique. Mémoires de la Societé Impériale des Naturalistes de Moscou. – Vol. 2. – Р. 327-337 (Фр.).
- Quincke, G. H. (1859). Ueber eine neue Art electrischer Ströme. Ann. Phys. Chem. – Vol. 107. – Р. 1-47 (Нім.).
- Helmholtz, H. (1879). Studien über electrische Grenzschichten. Annalen der Physik. – Vol. 243, Issue 7. – Р. 337-382 (Нім.).
- Gouy, M. (1910). Sur la constitution de la charge électrique à la surface d'un électrolyte. J. de Physique Théorique et Appliquée. – Vol. 9. – Р. 457-468 (Фр.).
- Chapman, D. J. (1913). A contribution to the theory of electrocapillarity. Philos. Mag. – Vol. 25. – Р. 475-481 (Англ.).
- Stern, O. (1924). Zur Theorie der elektrolytischen Doppelschicht. Zeitschrift für Elektrochemie. – Vol. 30. – Р. 508-516 (Нім.).
- Smoluchowski, Marian (1903). Contribution à la théorie de l’endosmose électrique et de quelques phénomènes corrélatifs. Bulletin international de l’Académie des Sciences de Cracovie. – Vol. 8. – Р. 182-200 (Фр.).
- Hoff, J. H. van't. (1884). Etudes de dynamique chimique (Фр.). Amsterdam: Frederik Muller Publisher. с. 242.
- Arrhenius, S. ( (1884). Recherches sur la conductivité galvanique des électrolytes, doctoral dissertation (Фр.). Stockholm: Royal publishing house, P.A. Norstedt & söner. с. 89.
- Langmuir, I. (1906). The Constitution and Fundamental Properties of Solids and Liquids. Journal of the American Chemical Society. – Vol. 39 (9). – Р. 1848-1906 (Англ.).
- Delgado, A. V. (2002). Interfacial Electrokinetics and Electrophoresis (Англ.). New York, NY: Marcel Dekker, Inc. с. 991.
- Ramos, A. (2011). Electrokinetics and Electrohydrodynamics in Microsystems (Англ.). Wien, New York: Springer. с. 300.