Оксид кальцію
Окси́д ка́льцію, негашене вапно — неорганічна бінарна сполука кальцію та оксигену складу CaO. В'язка мінеральна кристалічна тугоплавка речовина білого кольору. Температура плавлення 2585°С. Проявляє сильні осно́вні властивості.
| Оксид кальцію | |
|---|---|
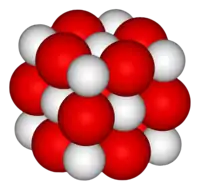 Кристалічна структура CaO | |
| Назва за IUPAC | Кальцій оксид |
| Інші назви | негашене вапно |
| Ідентифікатори | |
| Номер CAS | 1305-78-8 |
| Номер EINECS | 215-138-9 |
| DrugBank | 15648 |
| KEGG | C13140 і D01679 |
| ChEBI | 31344 |
| RTECS | EW3100000 |
| SMILES |
O=[Ca][1] |
| InChI |
InChI=1S/Ca.O |
| Номер Бельштейна | 8129996 |
| Номер Гмеліна | 485425 |
| Властивості | |
| Молекулярна формула | CaO |
| Молярна маса | 56,077 г/моль |
| Зовнішній вигляд | біло-сірі кристали |
| Густина | 3,34 г/см3[2] |
| Тпл | 2898 °C[2] |
| Розчинність (вода) | реагує |
| Розчинність (кислоти) | розчинний |
| Показник заломлення (nD) | 1,8396 |
| Структура | |
| Кристалічна структура | кубічна |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
-634,9 кДж/моль |
| Ст. ентропія S |
38,1 Дж/моль·К |
| Теплоємність, c |
42,0 Дж/моль·К |
| Пов'язані речовини | |
| Інші катіони | оксид магнію |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
У техніці оксид кальцію називають звичайно негашеним, або паленим вапном. Остання назва походить від способу його одержання: прожарювання, або «випалювання» вапняку. Одержують шляхом випалювання вапняку, крейди та інших карбонатних порід. Процес ведуть при низьких температурах розкладання карбонату кальцію.
Поширення у природі
Оксид кальцію є однією з найбільш поширених сполук у природі. Він часто трапляється у складі природних карбонатів, паралельно із оксидом магнію. Основними сполуками, з яких добувають CaO є кальцит, мармур, вапняк, арагоніт, доломіт та багато інших.
Хімічні властивості
З водою оксид кальцію реагує дуже енергійно, з виділенням значної кількості тепла і утворенням гідроксиду кальцію:
Реакцію взаємодії оксиду кальцію з водою в техніці називають «гашенням» вапна, а продукт реакції — гідроксид кальцію — гашеним вапном.
CaO проявляє сильні осно́вні властивості: взаємодіє з кислотами та кислотними оксидами (зокрема, активно поглинає вуглекислий газ із повітря), з амфотерними оксидами:
Кальцій піддається відновленню з оксиду алюмінієм та коксом:
Отримання
Виробництво у промисловості
Негашене вапно (оксид кальцію) одержують прожарюванням (випалюванням) вапняку або крейди. Карбонат кальцію починає розкладатися при 850°С. Чим вища температура, тим швидше йде розклад. Але вище 1200°С домішки, що є у вапняку, починають обплавлятися, і це ускладнює процес розкладу. Тому «випалювання» вапняку проводять при 1000—1200°С.
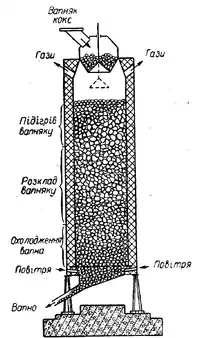
Процес «випалювання» здійснюють у вертикальних шахтних печах, облицьованих зсередини вогнетривкою цеглою. Шихту, тобто суміш вапняку і коксу, завантажують у піч через верхній отвір. Шматки вапняку і коксу роблять такими, щоб їх діаметр був приблизно 10 см. Тоді повітря і топочні гази легко проходять крізь шихту, і вапняк розкладається рівномірно по всій масі.
Гарячі гази, що виникають при горінні палива і розкладі вапняку, піднімаючись вгору, поступово охолоджуються, нагріваючи шихту. Палене вапно опускається в нижню частину печі, де охолоджується повітрям, що подається знизу.
Застосування
Будівництво
Вапно дуже широко застосовується у будівельній справі, а також у хімічній промисловості для одержання хлорного вапна. Щорічний світовий видобуток вапна становить сотні мільйонів тонн.
У будівництві використовують гашене вапно, тобто гідроксид кальцію. З цією метою негашене вапно обробляють водою. При цьому пористі шматки оксиду кальцію (негашеного вапна) жадібно поглинають воду і реагують з нею з виділенням значної кількості тепла. Внаслідок цього частина води випаровує, а оксид кальцію перетворюється у пухку масу гідроксиду кальцію (гашеного вапна), яку називають пушонкою[джерело?]. При надлишку води гашене вапно утворюється у вигляді тістоподібної маси.
Зброя
У 80 році до нашої ери римський воєначальник Серторій у боротьбі з харацитанами в Іспанії, які сховалися в недоступних печерах, використав задушливі хмари їдкого вапна. Подібна хімічна зброя застосовувалася в Китаї під час придушення збройного повстання селян 178 року н. е.: «вапняні колісниці», обладнані міхами, вдували порох вапняку в натовп.
Вважається, що негашене вапно також було складником грецького вогню. У разі контакту з водою негашене вапно може підвищити температуру понад 150 °C та запалити паливо.
Девід Юм, у власній історії Англії, розповідає, що на початку правління Генріха III англійський флот знищив вторгнення французького флоту, засліпивши флот противника негашеним вапном. Негашене вапно, можливо, було використано в середньовічній військово-морській війні — аж до використання «вапняних мінометів», для кидання його на ворожі кораблі.
Геноцид
Шар оксиду кальцію у кілька сантиметрів завтовшки, іноді наносили на підлогу вагонів для великої рогатої худоби, які використовувалися задля перевезення євреїв та інших затриманих, до нацистських концентраційних та винищувальних таборів під час Голокосту.
Безпека
Внаслідок бурхливої реакції негашеного вапна з водою, негашене вапно викликає сильне подразнення під час вдихання або у разі доторку з вологою шкірою чи очима. Вдихання може викликати кашель, чхання, посилене дихання. Потім це може розвинутися в опіки з перфорацією носової перегородки, болем у животі, нудотою та блювотою. Хоча негашене вапно не вважається пожежонебезпечним, його взаємодія з водою, може вивільнити достатню кількість тепла, щоби запалити горючі матеріали.
Див. також
Примітки
- CALCIUM OXIDE
- За тиску 101,3 кПа
Джерела
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2007. — Т. 2 : Л — Р. — 670 с. — ISBN 57740-0828-2.
- Рипан Р., Четяну И. Неорганическая химия: Химия металлов / В. И. Спицын. — М. : "Мир", 1971. — Т. 1. — 561 с. (рос.)
- Деркач Ф. А. Хімія. — Львів : Львівський університет, 1968. — 312 с.

