піРНК
піРНК, РНК що взаємодіють з PIWI (англ. PIWI-interacting RNA, piRNA) — окремий клас малих некодуючих РНК (нкРНК, англ. ncRNA) що взаємодіють з білками PIWI для реалізації механізму спрямованого заглушення активності генів у тварин. Довжина піРНК сягає 21-33 нуклеотиди[1]. Найбільша активність піРНК спостерігається в період ембріонального розвитку організмів і їхньою мішенню є транспозони.
піРНК разом з мікроРНК та міРНК (малі інтерферуючі РНК, англ. small interfering RNA, siRNA) виконують РНК індуковане заглушення генів (англ. RNA silencing) — механізм пост-транскрипційної регуляції рівня мРНК у клітинах. За допомогою РНК заглушення клітина здатна регулювати активність певних генів, швидко реагувати на сигнали що поступають до клітини, при цьому не змінювати нуклеотидну послідовність ДНК. Але піРНК на відміну від мікроРНК та міРНК не так сильно вивчені.
Історія відкриття
Вперше піРНК були виявлені у плодової мухи Drosophila melanogaster. При вивченні того, як в гаметах самців заглушується гени Stellate, було встановлено що з ділянки повторювальних елементів Su(Ste) зчитується РНК в обох напрямках: прямому та зворотному (сенс та антисенс), і така двоспіральна коротка РНК приводить до деградації транскриптів Stellate[2]. Пізніше група Олексія Аравіна показала, що у тканинах сім'яників та у раннього ембріона D. melanogaster наявна велика кількість РНК завдовжки у 23-29 нуклеотидів, які були названі rasiRNA (англ. repeat associated small interfering RNA, малі інтерферуючі РНК, що асоційовані з повторами)[3]. У 2006 році було встановлено, що Piwi (англ. P-element-induced wimpy testis), білок родини Аргонавт, що у D. melanogaster відповідає за заглушення ретротранспозонів, взаємодіє саме з rasiRNA[4].
Біогенез
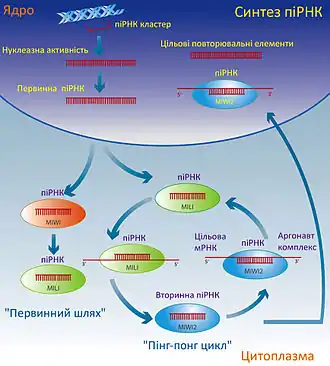
піРНК мають довжину 25-33 нуклеотидів, в залежності від того, який PIWI білок бере участь у їх утворенні[6]. піРНК походять з ДНК різних транспозонів, що називаються піРНК-кластерами. З різних локусів синтезуються піРНК, які мають свої власні, специфічні послідовності[7]. На відміну від біогенезу мікроРНК та ендогенних малих інтерферуючих РНК (ендо-міРНК), для дозрівання яких необхідна активність ферментів родини РНКази III (нуклеаз Дроша та Дайсер), піРНК генеруються незалежно від РНКаз III[8].
Біогенез піРНК краще всього зрозумілий у D. melanogaster. З одного піРНК кластеру може зчитуватися (транскрибуватися) РНК у прямому чи зворотному напрямках (сенс/антисенс). Результатом транскрипції є довга одноланцюгова молекула РНК, первинна піРНК чи піРНК прекурсор[6]. В цитоплазмі поки що не до кінця з'ясований механізм приводить до дозрівання (процесингу) первинної піРНК до антисенсової піРНК довжиною 23-29 нуклеотидів, 5' кінцева ділянка яких дуже схильна на уридин (У). Далі білки сімейства Аргонавт (aubergine (AUB) та PIWI) зв'язуються з такою одноланцюговою антисенсовою піРНК і формують комплекс, що здатен призводити до нуклеазного розрізання мРНК активних транспозонів. Розщеплення мРНК активного транспозону призводить до утворення змістовної піРНК з сильною схильністю до аденіну[5]. Цей механізм називається «пінг-понг цикл».
Функції
Основна роль піРНК — заглушення транспозонів, мобільних генетичних елементів в гаметах різних організмів (мухи, риби, ссавці). Ця роль достатньо консервативна, тобто залишається присутньою в несильно зміненому стані у багатьох тварин впродовж еволюціонування. Транспозони можуть негативно впливати на організм господаря, тому що такі генетичні елементи здатні до копіювання або вирізання та вставлення себе з одного місця ядерної ДНК на інше. Тому контроль активності транспозонів був важливим механізмом, який виробився в організмах. В дорослої тварини заглушення транспозонів відбувається також шляхом активності ендогенних інтерферуючих РНК, тоді як в гаметах таку функцію виконують саме піРНК.
РНК заглушення
Механізм РНК індукованого заглушення (англ. RNA silencing) виконує специфічне «вимкнення» генів-мішеней в організмах шляхом комплементарного розпізнавання мРНК відповідною малою некодуючою РНК (піРНК, мікроРНК чи міРНК). З такої нкРНК та білку сімейства Аргонавт формується RISC, РНК-індукований комплекс заглушення (англ. RNA induced silencing complex).
Деякі РНК формуються у вигляді двоспіральних молекул, але лише один ланцюг з'єднується з білком родини Аргонавт — це так званий гід-ланцюг (англ. guide strand)[8].
Порушення, що виникають через несправності піРНК-залежного механізму
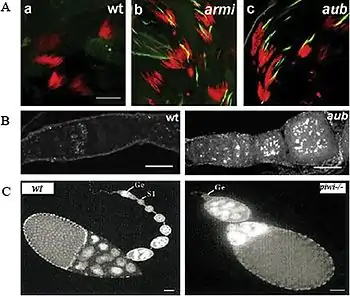
Заглушення генів за допомогою піРНК було досить детально вивчено в Drosophila, де цей каскадний шлях є важливим для формування гамет (гаметогенезу). Мутації в піРНК каскаді призводять до порушень як в створенні осі зародка, так і в формуванні гамет[9].
Див. також
Джерела
- RNA interference (RNAi): by Nature Video (англ.). Nature Reviews Genetics. 2011. ISSN 1471-0056.
- У млекопитающих найдена система управления мобильными генетическими элементами (рос.). «Элементы». 2007.
Примітки
- Maartje J. Luteijn & Rene F. Ketting (August 2013). PIWI-interacting RNAs: from generation to transgenerational epigenetics. Nature reviews. Genetics 14 (8): 523–534. PMID 23797853. doi:10.1038/nrg3495.
- A. A. Aravin, N. M. Naumova, A. V. Tulin, V. V. Vagin, Y. M. Rozovsky & V. A. Gvozdev (July 2001). Double-stranded RNA-mediated silencing of genomic tandem repeats and transposable elements in the D. melanogaster germline. Current biology : CB 11 (13): 1017–1027. PMID 11470406.
- Alexei A. Aravin, Mariana Lagos-Quintana, Abdullah Yalcin, Mihaela Zavolan, Debora Marks, Ben Snyder, Terry Gaasterland, Jutta Meyer & Thomas Tuschl (August 2003). The small RNA profile during Drosophila melanogaster development. Developmental cell 5 (2): 337–350. PMID 12919683.
- Kuniaki Saito, Kazumichi M. Nishida, Tomoko Mori, Yoshinori Kawamura, Keita Miyoshi, Tomoko Nagami, Haruhiko Siomi & Mikiko C. Siomi (August 2006). Specific association of Piwi with rasiRNAs derived from retrotransposon and heterochromatic regions in the Drosophila genome. Genes & development 20 (16): 2214–2222. PMID 16882972. doi:10.1101/gad.1454806.
- Stephane E. Castel & Robert A. Martienssen (February 2013). RNA interference in the nucleus: roles for small RNAs in transcription, epigenetics and beyond. Nature reviews. Genetics 14 (2): 100–112. PMID 23329111. doi:10.1038/nrg3355.
- Gunter Meister (July 2013). Argonaute proteins: functional insights and emerging roles. Nature reviews. Genetics 14 (7): 447–459. PMID 23732335. doi:10.1038/nrg3462.
- Mikiko C. Siomi, Kaoru Sato, Dubravka Pezic & Alexei A. Aravin (April 2011). PIWI-interacting small RNAs: the vanguard of genome defence. Nature reviews. Molecular cell biology 12 (4): 246–258. PMID 21427766. doi:10.1038/nrm3089.
- Benjamin Czech & Gregory J. Hannon (January 2011). Small RNA sorting: matchmaking for Argonautes. Nature reviews. Genetics 12 (1): 19–31. PMID 21116305. doi:10.1038/nrg2916.
- Jaspreet S. Khurana & William E. Theurkauf (2008). piRNA function in germline development. PMID 20614609.