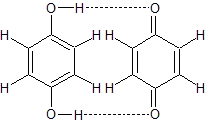Гідрохінон
Гідрохіно́н, або бензен-1,4-діо́л, або хіно́л — ароматична органічна сполука, яка належить до двоатомних фенолів, та має хімічну формулу C6H4(OH)2[3]. Ізомер пірокатехолу та резорцину. Вперше гідрохінон описисав Фрідріх Велер у 1844 році[2].
| Гідрохінон | |
|---|---|
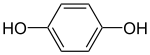 Гідрохінон | |
 | |
| Назва за IUPAC | Бензен-1,4-діол[1] |
| Інші назви | Гідрохінон Хінол 1,4-дигідроксибензен |
| Ідентифікатори | |
| Номер CAS | 123-31-9 |
| Номер EINECS | 204-617-8 |
| DrugBank | 09526 |
| KEGG | D00073, C15603 і C00530 |
| ChEBI | 17594 |
| RTECS | MX3500000 |
| Код ATC | D11AX11 |
| SMILES |
c1cc(ccc1O)O[1] |
| InChI |
1S/C6H6O2/c7-5-1-2-6(8)4-3-5/h1-4,7-8H[1] |
| Номер Бельштейна | 605970 |
| Номер Гмеліна | 2742 |
| Властивості | |
| Молекулярна формула | C6H4(OH)2[1] |
| Молярна маса | 110,1 г/моль[1] |
| Зовнішній вигляд | тверде безбарвне тіло[1] |
| Густина | 1,33 г/см3, тв.[1] |
| Тпл | 172 °C[1] |
| Ткип | 287 °C[1] |
| Розчинність (вода) | 5,4 г/100 мл (15 °C)[1], 8,3 г/100 мл (30 °C)[2] |
| Кислотність (pKa) | 10,85 (25 °C)[1] |
| Структура | |
| Дипольний момент | нуль |
| Небезпеки | |
| ГГС піктограми | 
|
| ГГС формулювання небезпек | H302, H317, H318, H341, H351, H400 |
| ГГС запобіжних заходів | P201, P202, P261, P264, P270, P272, P273, P280, P281, P301+P312, P302+P352, P305+P351+P338, P308+P313, P310, P321, P330, P333+P313, P363, P391, P405, P501 |
| Класифікація ЄС | Carc. Cat. 3 Muta. Cat. 3 |
| R-фрази | R22, R40, R41, R43, R50, R68 |
| S-фрази | S2 S26 S36/37/39 S61 |
| NFPA 704 |
 1
2
0
|
| Температура спалаху | 165 °C (закрита чаша)[1] |
| Температура самозаймання | 516 °C (закрита чаша)[1] |
| Пов'язані речовини | |
| Інші (Бензендиоли) | Пірокатехол Резорцин |
| Пов'язані речовини | 1,4-бензохінон |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Фізичні властивості
Є безбарвною твердою речовиною без запаху[1]. Розчинний в етанолі, ацетоні, воді, погано розчинний в бензені та третрахлорметані[2][1].
Має три кристалічні модифікації: α, β і γ. Перша з них є стабільною і утворюється при кристалізації гідрохінону з води. Має виглядів голок. Β-модифікація утворюється при кристалізації з метанолу чи ізопропанолу. Γ-модифікація утворюється при сублімації і має вигляд призм. Інші властивості показані в таблиці[2]:
| Модифікація | Температура плавлення | Сингонія |
|---|---|---|
| Α | 173.8 – 174.8 °C | Гексагональна |
| Β | - | - |
| Γ | 169 °С | Моноклінна |
Отримання
Окисненням п-диізопропілбензену
При алкілювання бензену пропіленом можна отримти п-диізопропілбензен. Його окиснюють повітрям в слаболужному середовищі до гідропероксиду при температурі 80-90 °С. Далі до гідрпероксиду додається 0,2—1% сульфатної кислоти, яка каталізуює його розщеплення з утворенням гідрохінону та ацетону. Вихід реакції складає 80% (починаючи з диізопропілбензену)[2]:
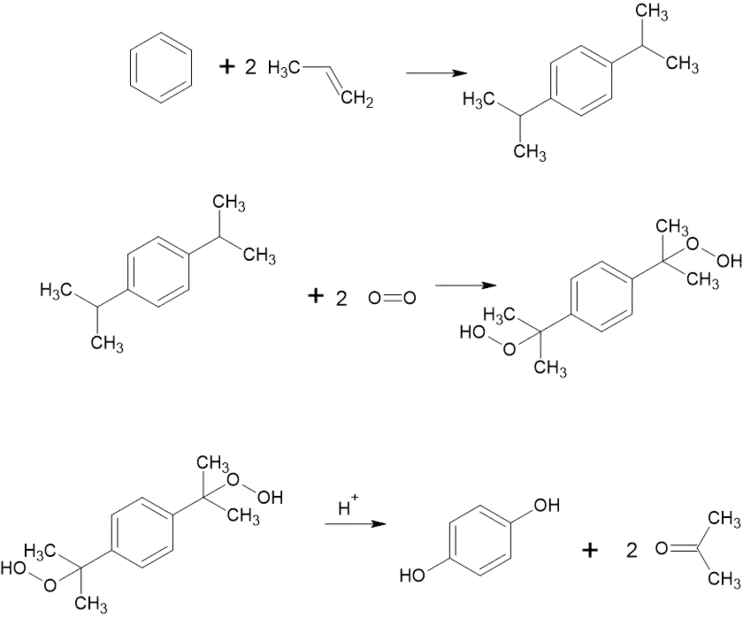
Гідроксилюванням фенолу
Гідрохінон також отримують гідроксилюванням фенолу 70% водним розчином пероксиду водню. Реакцію проводять при температурі 80 °С в присутності каталізаторів — сильних кислот, солей феруму(II) чи кобальту(II). При цьому утворюється суміш пірокатехолу та гідрохінону[2]:
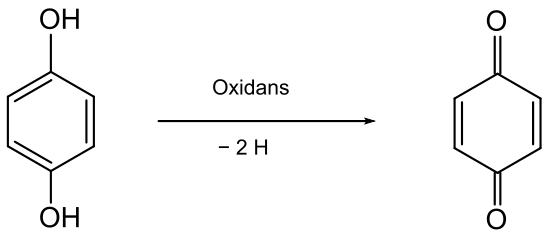
Відновлення 1,4-бензохінону
Гідрохінон утворюється також при відновленні 1,4-бензохінону, який отримують окисненням аніліну діоксидом марганцю в сульфатній кислоті при температурі 0-5 °С. Це найстаріший метод отримання гідрохінону[2]:
Інші методи
- Циклізація ацетилену з карбон монооксидом у присутності води[4]:
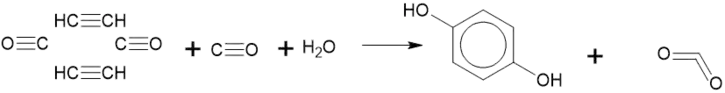
- Лужний гідроліз п-хлорофенолу[3]:
- Лужне сплавлення п-бензендисульфонової кислоти[3]:
Хімічні властивості
Проявляє слабкі кислотні властивості[3][5]. У лужному середовищі легко алкілюється, утворюючи етери[5]:
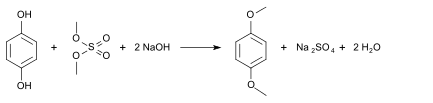
Примітки
- PubChem. Hydroquinone. pubchem.ncbi.nlm.nih.gov (англ.). Процитовано 23 вересня 2020.
- Hudnall, Phillip M. (15 червня 2000). У Wiley-VCH Verlag GmbH & Co. KGaA. Hydroquinone. Ullmann's Encyclopedia of Industrial Chemistry (англ.). Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. с. a13_499. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a13_499.
- Ластухін Ю. О., Воронов С. А. Органічна хімія : підручник. — Вид. 3-тє, стереотипне. — Львів : Центр Європи, 2006. — ISBN 966-7022-19-6.
- Pino, Piero; Braca, Giuseppe; Sbrana, Glauco (1964). Preparation of hydroquinone US3355503 A. Lonza Ag.
- Нейланд, О.Я. (1990). Органическая химия (російська). Москва: Высшая школа. с. 325-326. ISBN 5-06-001471-1.