Оксид алюмінію
Алюмі́ній окси́д (рос. алюминия оксид, англ. aluminium oxide, нім. Aluminiumoxid) — неорганічна сполука Алюмінію з Оксигеном складу Al2O3. Являє собою білі кристали, хімічно дуже стійкі, температура плавлення 2050 °C. У воді алюміній оксид не розчиняється і не взаємодіє з нею. Проявляє амфотерні властивості.
| Алюміній оксид | |
|---|---|
 структура Al2O3 | |
 | |
| Назва за IUPAC | Алюміній оксид |
| Інші назви | корунд, глінозем |
| Ідентифікатори | |
| Номер CAS | 1344-28-1 |
| Номер EINECS | 215-691-6 |
| DrugBank | 11342 |
| Назва MeSH | D01.056.050 і D01.650.550.050 |
| ChEBI | 30187 |
| RTECS | BD1200000 |
| Код ATC | D10AX04 |
| SMILES |
[O-2].[O-2].[O-2].[Al+3].[Al+3][1] |
| InChI |
InChI=1S/2Al.3O/q2*+3;3*-2 |
| Номер Гмеліна | 11099 |
| Властивості | |
| Молекулярна формула | Al2O3 |
| Густина | 3,97 г/см3 |
| Тпл | 2043 °C |
| Ткип | прибл. 3000 °C |
| Розчинність (вода) | нерозчинний |
| Розчинність (органічні розчинники) | розчинний |
| Термохімія | |
| Ст. ентальпія утворення ΔfH |
-1675,7 кДж/моль |
| Ст. ентропія S |
50,9 Дж/моль·К |
| Теплоємність, c |
79,0 Дж/моль·К |
| Пов'язані речовини | |
| Пов'язані речовини | оксид берилію |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Зустрічається у природі у вигляді мінералів корунду, рубіну, сапфіру. Сполуку застосовують для одержання алюмінію, виготовлення вогнетривів, абразивів, каталізаторів, сорбентів тощо.
Окрім оксиду Al2O3 існують також оксиди Al2O та AlO.
Поширення у природі
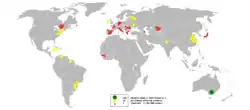
Алюміній має високу хімічну активність і тому в природі зустрічається тільки у зв'язаному стані, у формі різних мінералів і гірських порід. Близько 250 різних мінералів містять алюміній. Проте основною сировиною для виробництва глинозему є боксит (приблизно 95 % світового виробництва глинозему). Пояснюється це головним чином тим, що вміст оксиду алюмінію в промислових сортах бокситу вищий, а кремнезему нижчий, ніж в інших алюмінієвих рудах, а також нефелінів та алунітів. Запаси сировинних матеріалів у світі в цілому обмежені, а в Україні взагалі немає промислових запасів цих мінералів.
Багато видів небокситової сировини вигідно відрізняються від бокситу тим, що містять у своєму складі, крім алюміній оксиду, й інші корисні елементи, як, наприклад, натрій і калій у нефеліні, лужні метали і сірку в алуніті й ін. Тому промислова переробка цих руд на глинозем, незважаючи навіть на знижений вміст у них оксиду алюмінію, цілком доцільна і вигідна, якщо переробку вести комплексно, тобто з використанням не тільки оксиду алюмінію, але й інших складових цих руд. Таким, наприклад, є виробництво глинозему з глинистої сировини, при якому поряд із глиноземом можна одержувати соду, поташ і цемент. Особливо це актуально для Донецької області, де багато родовищ глини, у тому числі з високим вмістом Al2O3. Наприклад часів'ярська особлива глина містить до 35 % Аl2O3
Хімічні властивості
Алюміній оксид є малоактивною сполукою: не взаємодіє з водою, розведеними кислотами та лугами. Проте реагує з гарячими концентрованими кислотами й лугами, а також під час спікання, чим проявляє амфотерні властивості:
Взаємодіє також із кислотними та осно́вними оксидами:
Під дією коксу алюміній відновлюється з оксиду і переходить у солі:
При електролізі алюміній оксиду у розплаві Na3[AlF6] на катоді виділяється чистий алюміній. Це промисловий спосіб його отримання:
Отримання
Промислове виробництво
Відкритий у 1899 р. Байєром так званий гідрохімічний спосіб одержання алюміній оксиду з бокситів і донині є основним у світовій алюмінієвій промисловості. Цей спосіб досить ефективний і простий, але він може застосовуватися лише при використанні високоякісних, низькокремнистих бокситів з невеликим вмістом домішок. Світові запаси таких матеріалів обмежені. Широке поширення одержав спосіб спікання — більш коштовний, але універсальніший, сировиною для якого є боксити нижчої якості, нефеліни, алуніти, глиниста сировина, каолініти, кам'яновугільний попіл, серицити й інші алюмосилікатні породи, запаси яких практично невичерпні. Тому переробка цієї сировини способом спікання на глинозем, незважаючи навіть на знижений вміст оксиду алюмінію, цілком доцільна і вигідна, тому що крім глинозему при способі спікання утворюються побічні корисні продукти. Крім класичних способів отримання глинозему — гідрохімічного та спікання, у виробництво впроваджені й інші апаратурно-технологічні схеми виробництва глинозему:
- паралельно і послідовно комбіновані способи Байєр-спікання для переробки низькокремнистих і висококремнистих бокситів,
- спосіб спікання для переробки висококремнистих бокситів і нефелінів,
- відновно-лужний спосіб для переробки алунітів, гідролужні способи для переробки низькоякісних бокситів і нефелінів.
Одержання в лабораторії
Досліджується можливість отримати алюміній оксид способом спікання з глинистої сировини. Як об'єкт дослідження взято глину часів'ярську особливу, яка має наступний хімічний склад: 35 % Al2O3, 4 % Na2O,K2O, 50 % SiO2, 0,5 % Fe2O3 і 1 % CaO (мас. %). В лабораторних умовах на основі глини складалися суміші для спікання з карбонатною породою (крейда). Крейда вводиться в шихту згідно з молярним співвідношенням СаО:SiO2, яке дорівнює 2,0 ± 0,03. Для отримання малорозчинного кальцій ортосилікату (2CaO-SiO2). Вихідні матеріали попередньо подрібнювались, дозувалися та ретельно змішувались. Підготовану шихту спікали при 1200 °C з витримкою впродовж 30 хвилин у муфельній електричній печі. Ця стадія направлена на зв'язування оксиду кремнію й переводу алюміній оксиду до розчинної у воді сполуки. Цей процес характеризується наступною узагальненою хімічною реакцією:
Подрібнений спік для відділення алюмінатів лужних металів від решти спіку піддавали вилуговуванню. Вилуговування проводилося гарячим насиченим лужним розчином. Після вилуджування необхідно знекремнити розчин, тобто видалити кремнезем, який знаходиться у розчині, для підвищення якості глинозему. Знекремнення проводили у дві стадії. На першій стадії створюються умови для найповнішої кристалізації гідроалюмосилікату натрію. Друга стадія — це стадія глибокого знекремнення. Знекремнення проводилось довгим кип'ятінням розчину на електричній плитці.
Вилучення гідрату алюмінію здійснювалось шляхом карбонізації: протягом 5 годин за температури 80 °C крізь розчин повільно пропускався вуглекислий газ. При цьому сполуки натрію й калію, що містяться в розчині, переводяться у гідрокарбонати, що викликає випадіння гідрату алюмінію в осад. Процес відбувається за трьома такими реакціями:
На заключному етапі гідрат відфільтровувався. Попередні лабораторні дослідження показали, що можна вилучити приблизно 80 % алюміній оксиду, який міститься у глині. Необхідні подальші дослідження, які повинні бути спрямовані на оптимізацію технології, на підвищення ефективності вилучення глинозему.
Застосування
Алюміній оксид, або глинозем, є основним вихідним матеріалом для виробництва алюмінію. Крім цього, він використовується й в інших сферах народного господарства: для виробництва багатьох видів кераміки, різних сортів скла, нанесення покриттів для захисту металів від окиснення, дії агресивних середовищ і ерозійного зносу, і т. д.
Джерела
- Деркач Ф. А. Хімія. — Львів : Львівський університет, 1968. — 312 с.
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2007. — Т. 2 : Л — Р. — 670 с. — ISBN 57740-0828-2.
Посилання
- Aluminium oxide
