Ерлотиніб
Ерлотиніб (англ. Erlotinib, лат. Erlotinibum) — синтетичний лікарський препарат, який належить до групи інгібіторів тирозинкінази.[1][2][3] Застосовується перорально.[4][5][6] Ерлотиніб уперше синтезований у лабораторії американської компанії «OSI Pharmaceuticals»[7], та був схвалений FDA у 2004 році.[6] Пізніше «OSI Pharmaceuticals» передала на препарат компанії «Hoffmann-La Roche», яка разом із своїм підрозділом «Genentech» продовжила випуск препарату під торговою маркою «Тарцева».[1]
 | |
|---|---|
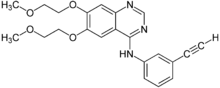
Ерлотиніб
| |
| Систематизована назва за IUPAC | |
| N-(3-ethynylphenyl)-6,7-bis(2-methoxyethoxy) quinazolin-4-amine | |
| Класифікація | |
| ATC-код | L01 |
| PubChem | |
| CAS | |
| DrugBank | |
| Хімічна структура | |
| Формула | C22H23N3O4 |
| Мол. маса | 393,436 г/моль |
| Фармакокінетика | |
| Біодоступність | 59% |
| Метаболізм | Печінка |
| Період напіввиведення | 36,2 год. |
| Екскреція | фекалії (> 90%), Нирки |
| Реєстрація лікарського засобу в Україні | |
| Назва, фірма-виробник, країна, номер реєстрації, дата | ТАРЦЕВА, «Ф.Хоффманн-Ля Рош Лтд»,Швейцарія UA/5372/01/02 21.09.2016-21/09/2021 |
Фармакологічні властивості
Ерлотиніб — синтетичний лікарський засіб, який належить до групи інгібіторів протеїнтирозинкінази. Механізм дії препарату полягає в інгібуванні ферменту тирозинкінази рецептора епідермального фактора росту людини. Це призводить до пригнічення фосфорилювання рецепторів епідермального фактору росту, наслідком чого є порушення процесів мітозу та проліферації клітин. Оскільки мітотична активність є більшою в пухлинних клітин, то ерлотиніб переважно блокує ріст та проліферацію пухлинних клітин, а також метастазування пухлини.[2][4][5] Біологічною мішенню ерлотинібу є білки SLCO2B1 та EGFR, у тому числі із мутацією рецептора епідермального фактору росту EGFR.[1][2][4] Ерлотиніб застосовується як самостійний препарат, так і в комбінації з іншими препаратами для лікування недрібноклітинного раку легень та раку підшлункової залози при місцево-розповсюдженому або метастатичному раку[4][5][6], а також при деяких формах раку молочної залози та колоректального раку.[8] Ерлотиніб у клінічних дослідженнях виявив значну ефективність при недрібноклітинному раку легень, у тому числі при неефективності хіміотерапії із застосуванням гемцитабіну та карбоплатину[2][8], а при деяких генетичних формах раку легень тривалість життя пацієнтів після виявлення пухлини зросла удвічі.[9] Незважаючи на те, що побічні ефекти при застосуванні ерлотинібу спостерігаються відносно часто[1], у переважній більшості випадків вони є легкими або помірними.[2]
Фармакокінетика
Ерлотиніб добре та відносно повільно всмоктується після перорального застосування, біодоступність препарату становить 59 %. Максимальна концентрація препарату в крові досягається протягом 4 годин після прийому препарату. Ерлотиніб майже повністю (на 95 %) зв'язується з білками плазми крові. Препарат проходить через плацентарний бар'єр, даних за виділення в грудне молоко людини немає. Ерлотиніб метаболізується у печінці, частково в пухлинних тканинах, з утворенням переважно неактивних метаболітів. Виводиться препарат переважно (на 90 %) із калом, частково із сечею у вигляді метаболітів. Період напіввиведення ерлотинібу становить 36,2 годин, цей час практично не змінюється у хворих із порушенням функції печінки або нирок.[4][5][6]
Покази до застосування
Ерлотиніб застосовують при недрібноклітинному раку легень та раку підшлункової залози.[4][5]
Побічна дія
Хоча при застосуванні ерлотинібу побічні ефекти спостерігаються відносно часто[1], у переважній більшості випадків вони є легкими або помірними.[2] Найчастішими побічними ефектами ерлотинібу є загальна слабкість, погіршення апетиту, шкірний висип, задишка, кашель, діарея[1]; іншими побічними явищами при застосуванні препарату є[4][5]:
- Алергічні реакції та з боку шкірних покривів — дерматит, алопеція, гіперпігментація шкіри, кропив'янка, підвищення потовиділення, синдром Стівенса-Джонсона, набряк Квінке, синдром Лаєлла, фотодерматоз, свербіж шкіри, гірсутизм, акне, гарячка.
- З боку травної системи — стоматит, езофагіт, нудота, блювання, диспепсія, метеоризм, біль у животі, шлунково-кишкові кровотечі, порушення функції печінки, печінкова недостатність, перфорація кишечника.
- З боку нервової системи — головний біль, неропатії, депресія, кон'юнктивіт, сухість склер, кератит, порушення росту вій, вкрай рідко — виразки рогівки або перфорація рогівки.
- З боку дихальної системи — інтерстиційне захворювання легень, пневмонія, носова кровотеча.
- Інфекційні ускладнення — сепсис, флегмона, фіброзне запалення підшкірної клітковини.
- Зміни в лабораторних аналізах — анемія, тромбоцитопенія, нейтропенія, підвищення рівня білірубіну в крові, підвищення рівня активності ферментів печінки в крові.
Протипокази
Ерлотиніб протипоказаний при підвищеній чутливості до препарату, важких порушеннях функції печінки або нирок, при вагітності та годуванні грудьми, особам віком до 18 років.[4][5]
Примітки
- FDA одобрило расширение показаний к применению препарата Тарцева (эрлотиниб) для лечения рака легкого (рос.)
- Эрлотиниб (Тарцева®) в первой линии терапии пациентов с немелкоклеточным раком легкого с мутациями EGFR: анализ эффективности (рос.)
- Противоопухолевые препараты влияющие на передачу внешнего сигнала в клетку (рос.)
- https://compendium.com.ua/dec/270271/
- https://www.vidal.ru/drugs/molecule/1688 (рос.)
- Erlotinib (англ.)
- Querida Anderson (15 червня 2007). OSI Pharma Needs to Expand Pipeline. Genetic Engineering & Biotechnology News (Mary Ann Liebert, Inc.). с. 14. Процитовано 20 січня 2008. (англ.)
- Тарцева при немелкоклеточном раке легкого (рос.)
- Лечение препаратом тарцева практически удваивает выживаемость без прогрессирования при особомгенетическом варианте немелкоклеточного рака легких Архівовано 23 листопада 2018 у Wayback Machine. (рос.)
- https://www.vidal.ru/drugs/molecule-in/1688 (рос.)