Декслансопразол
Декслансопразол — синтетичний препарат, що є похідним бензимідазолу[1], та належить до групи інгібіторів протонної помпи[2][3], що застосовується перорально.[4][3] За своїм хімічним складом є правообертовим (R-ізомером) лансопразолу.[2][4] Декслансопразол уперше синтезований у Японії у лабораторії компанії «Takeda Pharmaceutical»[5], де вперше синтезовано також лансопразол[6][7], і застосовується у клінічній практиці з 2009 року.[1][3]
 | |
|---|---|
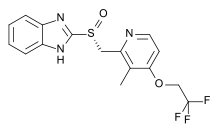
Декслансопразол
| |
| Систематизована назва за IUPAC | |
| (R)-(+)2-([3-methyl-4-(2,2,2-trifluoroethoxy)pyridin-2-yl]methylsulfinyl)-1H-benzo[d]imidazole | |
| Класифікація | |
| ATC-код | A02 |
| PubChem | |
| CAS | |
| DrugBank | |
| Хімічна структура | |
| Формула | C16H14F3N3O2S |
| Мол. маса | 369,363 г/моль |
| Фармакокінетика | |
| Біодоступність | 76% |
| Метаболізм | Печінка |
| Період напіввиведення | 1,3 год. |
| Екскреція | Нирки (51%), фекалії (47%) |
| Реєстрація лікарського засобу в Україні | |
| Назва, фірма-виробник, країна, номер реєстрації, дата | ДЕКСІЛАНТ, «Такеда Фармасьютікал Компані Лімітед»/«Такеда Ірландія Лтд»,Японія/Ірландія UA/13660/01/02 30.05.2014-30/05/2019 |
Фармакологічні властивості
Декслансопразол — синтетичний препарат, що є похідним бензимідазолу та належить до групи інгібіторів протонної помпи. За хімічним складом є R-ізомером лансопразолу. Механізм дії препарату полягає у інгібуванні ферменту парієтальних клітин шлунку H+/K+ АТФази (який також називають протонною помпою), що призводить до блокування перенесення іонів водню із парієтальних клітин у порожнину шлунку та гальмування кінцевого етапу секреції соляної кислоти.[8][2] Після введення в організм декслансопразол накопичується в каналах обкладинкових клітин шлунку, саме у просвіт яких заходять частини молекул протонної помпи, де виключно і відбувається взаємодія препарату із ферментом H+/K+ АТФазою виключно парієтальних клітин шлунку.[2][8] Декслансопразол переважає інших представників класу інгібіторів протонної помпи як по своїм фармакологічним властивостям (здатністю утримувати pH шлункового соку вище показника 4 від 16 до 24 годин), так і за рахунок новітньої технології випуску препарату — капсул із подвійним вивільненням препарату, завдяки чому забезпечується удвічі вищий період напівжиття молекул препарату в системному кровотоці, та поява другого піку максимальної концентрації декслансопразолу в крові, що також збільшує тривалість дії препарату.[4][2] Декслансопразол у меншому ступені, ніж інші препарати групи інгібіторів протонної помпи, взаємодіє із системою цитохрому Р-450, і не рекомендований до застосування лише із атазанавіром; хоча теоретично він може змінювати концентрацію в крові таких препаратів як дигоксин, кетоконазол, варфарин, ампіцилін та такролімус. При дослідженнях не було виявлено даних за біохімічну взаємодію декслансопразолу з діазепамом, теофіліном та фенітоїном.[4] Оскільки застосування декслансопразолу знижує рівень кислотності шлунку, то це призводить до стимуляції вироблення гастрину.[2] При застосуванні декслансопразолу в лікуванні ерозивного езофагіту та гастроезофагеальної рефлюксної хвороби спостерігається значно вищий ефект, ніж при застосуванні лансопразолу.[4][2] Натепер декслансопразол затверджений лише для лікування ерозивного езофагіту та гастроезофагеальної рефлюксної хвороби.[3] У 2010 році FDA випустило бюлетень із попередженням про підвищений ризик переломів стегна, зап'ястя та хребта при тривалому (більше 1 року) або при застосуванні у високих дозах препаратів із групи блокаторів протонної помпи (у тому числі декслансопразолу, а також омепразолу, пантопразолу, лансопразолу, рабепразолу та езомепразолу).[9]
Фармакокінетика
Декслансопразол повільніше, ніж інші препарати групи блокаторів протонної помпи, всмоктується при прийманні всередину, біодоступність препарату при пероральному застосуванні складає 76%. Завдяки новітній технології випуску препарату — капсул із подвійним вивільненням препарату, при пероральному прийманні декслансопразолу 25% препарату всмоктується у дванадцятипалій кишці та поступають у системний кровообіг швидше, а решта 75% препарату всмоктуються в нижчих відділах тонкої кишки та поступають у системний кровообіг пізніше. Завдяки цій особливості спостерігається два піки максимальної концентрації декслансопразолу в крові — через 1—2 години після застосування препарату та через 4—5 годин після застосування.[4][2] Хоча тривалість періоду напіввиведення декслансопразолу складає 1—2 години[8], тривалість середнього перебування молекули декслансопразолу в організмі зростає удвічі в порівнянні з молекулою класичного лансопразолу (5,5—6,0 годин проти 2,8—3,0 годин відповідно), що призводить до подовження фармакологічного ефекту препарату.[4][2] Метаболізується декслансопразол у печінці до неактивних метаболітів[4], виводиться з організму препарат переважно із сечею (майже 51%), а також із калом (47%).[10] При порушеннях функції печінки може спостерігатися збільшення періоду напіввиведення препарату.[4]
Показання до застосування
Декслансопразол натепер затверджений для застосування при ерозивному езофагіті та гастроезофагеальній рефлюксній хворобі.[11][10]
Побічна дія
При проведенні спостережень виявлено, що при застосуванні декслансопразолу побічні ефекти спостерігаються нечасто, та не мають серйозних клінічних наслідків. Найчастіше при застосуванні декслансопразолу спостерігаються діарея, нудота, блювання, біль у животі, головний біль, метеоризм, збільшення частоти інфекцій верхніх дихальних шляхів, частота яких була не вищою за 2%.[4] Також при застосуванні препарату можуть спостерігатися наступні побічні ефекти[11]:
- Алергічні реакції та з боку шкірних покривів — нечасто (0,1—1%) висипання на шкірі, свербіж шкіри, кропив'янка, кашель; рідше набряк гортані, лейкоцитокластичний васкуліт, тромбоцитопенічна пурпура, синдром Стівенса-Джонсона, синдром Лаєлла, анафілактичний шок.
- З боку травної системи — нечасто (0,1—1%) сухість у роті; рідко кандидоз ротової порожнини, гепатит, панкреатит.
- З боку нервової системи — нечасто головокружіння, безсоння, депресія, порушення смаку та апетиту; рідше порушення зору та слуху, парестезії, судоми, інсульт.
- Інші побічні ефекти — рідко гостра ниркова недостатність, збільшення частоти переломів кісток, припливи крові, артеріальна гіпертензія.
- Зміни в лабораторних аналізах — рідко спостерігаються гемолітична анемія, тромбоцитопенія, агранулоцитоз, панцитопенія, підвищення активності амінотрансфераз в крові, гіпонатріємія, гіпомагніємія.
Протипокази
Протипоказами до застосування декслансопразолу є підвищена чутливість до препарату, вагітність, годування грудьми, застосування разом із препаратами групи інгібіторів протеази. З обережністю декслансопразол застосовується при одночасному застосуванні такролімусу, варфарину, метотрексату та флувоксаміну.[11]
Форми випуску
Декслансопразол випускається у вигляді капсул із модифікованим виділенням по 0,03; 0,06; 0,09 та 0,12 г.[4]
Примітки
- http://www.mednovosti.by/journal.aspx?article=5079 (рос.)
- http://www.lvrach.ru/2015/02/15436161 (рос.)
- http://www.gastroscan.ru/handbook/144/3429 (рос.)
- http://rpht.com.ua/files/85750207.pdf%5Bнедоступне+посилання+з+липня+2019%5D (рос.)
- Takeda в Украине — начало долгой и успешной истории (рос.)
- http://www.gastroscan.ru/literature/authors/4024 (рос.)
- http://www.gastroscan.ru/literature/authors/2197 (рос.)
- http://www.gastroscan.ru/literature/authors/6497 (рос.)
- http://www.gastroscan.ru/literature/authors/3427 (рос.)
- Product Information: DEXILANT(R) delayed release oral capsules, dexlansoprazole delayed release oral capsules (англ.)
- http://www.vidal.ru/drugs/dexilant__42719 (рос.)
