Севофлуран
Севофлуран — інгаляційний анестетик, що часто використовується для ввідного наркозу через його фармакокінетичні властивості і відсутність подразнюючої дії на дихальні шляхи.[2]
 | |
|---|---|
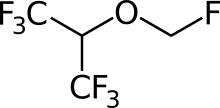
Севофлуран
| |
| Систематизована назва за IUPAC | |
| 1,1,1,3,3,3-гексафтор-2-(фторометокси)пропан | |
| Класифікація | |
| ATC-код | N01 |
| PubChem | |
| CAS | |
| DrugBank | DB01236 |
| Хімічна структура | |
| Формула | C4H3F7O |
| Мол. маса | 200,055 г/моль |
| Фармакокінетика | |
| Біодоступність | НД |
| Метаболізм | печінкою, незначний |
| Період напіввиведення | 15-23 год |
| Екскреція | легенями, із видихуваним повітрям |
| Реєстрація лікарського засобу в Україні | |
| Назва, фірма-виробник, країна, номер реєстрації, дата | СЕВОФЛУРАН, «Пірамал Крітікал Кер Інк», США UA/9979/01/01 29.12.2015 - 29.12.2020 |
| Назва, фірма-виробник, країна, номер реєстрації, дата | СЕВОРАН, «Аесіка Квінборо Лтд», Велика Британія, «Еббві С.р.л.», Італія UA/4139/01/01 29.12.2015 - 29.12.2020[1] |
Історія
Севофлуран був вперше синтезований в 1968 році Бернардом Реганом («Baxter Travenol Laboratories Inc.», штат Іллінойс; з 1988 року «Baxter International Inc.»[3]) при дослідженні ряду галометилових поліфтороізопропілових естерів. Перші дані про нього були опубліковані в 1971 році.[4] Перше клінічне випробування на добровольцях датується 1981 роком[5]; незважаючи на позитивні результати, подальші клінічні дослідження севофлурану були відстрочені з огляду на те, що в той час інший інгаляційний анестетик, ізофлуран, який перебував на третій фазі клінічних випробувань, мав більш високий комерційний потенціал зважаючи на низку причин. Серед них — нестійкість севофлурану при контакті з натронним вапном, що використовується для поглинання СО2 в апаратах ШВЛ з напівзакритим контуром[6], а також більш високий рівень його біотрансформації в порівнянні з ізофлураном.[7] «Baxter Travenol» продала права на севофлуран компанії «Anaquest» («Ohmeda» / BOC); та, в свою чергу, перепродала їх японській компанії «Maruishi». «Maruishi» продовжила дослідження, і в травні 1990 року севофлуран почав випускатися в Японії і застосовуватися в клінічній практиці.[4]
Використання в медичній практиці
Севофлуран — один з найбільш часто використовуваних інгаляційних анестетиків, в тому числі в педіатричній практиці.[6] Його дія розвивається швидко, він не подразнює дихальні шляхи, а також не має запаху, тому підходить для ввідного наркозу. Севофлуран також використовується для загальної анестезії при проведенні кесаревого розтину; безпеку його застосування при природних пологах не досліджена.[8]
Фізичні властивості
При кімнатній температурі і нормальному атмосферному тиску являє собою безбарвну летючу рідину з солодким запахом. При стандартних умовах не реагує з киснем, незаймистий, невибухонебезпечний.[9]
| Властивість | Значення[8] |
|---|---|
| Молекулярна маса | 200.05 г / моль |
| Температура кипіння (при тиску 760 мм рт. ст.) | 58,6 ⁰С |
| Мінімальна альвеолярна концентрація (МАК) | 2,05 об.% |
| Тиск пари при 20 ° C | 157 мм рт. ст. |
| Тиск пари при 25 ° C | 197 мм рт. ст. |
| Тиск пари при 36 ° C | 317 мм рт. ст. |
| Коефіцієнти розподілу при 37 ° C: | |
| Кров / газ | 0,63-0,69 |
| Вода / газ | 0,36 |
| Масло / газ | 47-54 |
| Мозок / газ | 1,15 |
Механізм дії
Точний механізм дії загальних анестетиків поки невідомий. Протягом 20 століття висувалося безліч теорій; вони будувалися на концепції про те, що всі анестетики діють за одним загальним механізмом (унітарні теорії). Провідна теорія передбачала, що ці сполуки змінюють властивості клітинних мембран, розчиняючись в них. Це припущення ґрунтується на правилі Овертон-Мейера, встановленому експериментальним шляхом. Воно свідчить, що існує прямо пропорційна залежність між коефіцієнтом розчинності масло / газ і мінімальною альвеолярною концентрацією.[9] Однак в даний час унітарні теорії втратили актуальність; домінує концепція про те, що кожен анестетик має певний набір молекулярних і рецепторних мішеней в різних відділах головного мозку.[10] Зокрема, експериментальні дані свідчать про те, що севофлуран є антагоністом NMDA-рецепторів[11], агоністом гліцинових рецепторів[12], а також пригнічує 5НТ-3 рецептори[13][14] і Н-холінорецептори.[15]
Фармакокінетика
Мінімальна альвеолярна концентрація (МАК[Примітки 1]) севофлурану знижується зі збільшенням віку пацієнта. Так, для пацієнтів віком 25-40 років вона становить 2.1 % в кисні або 1.1 % з 65 % N2O / 35 % кисню; у віці 40-60 років вона знижується до 1.7 % в кисні або 0.9 % з 65 % N2O / 35 % кисню. З огляду на низьку розчинність севофлурану в крові, МАК досягається дуже швидко. Дія настає через 2-3 хвилини.[8] Метаболізм севофлурану відбувається в печінці за участю цитохрому P450 2E1. Близько 5 % всієї дози піддається трансформації. При цьому утворюється гексафторізопропанол і іон фтору. Метаболізм севофлурану прискорюється індукторами P450 2E1 фенобарбіталом, етанолом, ізоніазидом, що може привести до підвищення концентрації неорганічного фтору в крові. Гексафторізопропанол потім піддається кон'югації з глюкуроновою кислотою і виводиться з сечею. Аніон фтору також виводиться з сечею; близько 50 % фтору, що утворився, захоплюється кістковою тканиною.[8]
Токсичність
Сполука А
Севофлуран може піддаватися розпаду при контакті з основними адсорбентами СО2 (зокрема, натронним вапном). При цьому він втрачає HF, перетворюючись в пентафторізопропенілфторметіловий ефір — сполуку А; утворюється також незначна кількість сполуки В -пентафторометоксіізопропілфторметілового ефіру. Інтенсивність розпаду севофлурана залежить від температури: чим вона вища, тим вище рівень розпаду. Подальше дефторування призводить до утворення сполук C, D і E.[16] В експериментах на щурах було показано значна нефротоксичність з'єднання А (і в меншій мірі з'єднання В). Дослідження на добровольцях і хірургічних пацієнтах показали, що за тривалої анестезії севофлураном (близько 8 годин) і низької інтенсивності подачі досягалася значна концентрація сполуки А в крові, а в сечі виявлялося тимчасове підвищення біохімічних маркерів пошкодження нирок. Однак клінічні дані, отримані за менш тривалої анестезії і більш високої інтенсивності подачі показали безпеку севофлурану щодо пошкодження нирок.[17] Метаболізм з'єднання А у щурів залучає кон'югування з глутатіоном і цистеїном, що може пояснювати різницю в дії сполуки А на нирки щурів і людини.[18]
Вплив на нервову систему
Севофлуран, як і інші препарати для загальної анестезії, може володіти нейротоксічностю і негативно позначатися на розвитку нервової системи при застосуванні у дітей.[19] Дослідження на мишах виявили нейротоксичний ефект, що прямо залежить від дози і часу впливу анестетика.[20] У мишей вплив севофлурану індукує апоптоз нейронів гіпокампу, пригнічує нейрогенез і негативно впливає на процеси навчання і довготривалу пам'ять[21][22], проте в експериментах на макаках не було виявлено токсичних ефектів цього препарату.[23]
Побічні ефекти
Застосування севофлурану в фазі індукції може викликати такі побічні ефекти, як брадикардія, гіпотензія, ларингоспазм і обструкція дихальних шляхів. Під час фази підтримки і в післяопераційний період можуть спостерігатися гіпотонія, підвищення або зниження частоти серцевих скорочень, сонливість, запаморочення, нудота, блювота, кашель.[8] У людей з генетичною схильністю під впливом севофлурану може виникнути злоякісна гіпертермія — гіперметаболичний розлад, що маніфестує раптовим підвищенням температури тіла, рабдоміолізом, тахікардією, ацидозом і гіперкаліємією.[24]
Протипоказання
Севофлуран не може застосовуватися у пацієнтів з відомою гіперчутливістю до севофлурану або іншого галогенованого інгаляційного анестетика, а також з відомою або можливою схильністю до злоякісної гіпертермії.[8]
Примітки
- МАК — така альвеолярна концентрація анестетика, яка забезпечує відсутність реакції на стандартний хірургічний стимул (розріз шкіри) у 50 % хворих при тиску 760 мм рт. ст.
Джерела
- Державний реєстр лікарських засобів України
- Vacanti, Charles A.; Sikka, Pankaj K.; Urman, Richard D.; Dershwitz, Mark; Segal, B. Scott, ред. (2011). Essential Clinical Anesthesia. NY, USA: Cambridge University Press. с. 214-216. ISBN 9780521720205.
- Wilson, Mark R. (2005). Baxter Travenol Laboratories Inc.. The Electronic Encyclopedia of Chicago. Процитовано 02 січня 2017.
- Smith, I.; Nathanson, M.; White, P.F. (1996). Sevoflurane - a long-awaited volatile anaesthetic. British Journal of Anaesthesia 76 (3): 435–445.
- Holaday, D.A.; Smith, F.R. (1981). Clinical characteristics and biotransformation of sevoflurane in healthy human volunteers.. Anesthesiology 54 (2): 100–106.
- Barash, J. Paul G.; Cullen, Bruce F.; Stoelting, Robert K. (2013). Clinical Anesthesia. United States: Lippincott Williams & Wilkins. с. 448-460, 672. ISBN 0781757452.
- Brown, Burnell R.; Frink, Edward J. (1992). Whatever happened to sevoflurane?. Canadian Journal of Anaesthesia 39 (2): 207–209.
- FDA Professional Drug Information on Sevoflurane. Drugs.com. Процитовано 02 січня 2017.
- Brunton, Laurence L.; Chabner, Bruce A.; Knollmann, Björn C. (2011). Goodman & Gilman's The Pharmacological Basis of Therapeutics. New York, United States: McGraw-Hill. с. 540-548. ISBN 9780071624428.
- Frank, N.P. (2006). Molecular targets underlying general anaesthesia.. British Journal of Pharmacology 147: S72–S81. doi:10.1038/sj.bjp.0706441.
- Bronsan, Robert J.; Thiesen, R. (2012). Increased NMDA receptor inhibition at an increased Sevoflurane MAC.. BMC Anesthesiology 12 (9). doi:10.1186/1471-2253-12-9.
- Eckle, V.S.; et al. (2013). Opposing actions of sevoflurane on GABAergic and glycinergic synaptic inhibition in the spinal ventral horn.. PLoS One 8 (4). doi:10.1371/journal.pone.0060286.
- Hang, L.H.; et al. (2010). Opposing actions of sevoflurane on GABAergic and glycinergic synaptic inhibition in the spinal ventral horn.. Pharmacologocal Reports 62 (4): 621–626.
- Suzuki, T.; et al. (2002). The diverse actions of volatile and gaseous anesthetics on human-cloned 5-hydroxytryptamine3 receptors expressed in Xenopus oocytes.. Anesthesiology 96 (3): 699–709.
- Yan, S.; Dai, T.J.; Zeng, Y.M. (2009). Nicotinic acetylcholine receptors mediate the hypnotic and analgesic effects of emulsified inhalation anesthetics.. Fundamental Clinical Pharmacology 23 (2): 235–240. doi:10.1111/j.1472-8206.2008.00657.x.
- Cunningham, D.D.; Webster, J.; Mayoral, J.; Grabenkort, R.W. (1996). Sevoflurane degradation to compound A in anaesthesia breathing systems.. British Journal of Anaesthesia 118 (1): 537–543. doi:10.1093/bja/77.4.537.
- Gentz, B.A.; Malan, T.P. Jr. (2002). Renal toxicity with sevoflurane: a storm in a teacup?. British Journal of Anaesthesia 61 (15): 2155–2162.
- Kharasch, E.D. (1998). Compound A: toxicology and clinical relevance. Anaesthesiology 47: S7–10.
- Jevtovic-Todorovic, V.; et al. (2015). Anaesthetic neurotoxicity and neuroplasticity: an expert group report and statement based on the BJA Salzburg Seminar.. British Journal of Anaesthesia 111 (2): 143–151. doi:10.1093/bja/aet177.
- Xiao, H.; et al. (2016). Learning, memory and synaptic plasticity in hippocampus in rats exposed to sevoflurane.. International Journal of Developmental Neuroscience 48: 38–49. doi:10.1016/j.ijdevneu.2015.11.001.
- Chung, W.; et al. (2015). Sevoflurane exposure during the neonatal period induces long-term memory impairment but not autism-like behaviors.. Paediatric Anaesthesia 25 (10): 1033–1045. doi:10.1016/j.ijdevneu.2015.11.001.
- Song, Q.; et al. (2015). Sevoflurane induces neurotoxicity in young mice through FAS/FASL signaling.. Genetics and Molecular Research 14 (4): 18059–18068. doi:10.4238/2015.December.22.32.
- Zhou, L.; et al. (2015). Neonatal exposure to sevoflurane may not cause learning and memory deficits and behavioral abnormality in the childhood of Cynomolgus monkeys.. Scientific Reports 5: 11145. doi:10.1038/srep11145.
- Rosenberg, Н.; et al. (2015). Malignant hyperthermia: a review.. Orphanet Journal of Rare Diseases 10 (93). doi:10.1186/s13023-015-0310-1.
