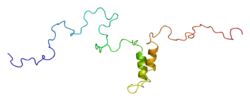GJA1
GJA1 (англ. Gap junction protein alpha 1) – білок, який кодується однойменним геном, член сімейства коннексинів.
Коннексин 43 є компонентом щілинних контактів, які складаються з масивів міжклітинних каналів, що забезпечують шлях дифузії низькомолекулярних речовин з клітини до клітини. GJA1 є основним білком щілинних контактів у серці, які, як вважають, відіграють вирішальну роль у синхронному скороченні серця та ембріональному розвитку. Мутації в цьому гені пов'язані з окуло-денто-дигітальною дисплазією, серцевими вадами розвитку, синдромом Халлерманна-Штрайффа[5].
Структура
Ген GJA1 є членом сімейства коннексинів. Розташований у людей на короткому плечі 6 хромосоми. Довжина - 14,168 пар основ. Ген містить два екзони та один інтрон. Відповідний псевдоген без інтрону знаходиться на 5-тій хромосомі [5].
Коннексин – 43 – це білок, довжина якого становить 382 амінокислот, а молекулярна маса — 43 008 кДа.[6] Кодований геном білок за функцією належить до фосфопротеїнів. Локалізований у клітинній мембрані, клітинних контактах, ендоплазматичному ретикулумі.
Cx43 складається з внутрішньоклітинного N-кінця, чотирьох трансмембранних доменів, двох позаклітинних петель, однієї цитоплазматичної петлі та внутрішньоклітинного C-кінця.[7]
Трансмембранні домени шести коннексинів можуть формувати гексамер – коннексон – спеціалізовану внутрішньоклітинну структуру, що оточує пору(напівканал). Дві позаклітинні петлі формують дисульфідні зв’язки, які взаємодіють з двома гексамерами у мембранах сусідніх клітин для правильного стикування та формування завершеного щілинного контакту[7]. Внутрішньоклітинна петля, як вважають, бере участь в регуляції проникності каналу[8].
Домен N-кінця бере участь у воротному механізмі каналів та олігомеризації і таким чином може контролювати переключення між відкритим та закритим станом каналу.
Хвіст С-кінця складається з 50-ти амінокислот і включає в себе сайти посттрансляційної модифікації та сайти зв’язування факторів транскрипції, елементів цитоскелета, та інших білків.[7][8] Як результат, хвіст С-кінця є дуже важливим для формування каналу та забезпечення таких функцій як pH–залежне регулювання зворотного механізму (канали закриваються при окисленні внутрішньоклітинного простору[9]). Регіон ДНК GJA1 гену, що кодує хвіст С- кінця, є високо консервативним, що вказує на високу стійкість до мутацій та на їх летальність, якщо вони все-таки відбуваються.
Функція
Cx43 найбільш широко експресується серед сімейства коннексинів і виявляється у більшості типів клітин. Є основним білком щілинних контактів у серці, які, як вважають, відіграють вирішальну роль у синхронному скороченні серця.
Щільні контакти складаються з кластерів тісно упакованих пар трансмембранних каналів, коннексонів, які дозволяють пасивну дифузію молекул до 1 кДа, включаючи поживні речовини, метаболіти (глюкозу), іони (К +, Са2 +) та вторинні посередники (IP3, цАМФ).
Білок діє як негативний регулятор функціональної здатності сечового міхура: діє шляхом посилення міжклітинної електричної та хімічної передачі, таким чином підвищуючи чутливість м'язів сечового міхура до холінергічних нервових стимулів і змушуючи їх скорочуватись[10].
Коннексин 43 виконує також функції, які не пов'язані з формуванням каналу та не потребують обміну молекулами між сусідніми клітинами чи між цитозолем та позаклітинним простором. Cx43 бере участь в ембріональному розвитку: експресується в точках контакту між радіальними волокнами глії та мігруючими нейронами, супресія експресії порушує процес міграції нейронів до коркової пластинки. В цьому випадку щілинні контакти забезпечують адгезивні контакти. Адгезивні контакти через взаємодію з внутрішнім цитоскелетом мігруючого нейрону, забезпечують його стабілізацію вздовж радіальних волокон, а також подальшу транслокацію ядра[11].
Клінічне значення
Хвороби, пов'язані з GJA1, включають Окуло-денто-дигітальну дисплазію(ОДДД) та Синдактити ІІІ типу. Відповідно до розташування гену Cx43, локус ОДДД був віднесений до хромосоми 6q22-q24
ОДДД - це, перш за все, аутосомно-домінантне захворювання людини, з такими симптомами як вроджені черепно-лицеві деформації, аномалії зубів і очей і деформації кінцівок На сьогоднішній день існує 73 відомі мутації Cx43, пов'язані з ОДДД, що призводять до мутаційної зміни в перших двох третіх амінокислотної послідовності Cx43 [10].
Роль в серцево-судинних захворюваннях. Cx43 у складі щілинних контактів бере участь в патологічному процесі ішемії-реперфузії через розповсюдження сигналів клітинної смерті та гіперскорочень. Негомогенні зміни в електричній провідності серед ішемічної тканини міокарду відіграють центральну роль у генезисі потенційно смертельних шлуночкових аритмій [12]. Напівканали Cx43 призводять до набухання кардіоміоцитів під час ішемії [13].
Проте нещодавно було показано, що коннексин 43 грає захисну роль в ішемічному прекондиціонуванні. Коннексин 43 локалізується в мітохондріях кардіоміоцитів та модулює мітохондріальну генерацію активних форм кисню, що грають ключову роль в прекондиційній сигналізації. З процесом старіння кількість коннексинів знижується, що може спричиняти втрату захисного ефекту. З’ясування ролі Сх43 в мітохондріях допоможе в подальшій розробці стратегій, спрямованих на обмеження клітинної смерті і дисфункції при різних патологічних станах [14].
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MGDWSALGKL | LDKVQAYSTA | GGKVWLSVLF | IFRILLLGTA | VESAWGDEQS | ||||
| AFRCNTQQPG | CENVCYDKSF | PISHVRFWVL | QIIFVSVPTL | LYLAHVFYVM | ||||
| RKEEKLNKKE | EELKVAQTDG | VNVDMHLKQI | EIKKFKYGIE | EHGKVKMRGG | ||||
| LLRTYIISIL | FKSIFEVAFL | LIQWYIYGFS | LSAVYTCKRD | PCPHQVDCFL | ||||
| SRPTEKTIFI | IFMLVVSLVS | LALNIIELFY | VFFKGVKDRV | KGKSDPYHAT | ||||
| SGALSPAKDC | GSQKYAYFNG | CSSPTAPLSP | MSPPGYKLVT | GDRNNSSCRN | ||||
| YNKQASEQNW | ANYSAEQNRM | GQAGSTISNS | HAQPFDFPDD | NQNSKKLAAG | ||||
| HELQPLAIVD | QRPSSRASSR | ASSRPRPDDL | EI |
Література
- Fishman G.I., Spray D.C., Leinwand L.A. (1990). Molecular characterization and functional expression of the human cardiac gap junction channel.. J. Cell Biol. 111: 589 — 598. PubMed DOI:10.1083/jcb.111.2.589
- Fishman G.I., Eddy R.L., Shows T.B., Rosenthal L., Leinwand L.A. (1991). The human connexin gene family of gap junction proteins: distinct chromosomal locations but similar structures.. Genomics 10: 250 — 256. PubMed DOI:10.1016/0888-7543(91)90507-B
- Haefliger J.-A., Goy J.J., Waeber G. (1999). Sporadic cases of dilated cardiomyopathies associated with atrioventricular conduction defects are not linked to mutation within the connexins 40 and 43 genes.. Eur. Heart J. 20: 1843 — 1843. PubMed DOI:10.1053/euhj.1999.1718
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC).. Genome Res. 14: 2121 — 2127. 2004. PubMed DOI:10.1101/gr.2596504
- Fu C.T., Bechberger J.F., Ozog M.A., Perbal B., Naus C.C. (2004). CCN3 (NOV) interacts with connexin43 in C6 glioma cells: possible mechanism of connexin-mediated growth suppression.. J. Biol. Chem. 279: 36943 — 36950. PubMed DOI:10.1074/jbc.M403952200
- Saffitz J.E., Laing J.G., Yamada K.A. (2000). Connexin expression and turnover: implications for cardiac excitability.. Circ. Res. 86: 723 — 728. PubMed DOI:10.1161/01.RES.86.7.723
Примітки
- Захворювання, генетично пов'язані з GJA1 переглянути/редагувати посилання на ВікіДаних.
- Сполуки, які фізично взаємодіють з Gap junction protein alpha 1 переглянути/редагувати посилання на ВікіДаних.
- Human PubMed Reference:.
- Mouse PubMed Reference:.
- Entrez Gene: GJA1 gap junction protein, alpha 1, 43kDa.
- Protein sequence of human GJA1 (Uniprot ID: P17302). Cardiac Organellar Protein Atlas Knowledgebase (COPaKB). Архів оригіналу за 5 жовтня 2015. Процитовано 18 вересня 2015.
- Laird DW (Apr 2014). Syndromic and non-syndromic disease-linked Cx43 mutations. FEBS Letters 588 (8): 1339–48. PMID 24434540. doi:10.1016/j.febslet.2013.12.022.
- Kameritsch P, Pogoda K, Pohl U (Aug 2012). Channel-independent influence of connexin 43 on cell migration. Biochimica et Biophysica Acta 1818 (8): 1993–2001. PMID 22155212. doi:10.1016/j.bbamem.2011.11.016.
- Ek-Vitorín J, Calero G, Morley GE, Coombs W, Taffet SM, Delmar M. (1996 Sep). PH regulation of connexin43: molecular analysis of the gating particle.. Biophys J. 71 (3): 1273–84. PMID 8874002. doi:10.1016/S0006-3495(96)79328-1.
- GeneCards: GJA1 gene.
- Elias LA1, Wang DD, Kriegstein AR (2007 Aug). Gap junction adhesion is necessary for radial migration in the neocortex. Nature 448 (7156): 901–7. PMID 17713529. doi:10.1038/nature06063.
- Cascio WE1, Johnson TA, Gettes LS (1995 Nov). Electrophysiologic changes in ischemic ventricular myocardium: I. Influence of ionic, metabolic, and energetic changes.. J Cardiovasc Electrophysiol 6 (11): 1039–62. PMID 17516165. doi:10.1007/s10741-007-9032-3.
- Schulz R1, Boengler K, Totzeck A, Luo Y, Garcia-Dorado D, Heusch G. (2007 Dec). Connexin 43 in ischemic pre- and postconditioning. Heart Fail Rev. 12 (3-4): 261–6. PMID 17516165. doi:10.1007/s10741-007-9032-3.
- Ruiz-Meana M, Rodríguez-Sinovas A, Cabestrero A, Boengler K, Heusch G, Garcia-Dorado D. (2008 Jan 15). Mitochondrial connexin43 as a new player in the pathophysiology of myocardial ischaemia-reperfusion injury. Cardiovasc Res. 77 (2): 325–33. PMID 18006437. doi:10.1093/cvr/cvm062.