Газ
Газ (нід. gas, від грец. chaos — хаос) — один із агрегатних станів речовини, для якого характерні великі відстані між частинками (молекулами, атомами, іонами) порівняно з твердим чи рідинним станами, слабка міжмолекулярна взаємодія, невпорядкованість структури, а середня кінетична енергія хаотичного руху частинок набагато більша за енергію взаємодії між ними.
Сутність
Характеристичною властивістю газу є те, що він здатний вільно поширюватися в усьому доступному для нього просторі[1], рівномірно заповнюючи його. На відміну від рідини та твердого тіла газ не утворює поверхні.
Газами називають хімічні речовини, які перебувають в газоподібному стані за нормальних умов. У фізичних, термодинамічних та інших дослідженнях до газів відносять також суміші газів, серед яких найбільший інтерес викликає повітря. Повітря складається з кількох газів — азоту, кисню, аргону, діоксиду вуглецю, та інших.
Етимологія назви
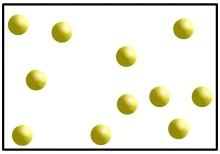
Термін «газ» (нід. gas) є неологізмом і вперше використаний на початку 17-го столітті фламандським хіміком Ян Баптист ван Гельмонтом. Він застосував це слово, мабуть, як спрощену фонетичну транскрипцію грецького слова «Хаос» (грец. chaos) — «g» в голландській вимові звучить як українська літера «х» і в цьому випадку Ван Гельмонт просто застосував установлений у використанні серед алхіміків термін, що вперше з'явився в працях Парацельса. Відповідно до термінології Парацельса «хаос» означало щось на кшталт «дуже розріджена вода»[2].
Фізичні властивості та характеристики
Макроскопічні характеристики
Оскільки більшість газів складно або неможливо спостерігати безпосередньо нашими органами чуттів, вони описуються за допомогою чотирьох фізичних властивостей або макроскопічних характеристик: тиском, об'ємом, кількістю часток (хіміки, згрупували їх у моль (одиниця)) і температури. Ці чотири характеристики здавна неодноразово досліджувались вченими, такими як Роберт Бойль, Жак Шарль, Джон Дальтон, Джозеф Гей-Люссак та Амедео Авогадро для різних газів в різних умовах. Їхнє детальне вивчення в підсумку, призвело до встановлення математичного зв'язку між цими властивостями, вираженого у рівнянні стану ідеального газу (див. нижче розділ «Спрощені моделі газу»).
Основною особливістю газу є те, що він заповнює весь доступний простір, не утворюючи поверхні. Гази завжди змішуються. Газ — ізотропна речовина, тобто його властивості не залежать від напрямку. За відсутності сил тяжіння тиск у всіх точках газу однаковий (див. Закон Паскаля).
У полі сил тяжіння густина й тиск не однакові в кожній точці, зменшуючись із висотою за барометричною формулою. Відповідно, в полі сил тяжіння неоднорідною стає суміш газів. Важчі гази мають тенденцію осідати нижче, а легші — підніматися вгору. В полі тяжіння на будь-яке тіло в газі діє Архімедова сила, яку використовують повітряні кулі, заповнені легкими газами або гарячим повітрям.
Газ має високу стисливість — при збільшенні тиску зростає його густина. При зростанні температури розширюються. При стискуванні газ може перейти в рідину, але конденсація відбувається не за будь-якої температури, а за температури, нижчій за критичну температуру. Критична температура є характеристикою конкретного газу й залежить від сил взаємодії між його молекулами. Так, наприклад, газ гелій можна зрідити тільки за температури, нижчій від 4,2 К.
Існують гази, які при охолодженні переходять у тверде тіло, оминаючи рідку фазу. Перетворення рідини в газ називається випаровуванням, а безпосереднє перетворення твердого тіла в газ — сублімацією.
Співіснування з рідиною
В певному діапазоні температури й тиску газова та рідка фаза однієї й тієї ж речовини можуть співіснувати. Частина молекул газу переходить в рідину, яка має більшу густину, отже густина газу над поверхнею рідини може залишатися нижчою. Газ над поверхнею рідини називають парою.
Мікроскопічні характеристики
Якби можна було спостерігати газ під потужним мікроскопом, можна побачити набір частинок (молекул, атомів, іонів, електронів і т. д.) без певної форми та об'єму, які знаходяться у хаотичному русі. Ці нейтральні частинки газу змінюють напрямок тільки тоді, коли вони стикаються з іншими частками або стінками ємності. Якщо припустити, що ці взаємодії (удари) абсолютно пружні, ця речовина перетворюється з реального до ідеального газу. Ця частка з мікроскопічної точки зору газу описується молекулярно-кінетичною теорією. Всі передумови, що лежать у цій теорії можна знайти в розділі «Основні постулати» кінетичної теорії.
Тепловий рух молекул газу
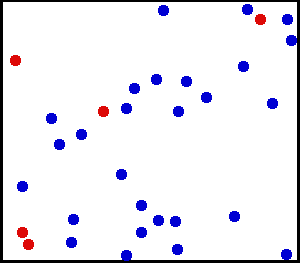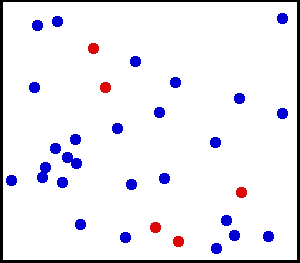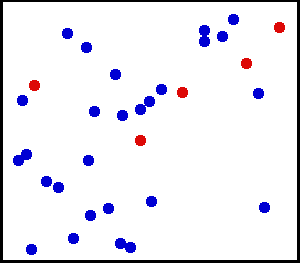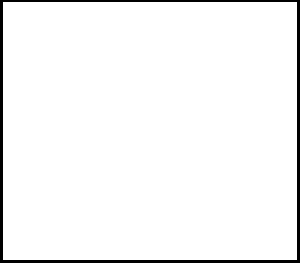
Найважливішою рисою теплового руху молекул газу — це безладність (хаотичність) руху. Експериментальним доказом безперервного характеру руху молекул є дифузія і броунівський рух.
Дифузія — це явище самовільного проникнення молекул однієї речовини в іншу. У результаті взаємної дифузії речовин відбувається поступове вирівнювання їх концентрації у всіх областях займаного ними об'єму. Встановлено, що швидкість протікання процесу дифузії залежить від роду речовин, що дифундують і температури.
Одним з найцікавіших явищ, які підтверджують хаотичність руху молекул, є броунівський рух, котрий проявляється у вигляді теплового руху мікроскопічних часток речовини, що знаходяться в завислому стані у газі. Це явище у 1827 році вперше спостерігав[3] Р. Браун, від імені якого воно отримало назву. Безладність переміщення таких частинок пояснюється випадковим характером передачі імпульсів від молекул газу до частки з різних сторін. Броунівський рух виявляється тим помітніше, чим менші частки і чим вища температура системи. Залежність від температури свідчить про те, що швидкість хаотичного руху молекул зростає зі збільшенням температури, саме тому його і називають тепловим рухом.
Закон Авогадро
Закон Авогадро — однакові об'єми будь-яких газів при однаковому тиску і температурі містять однакову кількість молекул.
Цей закон був відкритий на основі дослідів з хімії італійським вченим Амедео Авогадро (1776—1856) в 1811 році. Закон стосується мало стиснених газів, (наприклад, газів під атмосферним тиском). У разі сильно стиснених газів вважати його справедливим не можна. Закон Авогадро означає, що тиск газу при визначеній температурі залежить тільки від числа молекул в одиниці об'єму газу, але не залежить від того, які це молекули.
Кількість речовини, що містить число грамів, рівне його молекулярній масі, називається грам-молекулою або молем. Зі сказаного випливає, що молі різних речовин містять однакове число молекул. Число молекул в одному молі речовини, що отримало назву «стала (число) Авогадро», є важливою фізичною величиною. За ДСТУ 3651.2-97[4] значення сталої Авогадро приймається:
- NA = 6,0221367·1023 ± 0,0000036·1023 моль−1
Стала Авогадро За даними CODATA-2010[5] дорівнює
- NA = 6,02214129·1023 ± 0,00000027·1023 моль−1
Для визначення сталої Авогадро були зроблені численні та різноманітні дослідження (броунівського руху, явищ електролізу та ін.), що привели до досить узгоджених результатів і є яскравим свідченням реальності молекул і молекулярної будови речовини.
Кінетична теорія
Кінетична теорія дає уявлення про макроскопічні властивості газів, розглядаючи їх молекулярну будову і рух молекул. Починаючи з визначення імпульсу і кінетичної енергії,[6] можна використовуючи закон збереження імпульсу і геометричні залежності зв'язати макроскопічні властивості системи (температуру і тиск) з мікроскопічними властивостями (кінетичною енергію однієї молекули).
Кінетична теорія пояснює термодинамічні явища, виходячи з атомістських уявлень. Теорія постулює, що тепло є наслідком хаотичного руху надзвичайно великої кількості мікроскопічних частинок (атомів та молекул). Теорія пояснює, як газова система реагує на зовнішні впливи. Наприклад, коли газ нагрівається від абсолютного нуля, коли його частинки (теоретично) абсолютно нерухомі, швидкість частинок зростає зі зростанням його температури. Це призводить до більшого числа зіткнень зі стінками ємності кожну секунду за рахунок вищої швидкості частинок, пов'язаної з підвищеними температурами. У міру зростання числа зіткнень (за одиницю часу) зростає вплив на поверхню стінки ємності, тиск зростає пропорційно.
Успішне пояснення багатьох законів термодинаміки, виходячи з положень кінетичної теорії, стало одним із факторів підтвердження атомарної будови речовин у природі. В сучасній фізиці молекулярно-кінетична теорія розглядається як складова частина статистичної механіки.
Електричний струм у газах
Загалом гази не проводять електричний струм або мають дуже низьку електропровідність, оскільки їхні молекули нейтральні, проте якщо частина атомів газу йонізується, він стає здатним до проводження електричного струму. В газах також можливі газові розряди або при іонізації зовнішнім джерелом, або внаслідок ударної іонізації в самому розряді.
Один із видів йонізації газів — термічна йонізація. При цьому атоми газу йонізуються за рахунок зіткнень між атомами внаслідок підвищення температури — атоми набувають кінетичної енергії, достатньої для звільнення електрона від атома. Проте температури, за яких атоми газів набувають достатньої кінетичної енергії, високі (наприклад, для водню це значення 6 000 К).
Другий вид йонізації газів — йонізація електричним ударом. Дана йонізація відбувається і при низьких температурах внаслідок перевищення напруженості електричного поля в газі певного значення, що зумовлює вихід електрона з атома. Іноді виникають також самостійні електричні розряди, що зумовлюється зіткненням фотонів або позитивних йонів з катодом і ланцюгове повторення реакції, в процесі чого також відбувається збудження атомів газу. Прикладом самостійного електричного розряду є блискавка. Гази, молекули яких за йонізації перетворюються на суміш йонів та електронів, називаються плазмою.
При нагріванні катода електричним розрядом з великою силою струму відбувається його нагрівання до міри термоелектронної емісії електронів з нього (дуговий розряд).
Теплоємність та теплопровідність
Питома теплоємність газу сильно залежить від характеру процесу, що відбувається у ньому. Найчастіше використовуються ізобарна та ізохорна теплоємності; для ідеального газу .
Теплопровідність газів — явище направленого переносу теплової енергії за рахунок зіткнень молекул газу без переносу речовини.
В'язкість газів
На відміну від рідин, кінематична в'язкість газів з ростом температури зростає, хоча для динамічної в'язкості ця залежність не є так вираженою. Також в'язкість зростає із зростанням тиску.
Процеси переносу
Для газу характерні високий коефіцієнт самодифузії.
Гази мають невисоку теплопровідність, оскільки передача енергії від молекули до молекули відбувається за рахунок нечастих зіткнень. Цим пояснюються добрі теплоізоляційні властивості вовни й вати, матеріалів, в яких більшість об'єму заповнене повітрям. Але в газах діє інший механізм передачі тепла — конвекція.
Спрощені моделі газу
Під рівнянням стану (для газів) мають на увазі математичну модель, що використовується для наближеного опису чи моделювання властивостей газу. В наш час[коли?] не існує єдиного рівняння стану, яке б точно прогнозувало властивості всіх газів при будь-яких умовах. Тому було розроблено велике число набагато точніших рівнянь стану для конкретних газів в діапазоні певних температур і тисків. Математичні моделі газу, що найчастіше використовуються — це моделі «ідеального газу» та «реального газу».
Ідеальний газ
Ідеальний газ — це газ, в якому молекули можна вважати матеріальними точками, а силами притягання й відштовхування між молекулами можна знехтувати. У природі такого газу не існує, але близькими за властивостями до ідеального газу є реальні розріджені гази, тиск в яких не перевищує 200 атмосфер і які перебувають в не дуже низькій температурі, оскільки за таких умов відстань між молекулами набагато перевищує їх розміри. З позиції класичної термодинаміки ідеальними газами називають гіпотетичні (реально не існуючі) гази, які строго підкоряються термічному рівнянню стану Клапейрона. [7][8][9].
Розрізняють три типи ідеального газу:
Термодинамічні властивості ідеального газу можна описати такими двома рівняннями: Стан класичного ідеального газу описується рівнянням стану ідеального газу Клапейрона:
- ,
яке у формі об'єднаного газового закону має вигляд:
- ,
звідки випливають закони Бойля—Маріотта, Шарля і Гей—Люссака:
- — закон Гей-Люссака
- — закон Шарля (другий закон Гей-Люссака)
- — закон Бойля-Маріотта
Внутрішня енергія ідеального газу описується наступним рівнянням:
де є константою (рівною, наприклад, 3/2 для одноатомного газу) і
- U — внутрішня енергія (вим. у джоулях)
- P — тиск (паскаль)
- V — об'єм (метр кубічний)
- n — кількість речовини (моль)
- R — універсальна газова стала (джоуль на моль на градус Кельвіна)
- T — абсолютна температура (градуси Кельвіна)
- N — кількість молекул
- k — стала Больцмана (джоуль на градус Кельвіна на молекулу)
Реальний газ
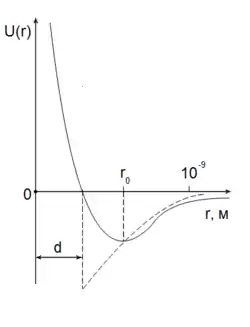
Реальний газ — це газ, між молекулами якого діють сили міжмолекулярної взаємодії.
Досвід показав, що закони ідеальних газів (Бойля-Маріотта, Гей-Люссака, Шарля, об'єднаний газовий закон) справедливі для реальних газів лише за умов, близьких до нормальних. У разі підвищення тиску і зниження температури виявляються значні відхилення у поведінці всіх реальних газів. Реальний газ має стискуваність від зовнішніх сил значно меншу, ніж ідеальний. Реальні гази конденсуються, а рівняння стану ідеального газу не може пояснити перехід речовини з газоподібного стану в рідкий.
Сили міжмолекулярної взаємодії — короткодіючі, тобто проявляються на відстанях r ≤ 10−9 м і швидко зменшуються із збільшенням віддалі.
Сили міжмолекулярної взаємодії залежно від віддалі між молекулами можуть бути силами притягання або силами відштовхування. Молекулярні сили притягання називають силами Ван дер Ваальса (Йоганнес Ван дер Ваальс — нідерландський фізик). Із рисунка видно, що для великих відстаней між молекулами, коли густина газу мала, сили Ван дер Ваальса правильно передають характер взаємодії між молекулами. Частині кривої, яка відповідає міжмолекулярному відштовхуванню, у моделі Ван дер Ваальса відповідає додатна частина кривої. На цій ділянці U(r)→ ∞ при r ≤ d, тобто центри молекул не можуть наблизитись на відстань r < d (d — діаметр молекули). Загалом, зображена пунктиром крива подає потенціальну енергію парної взаємодії молекул, між якими діють сили притягання, а сили відштовхування проявляються лише у разі зіткнення згідно з моделлю твердих кульок.
У 1873 році Ван дер Ваальс, проаналізувавши причини відхилення властивостей реальних газів від закону Бойля-Маріотта, вивів рівняння стану реального газу, в якому було враховано власний об'єм молекул і сили взаємодії між ними. Аналітичний вираз рівняння Ван дер Ваальса для одного моля газу має вигляд:
- ,
де коефіцієнти а і b називають сталими Ван дер Ваальса, які залежать від хімічної природи речовини, температури і тиску.
Рівняння Ван дер Ваальса для довільної кількості газу масою m має вигляд:
Рівняння Ван дер Ваальса є наближеним рівнянням стану реального газу, причому ступінь його наближення різний для різних газів. Записана велика кількість емпіричних і напівемпіричних рівнянь стану реальних газів (рівняння: Бертло[10], Клаузіуса — Клапейрона, Дітерічі[11], Редліха — Квонга[12], Камерлінг-Оннеса тощо). За рахунок збільшення числа констант у цих рівняннях можна досягти кращого узгодження з практикою, порівняно з рівнянням Ван дер Ваальса. Проте рівняння Ван дер Ваальса завдяки своїй простоті та фізичному змісту сталих a і b, що входять до нього, є найпоширенішим для аналізу якісної поведінки реальних газів.
Розріджений газ
Розрідженим називають газ, тиск якого нижчий від атмосферного. Такий стан газу називають також вакуумом. Ступінь розрідження газу залежить від співвідношення між середньою довжиною вільного пробігу молекул газу, що є характеристикою інтенсивності їхніх взаємних зіткнень у газі та характерного лінійного розміру посудини, у якій газ перебуває. Розрізняють ступені надвисокого , високого , середнього і низького вакууму. Відмінність властивостей розріджених газів від нерозріджених проявляється у перших трьох з перерахованих ступенів вакууму.
Для газів, що перебувають у стані високого вакууму довжина вільного пробігу молекул визначається розмірами посудини. Тому зменшення густини розрідженого газу не впливає на величину , а веде лише до зменшення кількості молекул, що беруть участь у перенесенні імпульсу або внутрішньої енергії. Тому коефіцієнти в'язкості і теплопровідності такого газу мають прямо пропорційну залежність від його густини.
Див. також
Примітки
- У планетарному масштабі газ атмосфери утримується силами гравітації
- Harper, Douglas. «gas». Online Etymology Dictionary.
- Robert Brown On the particles contained in the pollen of plants; and on the general existence of active molecules in organic and inorganic bodies The miscellaneous botanical works of Robert Brown, Volume 1. Опубліковано в Edinburgh new Philosophical Journal (pp. 358—371, July-September), 1828.
- ДСТУ 3651.2-97 Метрологія. Одиниці фізичних величин. Фізичні сталі та характеристичні числа. Основні положення, позначення, назви та значення. Архів оригіналу за 1 серпня 2013. Процитовано 16 листопада 2011.
- Avogadro constant(англ.)
- McPherson, William and Henderson, William. An Elementary study of chemistry. 1917
- Герасимов Я. И. и др., Курс физической химии, т. 1, 1970, с. 50.
- Кубо Р., Термодинамика, 1970, с. 25.
- Белоконь Н. И., Основные принципы термодинамики, 1968, с. 29.
- D. Berthelot in Travaux et Mémoires du Bureau international des Poids et Mesures — Tome XIII (Paris: Gauthier-Villars, 1907)
- C. Dieterici Ann. Phys. Chem. Wiedemanns Ann. 69, 685 (1899).
- Redlich O., Kwong J. N. S. On the Thermodynamics of Solutions. V. An Equation of State. Fugacities of Gaseous Solutions[недоступне посилання з липня 2019] // Chemical Reviews. — 1949. — Т. 44. — № 1. — С. 233—244
Література
- Яворський Б. М., Детлаф А. А., Лебедев А. К. Довідник з фізики для інженерів та студентів вищих навчальних закладів / Переклад з 8-го переробл. і випр. вид. — Т. : Навчальна книга — Богдан, 2007. — 1040 с. — ISBN 966-692-818-3.
- Константінов Ю. М., Гіжа О.О. Технічна механіка рідини і газу [Підручник]. — К. : Вища школа, 2002. — 277 с. — ISBN 966-642-093-7.
- Ландау Л. Д. Теоретическая физика: Учеб. пособ / Л. Д. Ландау, Е. М. Лифшиц. — М. : Наука, 1976. — Т. V. Статистическая физика. Часть 1. — 584 с.
- Сивухин Д. В. Общий курс физики / Д. В. Сивухин. — М. : Наука, 1990. — Т. ІІ. Термодинамика и молекулярная физика. — 592 с. — ISBN 5-02-014187-9.
- Рид Р., Праусниц Дж., Шервуд Т. Свойства газов и жидкостей: Справочное пособие / Пер. с англ. под ред. Б. И. Соколова — 3-е изд. — Л.: Химия, 1982. — 592 с.
- Бех І. І. Основи фізики вакууму та вакуумної техніки. Методи отримання високого й надвисокого вакууму [Текст]: навч. посіб. / І. І. Бех та ін. ; Київський національний ун-т ім. Тараса Шевченка. — К.: Видавничо-поліграфічний центр «Київський університет», 2001. — 105 с. — ISBN 966-594-261
- Мала гірнича енциклопедія : у 3 т. / за ред. В. С. Білецького. — Д. : Донбас, 2004. — Т. 1 : А — К. — 640 с. — ISBN 966-7804-14-3.
