Дазатиніб
Дазатиніб (англ. Dasatinib, лат. Dasatinibum) — синтетичний лікарський препарат, що належить до групи інгібіторів Bcr-Abl-тирозинкінази[1][2], що застосовується перорально.[3][4] Дазатиніб розроблений у співпраці компаніями «Bristol-Myers Squibb» та «Otsuka Pharmaceutical Co.»[5][6][7], та схвалений для клінічного використання FDA в 2006 році.[4]
 | |
|---|---|
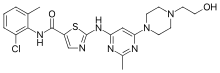
Дазатиніб
| |
| Систематизована назва за IUPAC | |
| N-(2-chloro-6-methylphenyl)-2-[[6-[4-(2-hydroxyethyl)- 1-piperazinyl]-2-methyl-4-pyrimidinyl]amino]-5-thiazole carboxamide monohydrate | |
| Класифікація | |
| ATC-код | L01 |
| PubChem | |
| CAS | |
| DrugBank | |
| Хімічна структура | |
| Формула | C22H26ClN7O2S |
| Мол. маса | 488,01 г/моль |
| Фармакокінетика | |
| Біодоступність | ~100% |
| Метаболізм | Печінка |
| Період напіввиведення | 5-6 год. |
| Екскреція | фекалії (85%), Нирки (4%) |
| Реєстрація лікарського засобу в Україні | |
| Назва, фірма-виробник, країна, номер реєстрації, дата | СПРАЙСЕЛ, «Брістол-Майєрс Сквібб Компані»,США UA/9227/01/01 17.12.2008-17/12/2013 |
Фармакологічні властивості
Дазатиніб — синтетичний лікарський засіб, який належить до групи інгібіторів протеїнтирозинкінази. Механізм дії препарату полягає в інгібуванні ферменту Bcr-Abl і SRC тирозинкінази. Це призводить до пригнічення проліферації та збільшення апоптозу в чутливих до препарату клітинних лініях, а також у щойно уражених лейкемічних клітинах, у тому числі резистентних до іматинібу.[2][3] Біологічною мішенню іматинібу є білки ABL1, c-kit, LCK, YES1, FYN та PDGF-β.[3][4] Дазатиніб застосовується як самостійний препарат, так і в комбінації з іншими препаратами для лікування чутливих до препарату форм хронічного мієлолейкозу та гострого лімфобластного лейкозу із наявністю філадельфійської хромосоми.[3][4] Хоча дазатиніб ефективніший у застосуванні при різних видах лейкозу, ніж інші препарати групи інгібіторів протеїнтирозинкінази, проте при його застосуванні спостерігається велика кількість побічних ефектів.[2] Дазатиніб має обрамлене застереження щодо можливості виникнення при його застосуванні важкої легеневої гіпертензії, яка частіше виникає за рік після початку прийому препарату.[8] Застосування дазатинібу при вагітності може призвести як до народження дитини із чисельними вадами розвитку, так і до самовільного переривання вагітності або народження мертвої дитини, хоча при довготривалих спостереженнях були випадки народження й здорових немовлят.[1]
Фармакокінетика
Дазатиніб швидко та повністю всмоктується після перорального застосування. Максимальна концентрація препарату в крові досягається протягом 0,5—6 годин після прийому препарату. Дазатиніб майже повністю (на 96 %) зв'язується з білками плазми крові.[3][4] Препарат проходить через гематоенцефалічний бар'єр.[2] Препарат проходить через плацентарний бар'єр, даних за виділення в грудне молоко людини немає. Дазатиніб метаболізується у печінці з утворенням переважно неактивних метаболітів. Виводиться препарат переважно із калом, частково із сечею у вигляді метаболітів, частково у незміненому вигляді. Період напіввиведення дазатинібу становить 3—5 годин, цей час може збільшуватися у хворих із порушенням функції печінки.[3][4]
Покази до застосування
Дазатиніб застосовують при хронічному мієлолейкозі (у тому числі при бластному кризі), гострому лімфобластному лейкозі із наявністю філадельфійської хромосоми при резистентності або непереносимості попереднього лікування.[3][4]
Побічна дія
При застосуванні дазатинібу побічні ефекти спростерігаються дуже часто. Найчастішими побічними ефектами препарату є затримка рідини, діарея, головний біль, шкірний висип, нудота, блювання, задишка, підвищена втомлюваність, крововиливи. біль у м'язах, біль у животі, гарячка, фебрильна нейтропенія, тромбоцитопенія.[2][3] Іншими побічними ефектами препарату є[3]:
- Алергічні реакції та з боку шкірних покривів — дерматит, алопеція, гіперпігментація або гіпопігментація шкіри, кропив'янка, підвищення потовиділення, синдром Стівенса-Джонсона, набряк Квінке, синдром Лаєлла, фотодерматоз, свербіж шкіри, виразки шкіри, долонно-підошовний синдром.
- З боку травної системи — стоматит, езофагіт, запор, метеоризм, погіршення апетиту, жовтяниця, холестаз, гепатит, шлунково-кишкові кровотечі, асцит, пептична виразка, гастрит, гастроезофагеальний рефлюкс, сухість у роті, печінкова недостатність, коліт, панкреатит, анальні тріщини.
- З боку нервової системи — запаморочення, порушення смаку, парестезії, безсоння, шум у вухах, затуманювання зору, кон'юнктивіт, підвищена сльозоточивість, сонливість, мігрень, депресія, порушення пам'яті, тривожність, сплутаність свідомості; рідко інсульт, судоми.
- З боку серцево-судинної системи — серцева недостатність, тахікардія, артеріальна гіпотензія або гіпертензія, набряк легень, підвищена кровоточивість, периферичні набряки, тромбози або емболії, перикардит, приливи крові, подовження інтервалу QT на ЕКГ, стенокардія, інфаркт міокарду.
- З боку дихальної системи — кашель, легеневі інфільтрати, легенева гіпертензія, респіраторний дистрес-синдром, ексудативний плеврит, бронхоспазм, бронхіальна астма, пневмонія.
- З боку сечостатевої системи — гінекомастія, порушення менструального циклу, ниркова недостатність, частий сечопуск, протеїнурія.
- З боку опорно-рухового апарату — болі у м'язах і суглобах, скованість м'язів і суглобів, рабдоміоліз.
- Інфекційні ускладнення — сепсис, герпетичні інфекції, інфекції верхніх дихальних шляхів, кишкові інфекції, грибкові інфекції, вірусні та бактеріальні інфекції різної локалізації.
- Зміни в лабораторних аналізах — анемія, панцитопенія, підвищення рівня креатиніну та сечовини в крові, підвищення рівня сечової кислоти в крові, зниження рівня альбуміну в крові.
Протипокази
Дазатиніб протипоказаний при підвищеній чутливості до препарату, при вагітності та годуванні грудьми, а також у дитячому та підлітковому віці.[3]
Форми випуску
Дазатиніб випускається у вигляді таблеток по 0,02; 0,05; 0,07; 0,08; 0,1 та 0,14 г.[4][9]
Примітки
- Ліки і вагітність. Дазатиніб
- Дазатиниб: 10 лет применения в мировой клинической практике (рос.)
- https://www.vidal.ru/drugs/molecule/1880 (рос.)
- Dasatinib (англ.)
- Otsuka and Bristol-Myers Squibb Announce a Change in Contract Regarding Collaboration in Japan in the Oncology Therapy Area (англ.)
- FDA Approves U.S. Product Labeling Update for Sprycel® (dasatinib) to Include Three-Year First-Line and Five-Year Second-Line Efficacy and Safety Data in Chronic Myeloid Leukemia in Chronic Phase (англ.)
- Bristol-Myers Squibb Announces Extension of U.S. Agreement for ABILIFY® and Establishment of an Oncology Collaboration with Otsuka (англ.)
- FDA: Sprycel (dasatinib): Drug Safety Communication — Risk of Pulmonary Arterial Hypertension (англ.)
- https://www.vidal.ru/drugs/molecule-in/1880 (рос.)