Стронгілоїдоз
Стронгілоїдо́з (застар. «кохінхінська діарея»; англ. Strongyloides stercoralis infection, лат. Strongyloidosis) — гельмінтоз, який спричинюють кишкові вугриці з роду Strongyloides. Ця паразитарна інвазія характеризується в клінічному плані хронічним перебігом з переважним ураженням органів травної системи і системною алергією.
| Стронгілоїдоз | |
|---|---|
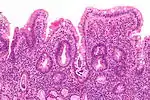 Кишкові вугриці в слизовій кишечнику (по центру і в лівому куті мікрофотографії). Забарвлення гематоксилин-еозином Кишкові вугриці в слизовій кишечнику (по центру і в лівому куті мікрофотографії). Забарвлення гематоксилин-еозином | |
| Спеціальність | інфекційні хвороби і гельмінтолог |
| Симптоми | гарячка, кропивниця, сверблячка, кашель, нудота, біль у животі, діарея, гепатомегалія, головний біль, астенія, запаморочення, міокардит, артралгія, міалгія, бронхіт, кон'юнктивіт, Ірит, виразка, менінгіт і сепсис |
| Причини | Strongyloides stercoralisd |
| Метод діагностики | клінічний аналіз крові, мікроскопія і ІФА |
| Препарати | івермектин[1][2], тіабендазолd[1], альбендазол і мебендазол |
| Класифікація та зовнішні ресурси | |
| МКХ-11 | 1F6B |
| МКХ-10 | B78 |
| DiseasesDB | 12559 |
| MedlinePlus | 000630 |
| eMedicine | article/999614-overview |
| MeSH | D013322 |
| | |
Історичні відомості
Стронгілоїдоз під назвою «кохінхінська діарея» вперше описав французький лікар Л. А. Норман в 1876 році у солдат, які поверталися до Франції з Кохінхіни (фр. Cochin-China) (району дельти річки Меконга у південно-східному Індокитаї). Він знайшов в їх фекаліях нового паразита[3][4]. У 1876-77 роках французький зоолог і фармаколог Артур Баве в стінці тонкої кишки людей, загиблих від такої діареї, виявив мікроскопічних нематод, які морфологічно відрізнялись від тих, які раніше були знайдені у фекаліях[5][6]. Він описав нематоду як окремий вид Anguillula stercoralis[7][8]. У 1879 році видатний італійський паразитолог Джованні Баттіста Грассі надав ґрунтовні відомості при життєвий цикл паразита[9], в подальшому дав найменування новому роду паразитів — грец. Στρογγυλός — округлий і грец. όμοιος — подібний. Біологічний цикл збудника розшифрував німецький зоолог Р. Лойкарт у 1882 році, який встановив, що всі до цього знайдені окремо личинки та дорослі особини належать одному паразиту[10]. У 1901—1902 роках бельгійський лікар П. Ван Дюрм описав перкутанний шлях зараження при стронгілоїдозі[11], тоді ж зоологи Ч. Стайлз і А. Гассалл дали остаточну назву збуднику Strongyloides stercoralis[12]. У 1914 році німецький паразитолог Ф. Фюллеборн виявив феномен автоінвазії й показав на собаках, як він реалізується[13]. У подальшому було відкрито ще багато представників роду Strongyloides[14], які паразитують у тварин, і деякі з них здатні заражати людей, зокрема Strongyloides fuelleborni[15], що є паразитом мавп і досить часто уражає людей, та Strongyloides fuelleborni kellyi[16], що був знайдений у мавп у Новій Гвінеї і також має схильність до ураження людей, але з них тільки Strongyloides stercoralis є повністю антропонозним збудником.
Актуальність
Стронгілоїдоз поширений переважно в країнах тропічного і субтропічного кліматичного пояса, але його спостерігають і в районах помірного клімату. Вважають, що від 30 до 100 млн людей в світі хворіють на стронгілоїдоз, хоча точна кількість хворих в ендемічних регіонах невідома[17], за іншими даними інвазовано до 370 млн людей. Значну ураженість людей стронгілоїдозом відзначають у країнах Східної та Південної Африки (до 25-30 %), Південно-Східної Азії (до 18 %), в країнах Південної Америки (від 4 % до 31 %)[18]. У країнах Європи показники ураженості населення стронгілоїдозом становлять 1-2 %, і тільки в окремих зонах (Румунія) досягають 20 %[19].
Стронгілоїдоз реєструють і в різних областях України з частотою 0,1-5 %. Випадки хвороби виявлені в багатьох регіонах України, майже повсюдно, але найбільша поширеність відзначена в лучно-степовій зоні Придністров'я, Закарпаття, Поліської низовини, на Волині. Показано, що вологий клімат рівнинних територій західних областей України створює сприятливі умови для розвитку ґрунтових стадій паразитів, прохолодний режим гірських Карпат гальмує цей процес.
Особливого значення на сьогодні ця інвазія заслуговує через факт того, що вона є ВІЛ-індикаторною і при цьому набуває тяжкого генералізованого характеру[20].
Етіологія
? Threadworm | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
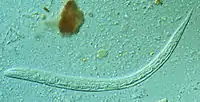 Перша стадія личинки Strongyloides stercoralis | ||||||||||||
| Біологічна класифікація | ||||||||||||
| ||||||||||||
Види | ||||||||||||
| ||||||||||||
Посилання | ||||||||||||
| ||||||||||||
Класифікація кишкових вугриць і морфологія
Основного збудника людського стронгілоїдозу — Strongyloides stercoralis відносять до роду Strongyloides, типу Nematoda. У цьому роді є ще 2 види патогенних для людини кишкових вугриць — Strongyloides fuelleborni та Strongyloides fuelleborni kellyi, але вони в Україні не зустрічаються, уражають невелику кількість осіб в Африці та Папуа-Новій Гвінеї. Кишкові вугриці є дуже дрібними нематодами, яйця їх прозорі, овальної форми.
Всередині кишок
Паразит має складний цикл розвитку з можливим чергуванням вільноживучих і паразитуючих поколінь статевозрілих черв'яків. Розвиток гельмінта йде без проміжного господаря, проходить зі зміною поколінь, як тих, що живуть вільно, так і паразитичних. Статевозрілі самки паразитичного покоління локалізуються в організмі людини в товщі слизової оболонки дванадцятипалої кишки, при інтенсивній інвазії можуть проникати в шлунок, слизову тонкого та товстого кишечника, панкреатичні та жовчні ходи[23]. Запліднені самки, що паразитують у слизовій оболонці тонкої кишки, відкладають туди за добу до 50 яєць, з яких у просвіт ліберкюнових залоз, а потім і кишечника виходять рабдитоподібні личинки довжиною 0,2-0,3 мм. Іноді личинки вилуплюються безпосередньо в порожнини матки самки, в цьому випадку самка народжує вже живі личинки. Ці личинки виділяються з фекаліями у довкілля, де перетворюються або на філярієподібних личинок, або на статевозрілих самців і самок, які живуть вільно і здатні відкладати яйця.
У ґрунті
За наявності зовнішніх сприятливих умов (температура 26-28 °C і достатня вологість ґрунту) розвивається вільноживуче покоління гельмінтів: з рабдитоподібних личинок, що потрапили з фекаліями в ґрунт, розвиваються статевозрілі форми, які можуть не тільки жити, але і розмножуватися у довкіллі. За певних умов (зниження температури навколишнього середовища нижче 25 °C) вільноживучі рабдитоподібні личинки можуть перетворюватися на інвазивні філярієподібні личинки. Вони здатні зберігатися в ґрунті до 3-4 тижнів. Зниження температури нижче 0 °C, висихання ґрунту сприяють швидкій їх загибелі.
Потрапляння до організму
Філярієподібні личинки в організм людини проникають через шкіру або через рот з водою і їжею. Якщо зараження відбулося через шкіру (перкутанно), личинки здійснюють міграцію в організмі, досягають кишечника через дихальні шляхи, глотку, стравохід.
.tif.jpg.webp)
Епідеміологічні особливості
Джерело і резервуар
Джерело інвазії — людина, яка хворіє на стронгілоїдоз і виділяє у зовнішнє середовище живі личинки. Заражені люди за відсутності гігієнічних навичок можуть бути безпосередньо заразними для оточуючих. Ґрунт є резервуаром при стронгілоїдозі.
Механізм і фактори передачі
Механізм зараження — контактний, інфікування реалізується при проникненні личинок через шкіру при контакті з контамінованим ґрунтом. Іноді інвазування відбувається й оральним механізмом при ковтанні личинок (вживання забруднених ними ягід, овочів, фруктів, води). Тривалий перебіг захворювання, ймовірно, обумовлений можливістю реалізації внутрішньокишкового типу розвитку паразита з автоінвазією, коли при уповільненій евакуації кишкового вмісту рабдитоподібні личинки перетворюються в філярієподібні безпосередньо в кишечнику. Іноді автоінвазія може бути зовнішньокишковою, коли рабдитоподібні личинки перетворюються на філярієподібні в промежині у неохайних осіб, після чого повертаються знову в кишечник. За відсутності застереження і при низькому рівні гігієнічних навичок людина може безпосередньо від хворого через рукостискання, предмети побуту отримати філярієподібні личинки і непомітно для себе заковтнути їх.
Сприйнятливий контингент та імунітет
У країнах з теплим і вологим кліматом розвиток личинок паразита до інвазійних стадії у відкритому ґрунті відбувається цілий рік. У зонах з помірним кліматом періоди поширення цієї інвазії лімітуються термінами теплого періоду року. Через це хворіти можуть ті особи, що мають частий контакт з ґрунтом. Стронгілоїдоз може поширюватися як невелика епідемія серед шахтарів, землекопів у випадках порушення ними санітарно-гігієнічного режиму. Імунітет не прояснений. Можливе вироблення антитіл проти личинок паразита, що здатне послабити інтенсивність процесу автоінвазіі та, навіть, призводити до елімінації паразита.
Патогенез
Загальні риси
Гельмінт потрапляє через шкіру чи рот. У ранню міграційну фазу гельмінтозу основне значення мають сенсибілізуюча дія антигенів личинок і запальні реакції слизової оболонки кишечника в місцях паразитування дорослих черв'яків. При хронічному перебігу стронгілоїдозу розвиваються атрофічні зміни слизової оболонки кишечника, порушується всмоктування поживних речовин, що призводить до аліментарної (харчової) недостатності, кахексії. Кишкова стадія стронгілоїдоза розвивається через 20-30 днів після зараження. Паразитування гельмінтів у слизовій оболонці супроводжується пошкодженням її: виникненням крововиливів, еозинофільної інфільтрації ерозій[24], а нерідко й виразок слизової оболонки. Яйця, які самки відкладають в підслизовому шарі, розкриваються поблизу епітеліального шару, спричиняючи додаткові місцеві пошкодження тканин. Кишкові ушкодження проявляються синдромами порушення всмоктування жиру і вуглеводів. Ентеропатія супроводжується втратою білка, що зумовлює гіпопротеїнемію. Гранульоми можуть виявлятися не тільки у кишечнику і шлунку, але й в печінці та інших органах. Вони містять гігантські багатоядерні клітини, що підтверджує розвиток гіперергічного стану.
Автоінвазійний процес
Пригнічується нормальною імунною відповіддю. У пацієнтів з порушеннями клітинного імунітету автоінвазія може призвести до виникнення двох найтяжчих клінічних форм стронгілоїдозу:
- гіперінфекційного синдрому;
- генералізації.
Наявність аутоінфекції є основною ознакою, що відрізняє стронгілоїдоз від інших широко поширених інвазій, які спричинюють геогельмінти (аскаридоз, трихоцефальоз, анкілостомідози).
Гіперінфекційний синдром
Проявляється пришвидшенням нормального життєвого циклу Strongyloides stercoralis, що призводить до розвитку великої кількості збудників без поширення личинок за межі звичайної схеми міграції[25], тобто з локалізацією в травній системі[26], легенях[27].
Генералізація
А от при наявності в хворого імунодефіциту, зокрема це часто відбувається при СНІДі, при тривалій терапії глюкокортикоїдами, при застосуванні імунодепресантів після трансплантації, відбувається генералізація стронгілоїдозу — спостерігається дифузне ураження всіх відділів кишечника, гематогенна дисемінація личинок з контамінацією легень, підшлункової залози, серця, ЦНС[28][29]. У таких тяжких випадках через ушкодження кишечника, спричинених великою кількістю кишкових вугриць, здійснюється й транслокація кишкових бактерій, що призводить до полімікробної бактеріємії майже у 50 % хворих та менінгіту[20][30].
Клінічні прояви
Класифікація
До МКХ-10 включений «Стронгілоїдоз» під кодом В78, в якому додатково виділяють:
- Стронгілоїдоз кишковий (В78.0);
- Стронгілоїдоз шкіри (В78.1);
- Дисемінований стронгілоїдоз (В78.7);
- Стронгілоїдоз неуточнений (В78.9).
Загальні прояви
Тривалість інкубаційного періоду точно невідома. Рання міграційна фаза стронгілоїдозу, яка відбувається при перкутанному зараженні, триває до 10 днів. Личинка, яка мігрує під шкірою, виглядає при поверхневому розташуванні як тоненька червона лінія, яка швидко рухається (більше 5 см за день), а потім швидко зникає. У цій ситуації хворобу визначають як стронгілоїдоз шкіри. У цю фазу також спостерігають гарячку, кропив'янку або папульозні висипання, що супроводжуються шкірним свербінням, кашель іноді з домішкою крові в мокроті, задишку. У пізній фазі інвазії, коли гельмінти досягають статевої зрілості і паразитують в кишечнику, клінічні прояви захворювання пов'язані з ураженням травної системи. Тоді мова йде про кишковий стронгілоїдоз. За відсутності лікування і продовження автоінвазії гельмінтоз набуває хронічного перебігу, іноді триває багато десятиліть[31][32].
Типовий перебіг
При легкому перебігу захворювання спостерігаються нудота, періодично біль в епігастрії. Можливе візуально непомітне виповзання личинок через анальний отвор, що супроводжується нерідко свербінням періанальної ділянки. Випорожнення, як правило, не змінені, можуть спостерігати запори або чергування запорів з проносами. При виражених проявах нудота нерідко супроводжується блюванням, іноді з'являється гематемезис, виникають гострий нападоподібний біль в епігастрії або по всьому животі, періодично рідкі випорожнення до 5-7 разів на добу. Печінка у деяких хворих збільшена і ущільнена. При симптомному перебігу стронгілоїдозу проноси стають постійними, випорожнення набувають гнильного запаху і містить залишки неперетравленої їжі. Діарея є в такій ситуації основним симптомом. Випорожнення часті, до 15-20 разів на добу, а іноді спостерігають надмірне їх почастішання, що отримало назву в старих літературних джерелах як «непереможна діарея» (англ. invincible diarrhea). Найчастіше випорожнення водянисті, іноді — з домішками слизу і крові. З боку нервової системи відзначають головний біль, запаморочення, підвищену розумову стомлюваність, неврастенічні і психастенічні прояви.
Перебіг з переважанням алергічних проявів
Характеризується явищами вперто рецидивуючої кропив'янки різного виду з утворенням прямолінійних або серпантиноподібних ліній, кілець, плям, пухирів тощо[33], свербежу, міалгій, артралгій[34]. У деяких хворих виявляють алергічні міокардити, бронхіти астматичного характеру, астеновегетативний синдром, поліартралгію як прояв алергії. Описані ураження органу зору алергічного і трофічного характеру: коньюнктивіти, ангіоретінопатіі, макуліти, виразки рогівки. З боку травного тракту при такому перебігу диспепсичні розлади і абдомінальний біль виражені помірно. Бувають і ураження слизистої оболонки сечового міхура з дизурією.
Гіперінфекційний синдром
Гастроінтестінальні і легеневі прояви виразні. Проноси стійки, практично невпинні. Розвивається зневоднення, тяжка вторинна анемія, кахексія. Легеневі прояви включають задишку, кровохаркання і дихальну недостатність. Інші прояви обумовлені ураженнями інших органів. Ураження ЦНС включає в себе паразитарний менінгіт, абсцес мозку, і дифузний енцефаліт. Вторинний менінгіт і сепсис, спричинений грамнегативними бактеріями відбуваються з високою частотою, вони пов'язані з порушенням цілісності слизової оболонки кишечника, із потраплянням цих бактерій до кровотоку через наявність їх на поверхні мігруючих личинок. Потрапляння личинок до печінки може призвести до холестатичної жовтяниці і гранулематозного гепатиту.
Дисемінований стронгілоїдоз
Розвивається на тлі імунодефіциту, через що практично всі симптоми пов'язані як з тяжким пошкодженням органів (кишечник, легені, печінка тощо), уражених кишковими вугрицями, так і з імунними порушеннями, які маскують прояви безпосередньо стронгілоїдозних уражень, через що нерідко сам стронгілоїдоз своєчасно не розпізнається. Нерідко алергічні прояви, притаманні типовому перебігу, змазані через переважання імунодефіциту.
Ускладнення
Нерідкі виразкові ураження кишечника, можуть бути апендицит[35], перфоративний перитоніт[36], кишкова непрохідність, панкреатит, мальабсорбція. Тяжкий гіперінфекційний і дисемінований стронгілоїдоз призводить до високої летальності, яка досягає 80 %, тому що діагноз часто встановлюється пізно через неспецифічність клінічних проявів і слабку відповідь імуноскомпрометованої людини, у якої зазвичай розвивається такий тяжкий процес[37][38].
Діагностика
Клініко-епідеміологічна діагностика
Підозрілим на стронгілоїдоз є:
- епідеміологічний анамнез (проживання або перебування в несприятливих по стронгілоїдозу регіонах);
- короткочасні, раптові шкірні алергічні прояви на ногах, пальцях рук, які виникають без видимої причини;
- алергічні та загальнотоксичні реакції, що швидко розвиваються слідом за цим;
- наявність літучих інфільтратів у легенях, що спостерігають при рентгенологічному дослідженні;
- поліорганність уражень;
- рецидивуюча алергія, особливо. коли вона поєднується з кишковими проявами;
- стійкий діарейний синдром, що супроводжується диспротеїнемією.
Загальнолабораторна і інструментальна діагностика
У периферичній крові у більшості хворих в ранню фазу в загальному аналізі виявляють еозинофілію[39] до 70-80 %, при тривалих інвазіях виникає помірна вторинна анемія, відзначають гіпопротеїнемію, і лише іноді еозинофілію. При тяжкому перебігу стронгілоїдозу еозинофілія може бути слабо виражена або, навіть, спостерігають анеозінофілію[40]. Через відсутність патогномонічних[41] симптомів при стронгілоїдозі обстеженню на наявність його підлягають всі хворі з високою еозинофілією[42]. Великі труднощі являє діагностика стронгілоїдозу у випадках відхилення від звичайного міграційного шляху Strongyloides stercoralis. Захворювання незалежно від особливостей початкових ознак може призвести до локалізації збудника в більш пізній стадії захворювання поза кишечником. Враховуючи це, на стронгілоїдоз слід обстежувати всіх хворих з хронічними рецидивуючими захворюваннями травної системи і жовчних шляхів. При ураженні слизової оболонки сечового міхура можуть виникати альбумінурія, гематурія. Біохімічні дослідження дозволяють виявити іноді підвищення рівня білірубіну, порушення антітоксичної функції печінки.
У міграційну фазу хвороби при рентгенографію легенів іноді виявляють летючі інфільтрати[43]. Зміни при інструментальних дослідженнях неспецифічні: рентгенологічне дослідження органів травної системи дозволяє виявити ознаки хронічного гастриту, дуоденіту, перидуоденіту, дискінезії дванадцятипалої кишки, спастичного коліту. При фіброгастродуоденоскопії виявляють геморагічний, ерозивний або виразковий гастродуоденіт[44].
Специфічна діагностика
Полягає у виявленні личинок в дуоденальному вмісті і калі (за методом Шульмана, Бермана тощо), зрідка й у сечі виявляють личинки паразитів. У міграційній фазі іноді вдається виявити личинки в мокроті. Використовують ІФА крові[45], зменшення кількісного титру антитіл в процесі лікування є показником адекватності терапії[46]. При стронгілоїдозній міграції іноді посів мокроти на бактеріальні збудники демонструє рост бактерій у вигляді «смужкових» колоній, де смужки росту бактерій, що відходять від округлої основної колонії, відбуваються через розповзання личинок гельмінта і проявлення сліду цього саме виявляють у вигляді смужок колоній.
Лікування
Лікування хворих на стронгілоїдоз здійснюється відповідно до загальних принципів терапії інфекційних захворювань.
Етіотропна терапія
Показана всім хворим, навіть з стертим перебігом через небезпеку виникнення гіперінфекційного синдрому або генералізації в разі приєднання імунодефіциту. Застосовують мебендазол або альбендазол по 0,2 г 2 рази на добу 3 дні. Через 3 тижні рекомендується провести повторний цикл лікування в тих же дозах. При тяжкому перебігу інвазії, у пацієнтів з імунодефіцитними станами можуть проводитися більш часті повторні курси протигельмінтної терапії зі зміною препаратів. У країнах Європи і Північної Америки рекомендують ще застосовувати івермектін і тіабендазол[47]. У регіонах, де проводиться профілактика онхоцеркозу або лімфатичних філяріїдозів із застосуванням івермектина, виявлене помітне зниження поширеності стронгілоїдозу, що свідчить про ефективність препарату при лікуванні цього гельмінтозу. Комітет ВООЗ по основних лікарських засобів включив івермектин у список препаратів для лікування стронгілоїдозу, в тому числі в поєднанні з альбендазолом. Івермектин та тіабендазол наразі не зареєстровані в Україні[48].
Патогенетичне лікування
При загрозі виникнення супутнього бактеріального менінгіту, сепсису в разі генералізації стронгілоїдозу додатково застосовують антибіотики. Характер і обсяг патогенетичної та симптоматичної терапії визначаються тяжкістю захворювання і наявними порушеннями функцій органів і систем.
Профілактика
Загальні заходи
Профілактика стронгілоїдозу включає санітарно-епідеміологічні заходи, спрямовані на охорону ґрунту від фекального забруднення, санітарну просвіту населення, обстеження населення на гельмінти та проведення дегельмінтизації хворим. З метою захисту від зараження в ендемічних по стронгілоїдозу регіонах необхідно ретельно мити овочі та зелень, для пиття використовувати кип'ячену або промислово виготовлену воду, передбачають заходи щодо захисту відкритих частин тіла від укорінення личинок. Мандрівники до ендемічних районів повинні носити взуття при ходьбі на пляжі та в інших місцях з відкритим ґрунтом. Знезараження об'єктів навколишнього середовища, зокрема ґрунту, від личинок збудника стронгілоїдозу, досягається шляхом обробки їх 10 % розчином хлориду натрію, азотними, калійними, мінеральними добривами, а також пестицидом карбатіоном у вигляді 2 % розчину, що зумовлює загибель личинок і статевозрілих вільноживучих паразитів.
Боротьба з атрактантами
Відомо, що личинки кишкових вугриць вловлюють із зовнішнього середовища відповідні хімічні сигнали, за якими вони знаходять потенційного господаря. Вони використовують як датчики свої нейрони, щоб ідентифікувати ці сигнали, якими є неспецифічні атрактанти тепла, вуглекислого газу, хлориду натрію, що надходять від людей або тварин[49]. Головним притягуючим цих личинок атрактантом є уроканінова кислота[50], яку широко виділяють шкірні залози ссавців. Ця кислота на шкірі може бути заблокована іонами металів, що є напрямком стратегії профілактики перкутанного зараження стронгілоїдозом при перебуванні у високоендемічних по цій інвазії територіях[51].
Примітки
- NDF-RT
- Drug Indications Extracted from FAERS — doi:10.5281/ZENODO.1435999
- Normand, L., 1876, sur la maladie dite diarrhee de cochinchine. (Extrait d'une lettre adresse a M. le President par M. le vice-amiral Jurien de la Graviere). Comptes Rendus Hebdomadaires des seances de l'Acadimie des sciences, 83. 316—318.
- Grove, D.I. (1990). A History of Human Helminthology, Wallingford: CAB International.
- Bavay, A., 1876, Sur l'Anguillule stercorale. (Presentee par M. P. Gervais). Comptes Rendus Hebdomadaires des Seances de l'Acadimie des Sciences, 83, 694—696.
- Cox FE (October 2002). «History of Human Parasitology». Clin. Microbiol. Rev. 15 (4): 595—612.
- Від лат. anguillula — вугор і лат. stercus — фекалії.
- Bavay, A., 1877, Sur l'Anguillule intestinale (Anguillala intestinalis), nouveau ver nematoide, trouve par le Dr. Normand chez les malades atteints de diarrhee de Cochinchine. (Presentee par M. P Gervais). Comptes Rendus Hebdonzadaires des Siances de l'Acaddmie des Sciences, 84, 266—268.
- Grassi, G.B., 1879. Sovra l'Anguillula intestinale. Rend R. Istit. Lomb. Sci. e Lett. Seconda Ser. 17, 228—233.
- Leuckart, R Ueber die Lebensgeschichte der sogenannten Anguillula stercoralis und deren Beziehungen zu der sogenannten Anguillala intestinalis. Bericht uber die Verhlandungen der Koniglich sachsischen Gesellschaft der Wissenschaften zu Leipzig. Mathematische-Physische Classe (1882) 34, 85-107.
- van Durme, P., l90l-l9O2, Quelques notes sur les embryons de ,,strongyloides intestinalis,, et leur penetration par la peau. Thompson yates Laboratoris Report, 4, 47I-474.
- Stiles CW, Hassall A (1902). Strongyloides stercoralis, the correct name of the parasite of Cochin China diarrhoea. Am Med 4:343.
- Fulleborn, F. (1914). Untersuchungen uber den Infektionsweg bei Strongyloides und Ankylostomum und die Biologie dieser Parasiten. Archiv firr Schiffs-und Tropen-Hygien 18, 26-80.
- На сьогодні відомо 58 видів.
- Linstow V. Strongyloides fulleborni n. sp. Centralblat Fur Bakteriologie 1905; 38: 532-3.
- Kelly A. Report of a nematode found in humans at Kiunga, Western District. Papua New Guinea Medical Journal 1973; 16: 59.
- Neglected tropical diseases. Strongyloidiasis. Key facts
- Yori PP, Kosek M, Gilman RH, Cordova J, Bern C, Chavez CB, et al. Seroepidemiology of strongyloidiasis in the Peruvian Amazon. Am J Trop Med Hyg. Jan 2006;74(1):97-102.
- Genta RM. Global prevalence of strongyloidiasis: critical review with epidemiologic insights into the prevention of disseminated disease. Rev Infect Dis 1989;11:755-767.
- Marcos, L. A.; Terashima, A.; Dupont, H. L.; Gotuzzo, E. (2008). «Strongyloides hyperinfection syndrome: An emerging global infectious disease». Transactions of the Royal Society of Tropical Medicine and Hygiene 102 (4): 314—318.
- Mark E. Viney, James B. Lok Strongyloides spp. 2007
- Ці 3 види виявлені у людей. Існує багато видів, які циркулюють у тварин.
- Schad GA. Morphology and life history of Strongyloides stercoralis. / Grove DI, ed. Strongyloidiasis: A Major Roundworm Infection of Man. London: Taylor & Francis, 1989:85-104.
- Поверхневе пошкодження епітелію слизових оболонок.
- Asdamongkol N, Pornsuriyasak P, Sungkanuparph S. Risk factors for strongyloidiasis hyperinfection and clinical outcomes. Southeast Asian J Trop Med Public Health. Sep 2006;37(5):875-84.
- Csermely L, Jaafar H, Kristensen J, Castella A, Gorka W, Chebli AA, et al. Strongyloides hyper-infection causing life-threatening gastrointestinal bleeding. World J Gastroenterol. Oct 21 2006;12(39):6401-4.
- Igra-Siegman, Y; Kapila, R; Sen, P; Kaminski, ZC; Louria, DB (1981). «Syndrome of hyperinfection with Strongyloides stercoralis». Reviews of infectious diseases 3 (3): 397—407.
- Stone WJ, Schaffner W. Strongyloides infections in transplant recipients. Semin Respir Infect. Mar 1990;5(1):58-64.
- Lim S, Katz K, Krajden S, Fuksa M, Keystone JS, Kain KC. Complicated and fatal Strongyloides infection in Canadians: risk factors, diagnosis and management. CMAJ. Aug 31 2004;171(5):479-84
- Newberry, AM; Williams, DN; Stauffer, WM; Boulware, DR; Hendel-Paterson, BR; Walker, PF (Nov 2005). «Strongyloides hyperinfection presenting as acute respiratory failure and gram-negative sepsis.». Chest 128 (5): 3681-4.
- Pelletier LL Jr, Gabre-Kidan T. Chronic strongyloidiasis in Vietnam veterans. Am J Med. Jan 1985;78(1):139-40
- Guyomard JL, Chevrier S, Bertholom JL, Guigen C, Charlin JF. [Finding of Strongyloides stercoralis infection, 25 years after leaving the endemic area, upon corticotherapy for ocular trauma]. J Fr Ophtalmol. Feb 2007;30(2): e4.
- Ly MN, Bethel SL, Usmani AS, Lambert DR. Cutaneous Strongyloides stercoralis infection: an unusual presentation. J Am Acad Dermatol. Aug 2003;49(2 Suppl Case Reports): S157-60.
- Masseau A, Hervier B, Leclair F, Grossi O, Mosnier JF, Hamidou M. [Strongyloides stercoralis infection simulating polyarteritis nodosa]. Rev Med Interne. Aug 2005;26(8):661-3.
- Komenaka IK, Wu GC, Lazar EL, Cohen JA. Strongyloides appendicitis: unusual etiology in two siblings with chronic abdominal pain. J Pediatr Surg. Sep 2003;38(9): E8-10.
- Harish K, Sunilkumar R, Varghese T, Feroze M. Strongyloidiasis presenting as duodenal obstruction. Trop Gastroenterol. Oct-Dec 2005;26(4):201-2.
- Arsic-Arsenijevic V, Dzamic A, Dzamic Z, Milobratovic D, Tomic D. Fatal Strongyloides stercoralis infection in a young woman with lupus glomerulonephritis. J Nephrol. Nov-Dec 2005;18(6):787-90.
- Fardet L, Généreau T, Poirot JL, Guidet B, Kettaneh A, Cabane J. Severe strongyloidiasis in corticosteroid-treated patients: case series and literature review. J Infect. Jan 2007;54(1):18-27.
- Підвищення кількості еозинофілів.
- Відсутність еозинофілів в периферичній крові.
- Тобто стовідсоткових.
- Pirisi M, Salvador E, Bisoffi Z, Gobbo M, Smirne C, Gigli C, et al. Unsuspected strongyloidiasis in hospitalised elderly patients with and without eosinophilia. Clin Microbiol Infect. Aug 2006;12(8):787-92.
- В поєднанні з еозинофілією крові це складає синдром Леффлера, який може зустрічатися ще й при міграційній фазі аскаридозу, при анкілостомідозі, деяких інших гельмінтозах, при алергії на медикаментозні засоби, на респіраторні біологічні антигени (пилок рослин, вовна тощо).
- Mittal S, Sagi SV, Hawari R. Strongyloidiasis: endoscopic diagnosis. Clin Gastroenterol Hepatol. Feb 2009;7(2): e8.
- Rodrigues RM, de Oliveira MC, Sopelete MC, Silva DA, Campos DM, Taketomi EA, et al. IgG1, IgG4, and IgE antibody responses in human strongyloidiasis by ELISA using Strongyloides ratti saline extract as heterologous antigen. Parasitol Res. Oct 2007;101(5):1209-14.
- Salvador F, Sulleiro E, Sánchez-Montalvá A, Saugar JM, Rodríguez E, Pahissa A, et al. Usefulness of Strongyloides stercoralis serology in the management of patients with eosinophilia. Am J Trop Med Hyg. May 2014;90(5):830-4.
- SPHTM Strongyloidiasis Home Page Архівовано 12 березня 2011 у Wayback Machine.
- Державний реєстр лікарських засобів України
- Forbes, WM; Ashton, FT; Boston, R; Zhu, X; Schad, GA (2004). «Chemoattraction and chemorepulsion of Strongyloides stercoralis infective larvae on a sodium chloride gradient is mediated by amphidial neuron pairs ASE and ASH, respectively». Veterinary parasitology 120 (3): 189-98.
- Вона є продуктом перетворення гістидина, яке відбувається в печінці і шкірі.
- Safer, D.; Brenes, M.; Dunipace, S.; Schad, G. (2007). «Urocanic acid is a major chemoattractant for the skin-penetrating parasitic nematode Strongyloides stercoralis». Proceedings of the National Academy of Sciences 104 (5): 1627.
Джерела
- Інфекційні хвороби (підручник) (за ред. О. А. Голубовської). — Київ: ВСВ «Медицина» (2 видання, доповнене і перероблене). — 2018. — 688 С. + 12 с. кольор. вкл. (О. А. Голубовська, М. А. Андрейчин, А. В. Шкурба та ін.) ISBN 978-617-505-675-2
- Возіанова Ж. І. Інфекційні і паразитарні хвороби: В 3 т. — К.: «Здоров'я», 2008. — Т.1.; 2-е вид., перероб. і доп. — 884 с. ISBN 978-966-463-012-9
- Шкурба А. В., Голубовская О. А., Безродная А. В., Винницкая Е. В., Подолюк О. А., Сукач М. Н. Стронгилоидоз. Обзор клинических рекомендаций Всемирной организации гастроэнтерологов по диагностике и лечению (2018 год). Клиническая инфектология и паразитология (международный научно-практический журнал). 2019. том 8, № 2. С. 182—195. (рос.)
- Паразитарные болезни человека (Шабловская Е. А., Падченко И. К., Мельник М. Н. и др.). — К.:Здоров'я, 1984. — 160 с. (рос.)
- Зюков А. М. (за участі Падалки Б. Я.) Гострі інфекційні хвороби та гельмінтози людини. К. 1947;
- Segarra-Newnham, M. (2007). «Manifestations, diagnosis, and treatment of Strongyloides stercoralis infection». Ann Pharmacother 41 (12): 1992—2001. (англ.)
- Pranatharthi Haran Chandrasekar, Hari Polenakovik, Sylvia Polenakovik Strongyloidiasis. Medscape/Infectious Diseases/ Gastrointestinal Tract and Intra-abdominal Infections. (Chief Editor Michael Stuart Bronze) Updated: Oct 16, 2014 . (англ.)
- Бронштейн А. М. Паразитарные болезни человека: Протозоозы и гельминтозы / А. М. Бронштейн, А. К. Токмалаев. — Москва: Издательство Российского университета дружбы народов, 2004. — 206 с. (рос.)
- Паразитарные болезни человека (протозоозы и гельминтозы): руководство для врачей / под ред. В. П. Сергиева, Ю. В. Лобзина, С. С. Козлова. — С.Пб. : ООО «Издательство Фолиант», 2008. — 592 с. (рос.)