Пазопаніб
Пазопаніб (англ. Pazopanib, лат. Pazopanibum) — синтетичний лікарський препарат, який належить до групи інгібіторів тирозинкінази[2][3][4], що застосовується перорально.[5][6][7] Пазопаніб схвалений до клінічного застосування у 2009 році в США, та в 2010 році у Великій Британії, Європейському Союзі та Австралії.[8][9][10][11][12]
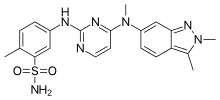 | |
|---|---|
Пазопаніб
| |
| Систематизована назва за IUPAC | |
| 5-({4-[(2,3-Dimethyl-2H-indazol-6-yl)methylamino]pyrimidin-2-yl}amino)-2-methylbenzenesulfonamide | |
| Класифікація | |
| ATC-код | L01 |
| PubChem | |
| CAS | |
| DrugBank | |
| Хімічна структура | |
| Формула | C21H23N7O2S |
| Мол. маса | 437,52 г/моль |
| Фармакокінетика | |
| Біодоступність | 21% (14–39%)[1] |
| Метаболізм | Печінка |
| Період напіввиведення | 30,9 год. |
| Екскреція | фекалії, Нирки (4 %) |
| Реєстрація лікарського засобу в Україні | |
| Назва, фірма-виробник, країна, номер реєстрації, дата | ВОТРІЄНТ™, «Глаксо Оперейшнс ЮК Лімітед», Велика Британія UA/12035/01/01 20.03.2017—необмежений |
Фармакологічні властивості
Пазопаніб — синтетичний лікарський засіб, який належить до групи інгібіторів протеїнтирозинкінази. Механізм дії препарату полягає в інгібуванні ферменту тирозинкінази великої кількості клітинних рецепторів. Препарат інгібує KDR, FLT4, PDGFRB, FGFR1 та FGFR3, FLT1, FLT3, c-kit, CSF1R та PDGFRA. Це призводить до інгібування ангіогенезу, який більше виражений у пухлинних тканинах, що призводить до гальмування росту пухлини.[5][6][4] Пазопаніб також інгібує фосфорилювання у клітинах організму, зокрема клітинах пухлин, що призводить до загибелі пухлинних клітин.[5][6][4] Пазопаніб застосовується у лікуванні саркоми м'яких тканин[2] та раку нирки, у тому числі з метастазуванням[3][4], причому з вищою ефективністю при більшості клінічних варіантів захворювання, та меншою кількістю побічних ефектів, у порівнянні як з хіміотерапевтичними препаратами, так і з іншими інгібіторами тирозинкінази.[2][3][4]
Фармакокінетика
Пазопаніб добре та відносно повільно всмоктується після перорального застосування, біодоступність препарату становить від 14 до 39 % у зв'язку з ефектом першого проходження препарату через печінку. Максимальна концентрація препарату в крові досягається протягом 2—4 годин після прийому препарату. Пазопаніб добре розподіляється в тканинах організму та майже повністю (на 99 %) зв'язується з білками плазми крові. Препарат проходить через плацентарний бар'єр, даних за виділення в грудне молоко людини немає. Пазопаніб метаболізується у печінці. Виводиться препарат переважно із калом, незначна частина виводиться з сечею у вигляді метаболітів. Період напіввиведення пазопанібу становить у середньому 30,9 годин, цей час може збільшуватися у хворих із порушенням функції печінки або нирок.[5][6][7]
Покази до застосування
Пазопаніб застосовують для лікування саркоми м'яких тканин та поширеного або метастатичного раку нирки.[5][6]
Побічна дія
Найчастішими побічними ефектами при застосуванні пазопанібу є діарея, артеріальна гіпертензія, зміна кольору волосся, нудота, блювання, втрата апетиту, швидка втомлюваність та астенія, кровотечі, біль у животі, головний біль, втрата ваги тіла, протеїнурія.[4] Іншими частими побічними ефектами препарату є[5][6]:
- Алергічні реакції та з боку шкірних покривів — шкірний висип, свербіж шкіри, алопеція, зміна кольору шкіри, гіпергідроз, долонно-підошовний синдром, сухість шкіри, синдром Лаєлла, фотодерматоз.
- З боку травної системи — стоматит, запор, метеоризм, гепатит, диспепсія, жовтяниця, перфорація кишки або іншого порожнистого органу, фістули порожнистих органів.
- З боку нервової системи — запаморочення, порушення смаку, транзиторна ішемічна атака, порушення мозкового кровообігу, інсульт.
- З боку серцево-судинної системи — серцева недостатність, тахікардія або брадикардія, периферичні набряки, тромбози або емболії, приливи крові, аритмії, біль у грудній клітці, зворотна серцева дисфункція зі зниженням фракції викиду, інфаркт міокарду, подовження інтервалу QT на ЕКГ.
- З боку дихальної системи — носова кровотеча, кашель, гикавка, біль у гортані, кровохаркання, втрата голосу.
- Інші побічні ефекти — гіпотиреоз, болі у м'язах і суглобах, біль у кінцівках, спазми в м'язах, біль у спині.
- Зміни в лабораторних аналізах — лейкопенія, тромбоцитопенія, нейтропенія, підвищення рівня креатиніну та сечовини в крові, підвищення рівня білірубіну, підвищення рівня активності амілази та амінотрансфераз.
Протипокази
Пазопаніб протипоказаний при підвищеній чутливості до препарату, при важкій печінковій та нирковій недостатності, при вагітності та годуванні грудьми, особам віком до 18 років.[5][6]
Примітки
- CHMP Assessment Report: Votrient (pazopanib). European Medicines Agency. Процитовано 8 жовтня 2016. (англ.)
- Пазопаніб у лікуванні сарком м'яких тканин: досвід мультидисциплінарних центрів
- Пазопаніб при нирково-клітинній карциномі пізніх стадій
- Пазопаниб — препарат первой линии терапии у больных с метастатическим раком почки (рос.)
- ВОТРІЄНТ™ (VOTRIENT™). Компендіум
- Пазопаниб (рос.)
- PAZOPanib (англ.)
- Votrient (pazopanib) dosing, indications, interactions, adverse effects, and more. Medscape Reference. WebMD. Процитовано 27 січня 2014. (англ.)
- Votrient- pazopanib hydrochloride tablet, film coated. DailyMed. 17 серпня 2020. Процитовано 9 листопада 2020. (англ.)
- Votrient : EPAR - Product Information. European Medicines Agency. Glaxo Group Ltd. 23 січня 2014. Процитовано 27 січня 2014. (англ.)
- Votrient 200 mg and 400 mg film coated tablets - Summary of Product Characteristics (SPC). electronic Medicines Compendium. GlaxoSmithKline UK. 20 грудня 2013. Процитовано 27 січня 2014. (англ.)
- Product Information Votrient Tablets (PDF). TGA eBusiness Services. GlaxoSmithKline Australia Pty Ltd. 25 березня 2013. Процитовано 27 січня 2014. (англ.)
- Активные вещества. Пазопаниб (рос.)